
【题目】对3NO2+H2O=2HNO3+NO反应的下列说法正确的是( )
A.NO2是氧化剂,H2O是还原剂
B.氧化产物与还原产物的物质的量之比为1∶2
C.氧化剂与还原剂的质量比为1∶2
D.在反应中若有6molNO2参与反应时,有3mol电子发生转移
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】工业上以铬铁矿![]() 主要成份为
主要成份为![]() ,还含有
,还含有![]() 、
、![]() 等杂质
等杂质![]() 为主要原料生产红矾钠晶体
为主要原料生产红矾钠晶体![]() ,其主要工艺流程如图:
,其主要工艺流程如图:
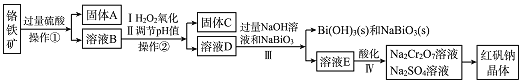
已知:![]() 在碱性条件下能将
在碱性条件下能将![]() 氧化为
氧化为![]() 。
。
![]() 固体A为 ______。
固体A为 ______。
![]() 实验室中操作
实验室中操作![]() 的名称为_____________。
的名称为_____________。
![]() 固体C中含有的物质是
固体C中含有的物质是![]()
![]() 和
和![]() ,则
,则![]() 的作用是 ______ 。
的作用是 ______ 。
已知:![]() ,
,![]() ,当
,当![]() 时
时![]() 开始沉淀.室温下,Ⅱ中需调节溶液pH范围为 ___
开始沉淀.室温下,Ⅱ中需调节溶液pH范围为 ___ ![]() 杂质离子浓度小于
杂质离子浓度小于![]() 视为沉淀完全
视为沉淀完全![]() 。
。
![]()
![]() Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是 ______
Ⅳ中酸化是用硫酸而不用盐酸酸化,理由是 ______ ![]() 结合化学方程式回答
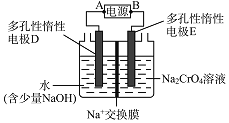
结合化学方程式回答![]() ;工业上也可设计如图示装置,用锂离子电池
;工业上也可设计如图示装置,用锂离子电池![]() 为难电离锂碳化合物
为难电离锂碳化合物![]() 为电源,电解
为电源,电解![]() 溶液制取
溶液制取![]() ,该装置工作时E电极的名称是 ___ 极;电源的A极的电极反应式为 ______
,该装置工作时E电极的名称是 ___ 极;电源的A极的电极反应式为 ______ ![]() 当电解过程中转移了
当电解过程中转移了![]() 电子时,理论上右侧溶液的质量减少 ______g。
电子时,理论上右侧溶液的质量减少 ______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】治疗癌症的有机小分子酯类药物X被批准使用。以芳香族化合物A为主要原料合成X的路线如下:
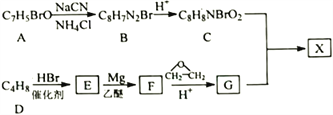
已知:
①核磁共振氢谱显示A有3种化学环境的氢,E只有1种化学环境的氢;
②![]()
③![]()
回答下列问题:
(1)A的名称是______________________;G中官能团名称是____________________。
(2)C在一定条件下反应生成高分子化合物,该反应的化学方程式为:__________________________。
(3)D生成E的反应类型为_____________________。
(4)X的结构简式为_____________________。
(5)已知:同一个碳原子若连有两个—OH时,易转化成![]() 。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
。H是C的同分异构体,写出两种满足下列要求的H的结构简式______________________。
①苯环上有两个取代基;
②能发生银镜反应,且在碱性条件下水解的两种产物也能发生银镜反应。
(6)参照上述合成路线和信息,用乙烯、乙醚、环氧乙烷为原料(其他无机试剂任选)合成1,6-己二酸_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 用石墨电极电解MgCl2溶液:Mg2++2C1-+2H2O![]() Mg(OH)2↓+Cl2↑+H2↑
Mg(OH)2↓+Cl2↑+H2↑
B. 向明矾溶液中滴加碳酸钠溶液:2Al3++3CO32-==Al2(CO3)3↓
C. 向Ca(HCO3)2溶液中滴加少最NaOH溶液:Ca2++2HCO3-+2OH-==CaCO3↓+CO32-+2H2O
D. 向Fe(NO3)3溶液中加入过量的HI溶液:2NO3-+8H++6I-==3I2+2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 mol NaOH固体溶于1 L水中,所得溶液的物质的量浓度为1 mol/L
B.40 g NaOH固体溶于100 g水中,所得溶液中溶质的质量分数为40%
C.标准状况下,22.4 L HCl气体溶于水中配成1 L溶液,所得溶液的物质的量浓度为1 mol/L
D.1 L物质的量浓度相同的溶液,所含溶质的质量一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,下列实验用如图所示装置不能完成的是 ( )
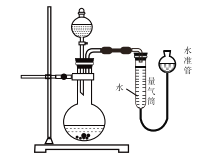
A. 测定一定质量的![]() 和
和![]() 混合物中
混合物中![]() 的含量
的含量
B. 确定分子式为![]() 的有机物分子中含活泼氢原子的个数
的有机物分子中含活泼氢原子的个数
C. 测定一定质量的![]() 晶体中结晶水数目
晶体中结晶水数目
D. 比较Fe3+和Cu2+对一定质量的双氧水分解反应的催化效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3+5O2![]() 4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
A.4v(NH3)=5v(O2)B.5v(O2)=6v(H2O)
C.4v(NH3)=6v(H2O)D.4v(O2)= 5v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在25℃、1.01×105Pa时,16g硫粉在足量的氧气中充分燃烧生成二氧化硫气体,放出148.5kJ的热量,则S的燃烧热的热化学方程式为:_____________________。
(2)1L 1mol/L稀盐酸跟1L 1mol/L NaOH溶液起中和反应放出57.3kJ热量,其中和热的热化学方程为:________________。
(3)已知如图所示的可逆反应:

①A(g)+B(g)![]() 2C(g) +D(g);ΔH = Q kJ/mol则Q_______0(填“>”、“<”或“=”)
2C(g) +D(g);ΔH = Q kJ/mol则Q_______0(填“>”、“<”或“=”)
②反应体系中加入催化剂,反应速率增大,则E1的变化是: E1_______,ΔH的变化是:ΔH________(填“增大”“减小”“不变”)。
(4)发射卫星用![]() 作燃料,
作燃料,![]() 作氧化剂,两者反应生成N2和水蒸气,已知:N2(g) +2O2(g)= 2NO2(g)△H1 =+67.7kJ/mol;N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol,则1mol气体肼和NO2完全反应时的反应热△H=____________kJ/mol。
作氧化剂,两者反应生成N2和水蒸气,已知:N2(g) +2O2(g)= 2NO2(g)△H1 =+67.7kJ/mol;N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol,则1mol气体肼和NO2完全反应时的反应热△H=____________kJ/mol。
(5)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①.v(A)=0.15mol/(Ls) ②.v(B)=0.6mol/(Ls)③.v(C)=0.4mol/(Ls) ④.v(D)=0.45mol/(Ls)则该反应进行最快的为________(填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B. Na2O2与CO2反应生成0.1 mol O2时转移电子0.4 mol
C. Na2O2投入到CuCl2溶液中有蓝色沉淀及气泡产生
D. 向饱和烧碱溶液中加入2 g Na2O2,充分反应完后,溶液中c(Na+)不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com