
【题目】现有中学化学常见的物质,其中甲、乙、丙是单质,甲为第三周期金属,A、B、C、D、E、F是化合物,B是红棕色气体,C在常温下是无色无味液体,甲元素的原子序数是丙元素原子序数的2倍,它们之间有如图所示的相互转化关系(部分反应条件已略去).
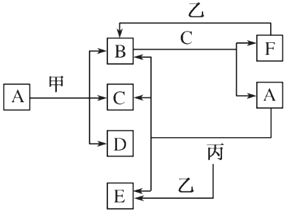
(1)B的化学式为 ,D的化学式为 .
(2)写出A与丙反应的化学方程式: .
(3)工业上制取A分三步进行,其中两步反应已经在图中得到体现,写出另外一步反应的化学方程式: .
(4)若9.6g甲与一定量A浓溶液完全反应后,生成标准状况下的8.96L气体中含有的B和F,且甲无剩余,则B和F的物质的量之比为 .
【答案】(1)NO2;Mg(NO3)2;
(2)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(3)4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(4)1:1.
【解析】
试题分析:B是红棕色气体,B是NO2;C在常温下是无色无味液体,则C为H2O,甲为第三周期金属,甲元素的原子序数是丙元素原子序数的2倍,甲的原子序数为偶数,则原子序数为12,即甲为Mg,则丙为C;结合转化可知,A溶液是浓硝酸,则D为Mg(NO3)2,B与C生成F,F为NO,F与乙生成B,则乙为O2,由丙和A的反应C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O可知,E为CO2,以此来解答.
CO2↑+4NO2↑+2H2O可知,E为CO2,以此来解答.
解:B是红棕色气体,B是NO2;C在常温下是无色无味液体,则C为H2O,甲为第三周期金属,甲元素的原子序数是丙元素原子序数的2倍,甲的原子序数为偶数,则原子序数为12,即甲为Mg,则丙为C;结合转化可知,A溶液是浓硝酸,则D为Mg(NO3)2,B与C生成F,F为NO,F与乙生成B,则乙为O2,由丙和A的反应C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O可知,E为CO2,
CO2↑+4NO2↑+2H2O可知,E为CO2,
(1)由上述分析可知,B为NO2,D为Mg(NO3)2,故答案为:NO2;Mg(NO3)2;
(2)A与丙反应的化学方程式为C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O;
CO2↑+4NO2↑+2H2O;
(3)制取A分三步进行,氨气的催化氧化、NO氧化生成二氧化氮、二氧化氮与水反应生成硝酸,则除图中转化外的另外一步反应的化学方程式为4NH3+5O2![]() 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(4)n(Mg)=![]() =0.4mol,8.96L气体中含有的B和F,气体的物质的量为
=0.4mol,8.96L气体中含有的B和F,气体的物质的量为![]() =0.4mol,Mg完全反应,设B和F的物质的量分别为x、y,由电子守恒及原子守恒可知,
=0.4mol,Mg完全反应,设B和F的物质的量分别为x、y,由电子守恒及原子守恒可知,![]() ,解得x=0.2mol,y=0.2mol,所以B和F的物质的量之比为1:1,故答案为:1:1.
,解得x=0.2mol,y=0.2mol,所以B和F的物质的量之比为1:1,故答案为:1:1.


科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 稀盐酸 | CaCO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
B | 浓硫酸 | 蔗糖 | Ba(NO3)2溶液 | 验证SO2与可溶性钡盐可生成白色沉淀 |
C | 浓氨水 | 生石灰 | 酚酞溶液 | 氨气的水溶液呈碱性 |
D | 浓硝酸 | Fe | NaOH溶液 | 铁和浓硝酸反应可生成NO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32﹣、SO42﹣、Cl﹣中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )

A. 原溶液一定存在CO32﹣和SO42﹣,一定不存在Fe3+
B. 原溶液一定存在Cl﹣,可能存在Na+
C. 原溶液中c(Cl﹣)≥0.1molL﹣1
D. 若原溶液中不存在Na+,则c(Cl﹣)<0.1molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙晶体CaO2·8H2O不溶于水,遇水缓慢地分解,放出氧气,是一种用途广泛的优良供氧剂,某学习小组欲利用工业废渣CaCl2(含生石灰和熟石灰)制取CaO2·8H2O,发现用Ca(OH)2和H2O2直接反应,生成杂质较多,按下列方法制取过氧化钙晶体,请回答:
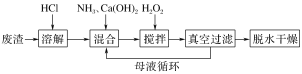
下列说法不正确的是( )
A.Ca(OH)2的主要作用是调节溶液酸碱性和循环母液反应产生氨气
B.为了加快反应,搅拌时应该在较低温度下进行
C.真空过滤的目的是加快过滤,减少和水反应
D.搅拌步骤中加入了双氧水,发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CO2、H2为原料合成乙烯的方程式为:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在常压下,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应。测得温度对CO2的平衡转化率和催化剂催化效率影响情况如下图所示。
C2H4(g)+4H2O(g) ΔH。在常压下,按n(CO2)∶n(H2)=1∶3(总物质的量为4a mol)的投料比充入密闭容器中发生反应。测得温度对CO2的平衡转化率和催化剂催化效率影响情况如下图所示。
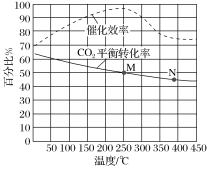
①下列说法不正确的是________。
A ΔH<0;平衡常数:KM<KN
B 改用其他催化剂,如果能加快反应速率,可能影响平衡转化率
C 若投料比改为n(CO2)∶n(H2)=3∶1,可以提高CO2的平衡转化率
D 250 ℃时,催化效率最高,但不是最佳反应温度
②250 ℃下,上述反应达平衡时容器体积为V L,则此温度下该反应的平衡常数为________(用含a、V的代数式表示)。
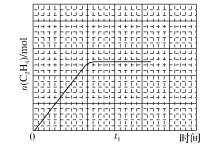
③某温度下,n(C2H4)随时间(t)的变化趋势曲线如图所示。其它条件相同时,若容器的体积为其一半,画出0~t1时刻n(C2H4)随时间(t)的变化趋势曲线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列热化学方程式的书写正确的是
①CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol1
CO2(g)+2H2O(l) ΔH=+890.3 kJ·mol1
②CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=890.3 kJ·mol1
CO2(g)+2H2O(l) ΔH=890.3 kJ·mol1
③CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) ΔH=890.3 kJ·mol1
CO2(g)+2H2O(g) ΔH=890.3 kJ·mol1
④2H2(g)+O2(g)![]() 2H2O(l) ΔH=571.6 kJ·mol1
2H2O(l) ΔH=571.6 kJ·mol1
A. 仅有② B. 仅有②④ C. 仅有②③④ D. 全部符合要求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉和油脂为原料,制备生活中的某些物质。
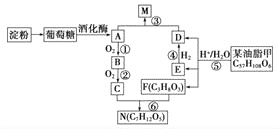
已知:反应![]() 生成D、E、F的物质的量之比为
生成D、E、F的物质的量之比为![]() ,E与等物质的量的
,E与等物质的量的![]() 反应生成D。请回答下列问题:
反应生成D。请回答下列问题:
![]() 葡萄糖的分子式为________,C分子中官能团的名称为________。
葡萄糖的分子式为________,C分子中官能团的名称为________。
![]() 下列说法正确的是________。
下列说法正确的是________。
A.淀粉、油脂都是高分子化合物,都能发生水解反应
B.C、D属于同系物;M、N也属于同系物
C.上述![]() 中属于取代反应的为
中属于取代反应的为![]()
D.B、E含不同官能团,但都能使酸性高锰酸钾溶液褪色
![]() 写出N的一种结构简式:_________________________;C与F按不同的比例反应,还可以生成另外两种物质X、Y,且相对分子质量
写出N的一种结构简式:_________________________;C与F按不同的比例反应,还可以生成另外两种物质X、Y,且相对分子质量![]() ,则Y的分子式为________。
,则Y的分子式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如下图所示。

已知:I 在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II相关金属离子形成氢氧化物沉淀的pH范围如下:
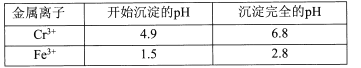
回答下列问题:
(l)滤渣②的主要成分为____(填化学式)。
(2)写出“氧化”步骤中反应的化学方程式____。
(3)“加热”操作的目的是____。
(4)“酸化”过程中发生反应2CrO42-+2H+![]() Cr2O72-+H2O (K=4×1014L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=____
Cr2O72-+H2O (K=4×1014L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=____
(5)“结晶”后得到K2Cr2O7(M=294g.mol-1)产品0.5000 g,将其溶解后用稀H2SO4酸化,再用浓度为1.0000 mol.L-l (NH4)2Fe(SO4)2 标准溶液滴定,滴定终点消耗标准溶液的体积为9.00 mL,则产品的纯度为____。[滴定反应为:K2Cr2O7+6(NH4)2Fe(SO4)2+7H2SO4 =K2SO4 +Cr2(SO4)3 +6(NH4)2SO4+3Fe2(SO4)3+7H2O]
(6)在K2Cr2O7存在下,可利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如下图所示。

①负极的电极反应式为____;
②一段时间后,中间室中NaCl溶液的浓度____(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O和CO是环境污染性气体,可在Pt2O+ 表面转化为无害气体,其反应原理为N2O(g) + CO(g)![]() CO2(g) + N2(g) ΔH,有关化学反应的物质变化过程及能量变化过程如下。下列说法不正确的是
CO2(g) + N2(g) ΔH,有关化学反应的物质变化过程及能量变化过程如下。下列说法不正确的是
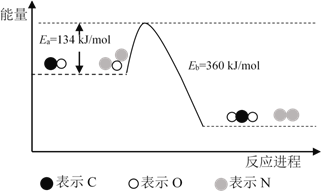
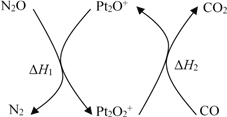
A. ΔH = ΔH1 + ΔH2
B. ΔH = 226 kJ/mol
C. 该反应正反应的活化能小于逆反应的活化能
D. 为了实现转化需不断向反应器中补充 Pt2O+ 和 Pt2O2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com