
【题目】磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。一种回收废旧磷酸亚铁锂电池正极片(主要成分LiFePO4、炭黑和铝箔)中金属的流程如下:

(1)步骤①中“碱溶”反应的化学方程式为_____。
(2)步骤②中反应的离子方程式为_____。若用H2O2代替HNO3,其优点是_____。
(3)步骤③沉淀的主要成分是_____。
(4)步骤④中生成含Li沉淀_____(填“能”或“不能”)用硫酸钠代替碳酸钠,原因是_____。
【答案】2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4] 3LiFePO4+NO3﹣+13H+=3Li++3Fe3++3H3PO4+NO↑+2H2O 不产生氮氧化物大气污染物 Fe(OH)3 不能 硫酸锂易溶于水,不能形成含锂沉淀 。
【解析】
步骤①中“碱溶”反应的化学方程式为2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4],过滤分离出铝元素,步骤②滤渣中加入氧化性酸硝酸,将亚铁离子氧化为铁离子,强酸制弱酸有磷酸生成,产物为Li+、Fe3+、H3PO4、NO,加入碱液,铁离子生成Fe(OH)3沉淀,过滤分离出铁元素,滤液中加入碳酸钠,生成碳酸锂沉淀。
(1)步骤①中“碱溶”反应的化学方程式为2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4];
答案:2Al+2NaOH+6H2O=3H2↑+2Na[Al(OH)4]。
(2)步骤②中反应的离子方程式为3LiFePO4+NO3﹣+13H+=3Li++3Fe3++3H3PO4+NO↑+2H2O,若用H2O2代替HNO3,其优点是不产生氮氧化物大气污染物;
答案:3LiFePO4+NO3﹣+13H+=3Li++3Fe3++3H3PO4+NO↑+2H2O;不产生氮氧化物大气污染物。
(3)由以上分析可知步骤③沉淀的主要成分是Fe(OH)3;
答案:Fe(OH)3。
(4)硫酸锂易溶于水,不能用硫酸钠代替碳酸钠;
答案:不能;硫酸锂易溶于水,不能形成含锂沉淀。


科目:高中化学 来源: 题型:
【题目】
丹参素是中药丹参的水溶性成分,结构为 F ,具有扩张血管、增加冠脉血流量等作用,某一种合成路线如下图所示:

已知:![]()
![]()
(1)丹参素的分子式为____________; D →E 的反应类型是_______________。
(2)试剂X是____________(写化学式);C 中含氧官能团名称为_____________。
(3) A→B 的反应方程式为________________。
(4)G与 E互为同分异构体,请写出满足下列条件的任意两种G的结构简式______________。
①lmolG 能与4molNaOH发生反应;
②能够发生水解反应;
③核磁共振氢谱显示5个吸收峰,且峰面积之比为 1 : 2 : 2 : 2 : 3 。
(5)参考上述流程信息,设计以![]() 、CH3CHO为原制取
、CH3CHO为原制取![]() 的合成路线(其它无机试剂任选)。________________
的合成路线(其它无机试剂任选)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列对该化合物的说法中,正确的是( )

A. 名称是乙醚
B. 只含有一种官能团
C. 链状同分异构体中,属于羧酸的有3种
D. 既能发生加聚反应,又能发生缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2L的刚性密闭容器中,加入1mol CO2和3mol H2,发生反应CO2+3H2CH3OH+H2O.在其他条件不变的情况下,温度对反应的影响结果如图所示(注:T1、T2均大于300℃)。下列说法正确的是

A. 该反应在T1时的平衡常数比T2时的小
B. 处于A点的反应体系从T1变到T2,达到平衡时![]() 减小
减小
C. T2下,反应达到平衡时生成甲醇的平均速率为v(CH3OH)=![]() molL﹣1min﹣1
molL﹣1min﹣1
D. T1下,若反应达到平衡后CO2转化率为a,则容器内的压强与起始压强之比为(2﹣a):2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为一种特殊的热激活电池示意图,当无水LiCl-KCl混合物受热熔融后即可工作。 该电池总反应为: PbSO4(s)+2LiCl+Ca(s) = CaCl2(s)+Li2SO4+Pb(s)。下列说法不正确的是
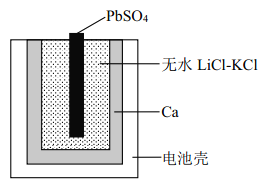
A. PbSO4 电极发生还原反应
B. 负极的电极反应:Ca + 2Cl--2e-=CaCl2
C. 放电时 Li+、 K+向正极移动
D. 用 LiCl 和 KCl 水溶液代替无水 LiCl-KCl,可将该电池改为常温使用的电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于元素周期表的说法正确的是( )
A. 元素周期表有7个周期,8个主族
B. 元素周期表有18个纵行,共16个族
C. 短周期元素中可能有副族元素
D. 在元素周期表中的金属元素和非金属元素交界处最容易找到优良的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数 K=2×10-5。已知:Ni(CO)4的沸点为 42.2℃,固体杂质不参与反应。第一阶段:将粗镍与 CO 反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是
Ni(CO)4(g)。230℃时,该反应的平衡常数 K=2×10-5。已知:Ni(CO)4的沸点为 42.2℃,固体杂质不参与反应。第一阶段:将粗镍与 CO 反应转化成气态Ni(CO)4;第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。下列判断正确的是
A. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
B. 增大c(CO),平衡正向移动,反应的平衡常数增大
C. 第二阶段,Ni(CO)4分解率较低
D. 增加Ni的含量,CO的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“H2O(l)→H2O(g)→H2和O2”的变化过程中,被破坏的作用力依次是
A. 分子间作用力、离子键B. 分子间作用力、共价键
C. 共价键、离子键D. 共价键、共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com