
【题目】单晶硅是信息产业中重要的基础材料。通常用焦炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
相关信息如下:
a.四氯化硅遇水极易水解;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
物 质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
沸点/℃ | 57.7 | 12.8 | - | 315 | - |
熔点/℃ | -70.0 | -107.2 | - | - | - |
升华温度/℃ | - | - | 180 | 300 | 162 |
请回答下列问题:
(1)写出装置A中发生反应的离子方程式。
(2)装置A中g管的作用是;装置C中的试剂是;装置E中的h瓶需要冷却的理由是。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是(填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成
Fe2+ , 再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?(填“是”或“否”),请说明理由。
②某同学称取5.000g残留物,经预处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00mL,则残留物中铁元素的质量分数是。
【答案】
(1)MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(2)平衡压强;浓硫酸;使SiCl4冷凝
(3)Al、P、Cl
(4)①否;KMnO4溶液自身可作指示剂;②4.480%
【解析】 (1)A装置是制备Cl2的,注意要求写的是MnO2与浓盐酸的“离子方程式”。(2)装置A中“g”管的作用是“使分液漏斗与圆底烧瓶压强保持一致,便于液体顺利滴下”,简单说就是“平衡压强”。B是除杂装置,除去Cl2中的HCl气体,C就是干燥装置。干燥Cl2一般用浓硫酸。由于反应温度是450~500℃,此时SiCl4是气体,而题目表格中SiCl4通常应是液态的,故装置E中h瓶需要冷却的理由应是便于分离得到SiCl4。(3)根据已知条件AlCl3、FeCl3、PCl5都会在精馏后的残留物中存在,注意要先答上Cl,容易遗漏。(4)①由于紫色的KMnO4溶液反应后颜色会褪去,所以不用滴加指示剂。②根据KMnO4的用量计算出Fe2+的用量,再算其质量分数,属于典型的常见计算。


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:
【题目】固体D是一种红色氧化物. 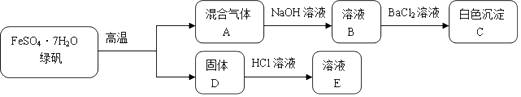
(1)混合气体A通入足量NaOH溶液后,溶液B中属于盐的溶质有 .
(2)白色沉淀C中加入盐酸的实验现象为 .
(3)固体D与HCl溶液反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微粒间的作用力主要有离子键、共价键、金属键(存在于金属单质与合金中)、一般的 分子间作用力和氢键,下列各组物质中,所含有的相互作用力类型最多的一组是
A. Na2O2 Na2OB. KClO CO2C. K HBrD. HF NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10﹣13 , 下列说法错误的是( ) 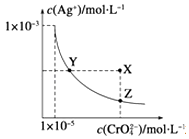
A.t℃时,Ag2CrO4的Ksp为1×10﹣8
B.在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C.一定温度下Y点和Z点时Ag2CrO4的Ksp相等
D.在t℃时,Ag2CrO4(s)+2Br﹣(aq)2AgBr(s)+CrO42﹣(aq)平衡常数K=4.0×1010
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝基甲苯有领、间、对三种,其中对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备.一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐(有脱水作用),45℃反应1h.反应结束后,过滤,滤液分别用5%NaHCO3 , 溶液、水洗至中性,再经分离提纯得到对硝基甲苯.
请回答下列问题:
(1)仪器B的名称是 , 其作用是
(2)过滤在分液漏斗中洗涤静后,有机层处于层(填“上”或“下”)放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有 .
(3)上述新的试验方法中过滤的目的是 , 滤液用5%NaHCO3溶液洗涤的原因是 .
(4)下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果.
催化剂 | n(催化剂) | 硝化产物中各种异构体质量分数(%) | 总产率 | ||
n(甲苯) | 对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | ||
浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 82.0 |
1.2 | 36.5 | 59.2 | 4.0 | 83.8 | |
NaHSO4 | 0.25 | 46.3 | 52.8 | 0.9 | 92.8 |
0.32 | 48.0 | 51.7 | 0.3 | 95.0 | |
0.36 | 45.0 | 54.4 | 0.6 | 93.9 | |
催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为 , 此时若使用13.0g甲苯,分离出对硝基甲苯的质量是g(保留一位小数).
②由表中数据可知甲苯硝化主要得到对硝基甲苯和邻硝基甲苯,原因是 .
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优有(回答一条)
④对硝基甲苯和邻硝基甲苯的部分物理特性如表:
密度/gcm﹣3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |

其中,操作1的名称为;操作2中需要使用下列仪器中的(填序号).
A.冷凝管 B.酒精灯 C.温度计 D.分液漏斗 E.蒸发皿.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2俗称双氧水,医疗上常用3%的双氧水进行伤口或耳炎消毒。下列关于H2O2的说法正确的是( )
A. H2O2分子中含有氢离子
B. H2O2分子中既有离子键,又有共价键
C. H2O2属于共价化合物
D. H2O2属于H2和O2组成的混合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是合成某种耐热聚合物的单体,其合成方法如下: 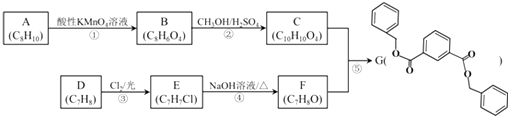
已知:R1COOR2+R3OH ![]() RCOOR3+R2OH
RCOOR3+R2OH
(1)根据系统命名法,A的名称为 .
(2)上述流程中的取代反应除②、③外还有(填序号).第⑤步反应中,可使用含有18O的F,将之与C反应,并检测产物中18O的分布情况,从而推断反应机理,这种研究方法称为 .
(3)化合物E的核磁共振氢谱图中共有多个吸收峰,各峰的峰面积比为 .
(4)按下列合成路线可得到F的同分异构体H,则可鉴别H与F的试剂是 . 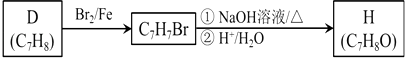
(5)C与足量NaOH溶液反应的化学方程式为 .
(6)J与C互为同分异构体,其具有如下性质.符合要求的有机物有种(不考虑立体异构)
①能与NaOH溶液反应,且1mol J完全反应消耗4mol NaOH
②能发生银镜反应,且1mol J与足量的银氨溶液反应生成4mol Ag
③分子中苯环上的一氯取代物只有一种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是工业利用铝土矿(含杂质SiO2、Fe2O3)制取铝的工艺流程,回答有关问题: 
(1)铝土矿磨碎化浆,利用胶体粒子的性质,通入直流电除去 , 制得50%铝土矿.
(2)操作I的名称是 , 实验室进行此操作所需玻璃仪器为 .
(3)加入NaOH所发生的离子反应方程式为 , 滤渣一为(填化学式).
(4)电解槽用石墨作阳极,生成二氧化碳的原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com