
【题目】结构决定性质,研究物质的组成、结构对于学习物质的性质至关重要。
(1)如图中每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点、b点分别代表的是 ___________、___________ (写化学式),a比b的沸点高的原因是__________________________________。

(2)在超高压下,科学家用激光器将CO2加热到1800K,成功制得了类似石英的CO2原子晶体。由此推测该CO2晶体中O—C—O键角为__________,与石英相比该晶体的熔点、沸点________(“更高”或“更低”),理由是_________________________________。
(3)利用铜萃取剂M可通过如下反应实现铜离子的富集:


①M所含元素的电负性由大到小顺序为____,其中氮原子以__轨道与氧原子形成σ键。
②M与W(右图)相比,M的水溶性较小,更利于Cu2+的萃取。M水溶性较小的主要原因是___________________________________。
(4)常用![]() 表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为
表示分子中的大π键,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,例如苯分子中的大π键可表示为![]() 。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为________,吡咯分子中N原子的杂化类型为 ________,1mol吡咯分子中所含的σ键数目为________。
。已知吡咯(下图)中的各个原子均在同一平面内且吡咯分子中也含有大π键,请问:吡咯分子中的大π键应表示为________,吡咯分子中N原子的杂化类型为 ________,1mol吡咯分子中所含的σ键数目为________。
【答案】 H2O HF 水分子间形成的氢键数目较多 10928ˊ 更高 C原子半径较小,C-O键键长较短,键能较大 O>N>C>H sp2杂化 M能形成分子内氢键,使溶解度减小 ![]() sp2 10NA
sp2 10NA
【解析】(1)a点、b点对应是第二周期IVA~VIIA族元素的氢化物,第二周期IVA~VIIA族元素的氢化物依次为CH4、NH3、H2O、HF,NH3、H2O、HF分子间都存在氢键,氢键的强度:NH3分子间氢键![]() H2O分子间氢键
H2O分子间氢键![]() HF分子间氢键,水分子间形成的氢键的数目比HF分子间形成氢键数目多,沸点:CH4
HF分子间氢键,水分子间形成的氢键的数目比HF分子间形成氢键数目多,沸点:CH4![]() NH3
NH3![]() HF
HF![]() H2O(H2O的沸点为100℃),a点代表H2O,b点代表HF。
H2O(H2O的沸点为100℃),a点代表H2O,b点代表HF。
(2)CO2原子晶体类似石英,CO2晶体中O—C—O键角为10928ˊ。与石英相比,该晶体的熔点、沸点更高,因为:C原子半径较小,C-O键键长较短,键能较大。
(3)①M中的元素有C、H、O、N,四种元素电负性由大到小的顺序为O![]() N
N![]() C
C![]() H。M中N原子形成1个C=N键和1个N-O键,N原子上还有1对孤电子对,N原子为sp2杂化。
H。M中N原子形成1个C=N键和1个N-O键,N原子上还有1对孤电子对,N原子为sp2杂化。
②W能与H2O分子间形成氢键,M形成分子内氢键,使溶解度减小。
(4)吡咯分子中的各个原子均在同一平面内,吡咯分子中C和N都采用sp2杂化,每个C原子未参与杂化的2p轨道上有1个电子,N原子的sp2杂化轨道形成1个N-H键和2个N-C键,N原子的未参与杂化的2p轨道上有2个电子,吡咯中形成大π键的原子为4个C原子和1个N原子,形成大π键的电子数为4+2=6个。1个吡咯分子中含10个σ键。
(1)a点、b点对应是第二周期IVA~VIIA族元素的氢化物,第二周期IVA~VIIA族元素的氢化物依次为CH4、NH3、H2O、HF,NH3、H2O、HF分子间都存在氢键,氢键的强度:NH3分子间氢键![]() H2O分子间氢键
H2O分子间氢键![]() HF分子间氢键,水分子间形成的氢键的数目比HF分子间形成氢键数目多,沸点:CH4
HF分子间氢键,水分子间形成的氢键的数目比HF分子间形成氢键数目多,沸点:CH4![]() NH3
NH3![]() HF
HF![]() H2O(H2O的沸点为100℃),a点代表H2O,b点代表HF。H2O比HF沸点高的原因是:水分子间形成的氢键的数目比HF分子间形成氢键数目多。
H2O(H2O的沸点为100℃),a点代表H2O,b点代表HF。H2O比HF沸点高的原因是:水分子间形成的氢键的数目比HF分子间形成氢键数目多。
(2)CO2原晶体类似石英,其中C原子与4个O原子形成4个C—O键,CO2晶体中O—C—O键角为10928ˊ。与石英相比,该晶体的熔点、沸点更高,因为:CO2原子晶体和石英都属于原子晶体,C原子半径较小,C-O键键长较短,键能较大。
(3)①M中的元素有C、H、O、N,非金属性O![]() N
N![]() C
C![]() H,四种元素电负性由大到小的顺序为O
H,四种元素电负性由大到小的顺序为O![]() N
N![]() C
C![]() H。M中N原子形成1个C=N键和1个N-O键,N原子上还有1对孤电子对,N原子为sp2杂化,N原子以sp2杂化轨道与氧原子形成σ键。
H。M中N原子形成1个C=N键和1个N-O键,N原子上还有1对孤电子对,N原子为sp2杂化,N原子以sp2杂化轨道与氧原子形成σ键。
② W能与H2O分子间形成氢键,M形成分子内氢键,使溶解度减小,M的水溶性更小。
(4)吡咯分子中的各个原子均在同一平面内,吡咯分子中C和N都采用sp2杂化,每个C原子未参与杂化的2p轨道上有1个电子,N原子的sp2杂化轨道形成1个N-H键和2个N-C键,N原子的未参与杂化的2p轨道上有2个电子,吡咯中形成大π键的原子为4个C原子和1个N原子,形成大π键的电子数为4+2=6个,吡咯中的大π键应表示为![]() ,吡咯分子中N原子为sp2杂化。1个吡咯分子中含10个σ键(3个碳碳σ键、2个碳氮σ键、4个碳氢σ键和1个氮氢σ键),1mol吡咯分子中所含σ键为10NA。
,吡咯分子中N原子为sp2杂化。1个吡咯分子中含10个σ键(3个碳碳σ键、2个碳氮σ键、4个碳氢σ键和1个氮氢σ键),1mol吡咯分子中所含σ键为10NA。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA。关于1mol H2O的叙述正确的是
A.含有1mol H2B.含有NA个水分子
C.质量为18 g/molD.在标准状况下的体积为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A. ![]() 和
和![]() 为同系物 B. 乙醇和乙醚互为同分异构体
为同系物 B. 乙醇和乙醚互为同分异构体
C. 可用浓溴水来区分乙醇和苯酚 D. 甲醇、乙二醇、丙三醇互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现以CO、O2、熔融盐Z(Na2CO3)组成的燃料电池,采用电解法处理CO同时制备N2O5,装置如图所示,其中Y为CO2。下列说法不合理的是( )
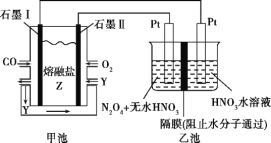
A. 石墨Ⅰ是原电池的负极,发生氧化反应
B. 甲池中的CO32-向石墨Ⅱ极移动
C. 乙池中左端Pt极电极反应式:N2O4-2e-+2HNO3![]() 2N2O5+2H+
2N2O5+2H+
D. 若甲池消耗标准状况下的氧气2.24 L,则乙池中产生氢气0.05 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~J均为有机化合物,它们之间的转化如下图所示:

实验表明:①D既能发生银镜反应,又能与金属钠反应放出氢气:
②核磁共振氢谱表明F分子中有三种氢,且其峰面积之比为1:1:1;
③G能使溴的四氯化碳溶液褪色;④1mol J与足量金属钠反应可放出22.4L氢气(标准状况)。
请根据以上信息回答下列问题:
(1)A的结构简式为____________(不考虑立体结构),由A生成B的反应类型是____________反应;
(2)D的结构简式为_____________;
(3)由E生成F的化学方程式为_______________,E中官能团有_________(填名称),与E具有相同官能团的E的同分异构体还有________________(写出结构简式,不考虑立体结构);
(4)G的结构简式为_____________________;
(5)由I生成J的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾是一种常见的化合物,工业上它也是一种制取其它含铜化合物的原料。现有废铜(主要杂质为Fe)来制备胆矾。有人设计了如下流程:
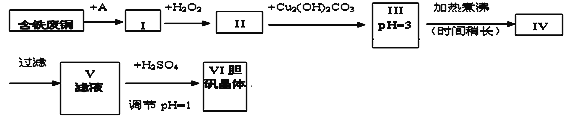
pH值控制可参考下列数据
物 质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
氢氧化铁 | 2.7 | 3.7 |
氢氧化亚铁 | 7.6 | 9.6 |
氢氧化铜 | 5.2 | 6.4 |
请根据上述流程回答下列问题:
(1)A物质可选用_____(填字母)。
a.稀H2SO4 b.浓H2SO4/△ c.浓FeCl3溶液 d.浓HNO3
(2)I中加H2O2的离子方程式________________________________________。
(3)II中加Cu2(OH)2CO3的目的是________________________;其优点是__________。
(4)III加热煮沸时发生的化学反应的离子方程式为________________________。
(5)V中加H2SO4调节pH=1是为了____________________________________________。
(6)V到VI的操作是_________________________________
(7)某同学认为上述流程中所加的A物质并不理想,需作改进,其理由是__________。如何改进___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用科学技术减少氮氧化物、SO2等物质的排放,可促进社会主义生态文明建没。
(1)采用“联合脱硫脱氮技术”处理烟气(含CO2、SO2、NO)可获得含CaCO3、CaSO4.Ca(NO3)2的副产品,工业流程如题20图一l所示。

①反应釜I采用“气一液逆流”接触吸收法(如题20图-2),其优点是________________。
②反应釜Il中CaSO3转化为CaSO4的化学反应方程式为 ___________________________。
(2)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。写出电解时阳极的电极反应式:____________________________________。
(3)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90s的情况下,测得不同条件下NO的脱氮率如图I、Ⅱ所示。

① 由图I知,当废气中的NO含量增加时,宜选用______法提高脱氮的效率。
② 图Ⅱ中,循环吸收液加入Fe2+、Mn2+,提高了脱氮的效率,其可能原因为________。
(4)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。
①温度高于60℃后,NO去除率下降的原因为__________。
②写出废气中的SO2与NaC1O2反应的离子方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某透明溶液中,能大量共存的离子组是( )
A.K+、MnO4-、SO42-B.Ba2+、Cl-、SO42-
C.Na+、CO32-、H+D.OH-、Na+、Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com