
【题目】已知:A是石油裂解气的主要成分,A的产量通常用来衡量一个国家的石油化工发展水平;它有如图所示的转化关系。E是有香味的有机物,F是高分子化合物(已知醛类氧化可生成羧酸)。
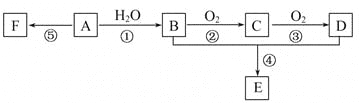
(1)B、D分子中的官能团名称分别是_________、_________。
(2)写出下列反应的化学方程式及反应类型:
①________;反应类型________。②________;反应类型________。
④________;反应类型________。⑤________;反应类型________。
【答案】羟基 羧基 CH2=CH2+H2O![]() CH3CH2OH 加成反应 2CH3CH2OH+O2
CH3CH2OH 加成反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应 CH3COOH+CH3CH2OH
2CH3CHO+2H2O 氧化反应 CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 酯化(或取代)反应
CH3COOCH2CH3+H2O 酯化(或取代)反应 ![]() 加聚反应
加聚反应
【解析】
由题意知,A为CH2=CH2,水化加成为CH3CH2OH,CH3CH2OH连续氧化为CH3CHO、CH3COOH,CH3CH2OH和乙酸酯化为CH3COOCH2CH3;CH2=CH2发生加聚生成![]() ,结合以上各物质的性质进行分析。
,结合以上各物质的性质进行分析。
由题意知,A、B、C、D、E、F分别为CH2=CH2、CH3CH2OH、CH3CHO、CH3COOH、CH3COOCH2CH3、![]() ,
,
(1)B为CH3CH2OH,D为CH3COOH,分子中分别含有羟基和羧基官能团;
(2)①、②、④、⑤反应的化学方程式及反应类型分别为:
①CH2=CH2+H2O![]() CH3CH2OH,加成反应;
CH3CH2OH,加成反应;
②2CH3CH2OH+O2![]() 2CH3CHO+2H2O,氧化反应;
2CH3CHO+2H2O,氧化反应;
④CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O,酯化(或取代)反应;
CH3COOCH2CH3+H2O,酯化(或取代)反应;
![]() ,加聚反应。
,加聚反应。


科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管桩,常用外加电流的阴极保护法进行防腐,工作原理如图所示,下列有关表述错误的是
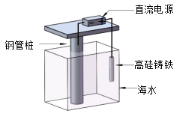
A.利用了电解原理
B.钢管桩上有刺激性气味气体生成
C.电子由电源负极流向钢管桩
D.高硅铸铁作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下存在反应:2SO2(g)+ O2(g)![]() 2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,并在400℃条件下开始反应,达到平衡时,下列说法正确的是( )
2SO3(g) △H<0。现有三个体积相同的密闭容器Ⅰ、Ⅱ、Ⅲ,并在400℃条件下开始反应,达到平衡时,下列说法正确的是( )

A.容器I、Ⅲ中平衡常数相同
B.容器II、Ⅲ中正反应速率始终相同
C.容器Ⅱ、Ⅲ中的反应达平衡时,SO3的转化率:II>III
D.容器I中SO2的转化率与容器Ⅱ中SO3的转化率之和小于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中科院科学家设计出一套利用SO2和太阳能综合制氢方案,其基本工作原理如图所示,下列说法错误的是( )

A. 该电化学装置中,Pt电极作正极
B. BiVO4电极上的反应式为SO32--2e-+2OH=SO42-+H2O
C. 电子流向:Pt电极→导线→BiVO4电极→电解质溶液→Pt电极
D. Pt电极的电势高于BiVO4电极的电势
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雄黄![]() 酒,即是用研磨成粉末的雄黄泡制的白酒或黄酒,中华民族传统节日端午节的饮品。雌黄
酒,即是用研磨成粉末的雄黄泡制的白酒或黄酒,中华民族传统节日端午节的饮品。雌黄![]() 是工业制取高纯度砷的重要原料,下图是工业制纯砷流程:
是工业制取高纯度砷的重要原料,下图是工业制纯砷流程:
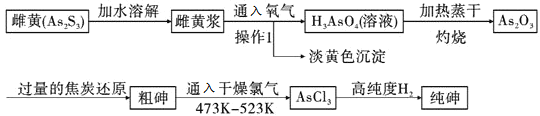
已知:砷在元素周期表中,位于硅元素相邻的右下角位置。
![]() 操作1的名称________。
操作1的名称________。
![]() 写出雌黄浆中通入氧气的化学方程式________。
写出雌黄浆中通入氧气的化学方程式________。
![]() 在粗砷的提纯过程中通常将温度控制在
在粗砷的提纯过程中通常将温度控制在![]() 以上,其目的是什么?________。
以上,其目的是什么?________。
![]() 在粗砷的提纯过程中,通入氯气这步操作为什么必须在干燥的环境中进行?________。
在粗砷的提纯过程中,通入氯气这步操作为什么必须在干燥的环境中进行?________。
![]() 写出
写出![]() 在灼烧条件下生成
在灼烧条件下生成![]() 的化学方程式:________。
的化学方程式:________。
![]() 砒霜的主要成分是
砒霜的主要成分是![]() ,古时候确定人是否砒霜中毒,常用马氏试砷法。其原理是在含砒霜的物质中加入Zn和稀硫酸,得到一种气体A,加热气体A,会得到单质砷。请写出A的化学式________。
,古时候确定人是否砒霜中毒,常用马氏试砷法。其原理是在含砒霜的物质中加入Zn和稀硫酸,得到一种气体A,加热气体A,会得到单质砷。请写出A的化学式________。
![]() 亚砷酸
亚砷酸![]() ,是三元弱酸,第一步和第二步产生
,是三元弱酸,第一步和第二步产生![]() 是通过和水中的氢氧根结合实现的,第三步则直接电离出
是通过和水中的氢氧根结合实现的,第三步则直接电离出![]() 。第一步电离方程式为:
。第一步电离方程式为:![]() ,第二步的电离方程式为________。
,第二步的电离方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式SO2(g)+1/2O2(g)![]() SO3(g) △H=-98.32kJ·mol-1,在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量
SO3(g) △H=-98.32kJ·mol-1,在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量
A. 等于196.64kJ B. 等于196.64kJ·mol-1
C. 小于196.64kJ D. 大于196.64kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列能用勒夏特列原理解释的是
A.Fe(SCN)3溶液中加入固体KSCN后颜色变深
B.工业上由氢气和氮气合成氨是在较高温度下进行的(合成氨是放热反应)
C.SO2催化氧化成SO3的反应,往往需要使用催化剂
D.H2、I2、HI平衡混和气加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA是阿伏加德罗常数的值。下列说法正确的是
A.0.5 molN4(分子为正四面体结构)含共价键数目为2NA
B.1 L 0.5 mol·L1 Na2S溶液中含阴离子数目小于0.5NA
C.锌与浓硫酸反应生成气体11.2 L(标准状况)时转移电子数目为NA
D.14 g己烯和环己烷的混合物含氢原子数目为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中充入1 mol H2和1 mol I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) ![]() 2HI(g)
2HI(g)
(1)保持容器容积不变,向其中充入1 mol H2,反应速率_____(填“增大”、“减小”或“不变”,下同)。
(2)升高温度,反应速率_____。
(3)扩大容器体积,反应速率_____。
(4)保持容器内气体压强不变,向其中充入1 mol H2(g)和1 mol I2(g),反应速率_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com