
【题目】已知t℃时,某些物质的平衡常数K的值如表所示,下列说法错误的是( )
物质 | HCIO | H2CO3 | AgCl | AgI |
平衡常数 | Ka≈10﹣9 | K≈10﹣7 K≈10﹣11 | Ksp≈1.8×10﹣10 | Ksp≈8.51×10﹣17 |
A.向新制氯水中加入少量NaHCO3增强氯水漂白性
B.相同温度和浓度下,NaClO溶液的pH比Na2CO3溶液的pH小
C.t℃时,AgCl(s)+I﹣(aq)![]() AgI(s)+Cl﹣(aq)的平衡常数K=2.1×106
AgI(s)+Cl﹣(aq)的平衡常数K=2.1×106
D.将AgCl和AgI的饱和溶液等体积混合,再加入足量AgNO3溶液,会生成等量的AgCl和AgI沉淀
【答案】D
【解析】
A. 由Ka可知,酸性为H2CO3>HClO>HCO3﹣,据此分析判断;
B. 由对应酸的酸性可知,NaClO溶液比Na2CO3溶液的水解程度小;
C. AgCl(s)+I﹣(aq)![]() AgI(s)+Cl﹣(aq)的平衡常数K=
AgI(s)+Cl﹣(aq)的平衡常数K=![]() ;
;
D. 由Ksp可知,AgCl和AgI的饱和溶液中Cl﹣浓度大于I﹣浓度。
A.由Ka可知,酸性为H2CO3>HClO>HCO3﹣,则向新制氯水中加入少量NaHCO3,HClO浓度增大,增强氯水漂白性,A项正确;
B.由对应酸的酸性可知,NaClO溶液比Na2CO3溶液的水解程度小,则NaClO溶液的pH比Na2CO3溶液的pH小,B项正确;
C.AgCl(s)+I﹣(aq)![]() AgI(s)+Cl﹣(aq)的平衡常数K=
AgI(s)+Cl﹣(aq)的平衡常数K=![]() =
=![]() =2.1×106,C项正确;
=2.1×106,C项正确;
D.由Ksp可知,AgCl和AgI的饱和溶液中Cl﹣浓度大于I﹣浓度,则再加入足量AgNO3溶液,生成AgCl的量大于AgI沉淀的量,D项错误;
答案选D。


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:

回答下列问题:
(1)NaClO2中Cl的化合价为_________;
(2)写出“反应”步骤中生成ClO2的化学方程式________________________;
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、_______________;
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应中,氧化剂与还原剂的物质的量之比为__________________,该反应中氧化产物是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用核磁共振仪对分子式为C3H8O的有机物进行分析,核磁共振氢谱有三个峰,峰面积之比是1:1:6,则该化合物的结构简式为
A.CH3-O-CH2-CH3B.![]()
C.CH3CH2CH2OHD.C3H7OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%~5%、单宁酸(Ka约为104,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。实验室从茶叶中提取咖啡因的流程如下图所示。

索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:

(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________,圆底烧瓶中加入95%乙醇为溶剂,加热前还要加几粒______________。
(2)提取过程不可选用明火直接加热,原因是______________,与常规的萃取相比,采用索氏提取器的优点是______________。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂的优点是______________。“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有______________(填标号)。
A.直形冷凝管 B.球形冷凝管C.接收瓶D.烧杯
(4)浓缩液加生石灰的作用是中和______________和吸收______________。
(5)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】鸟粪石[化学式为Mg(NH4)PO4·6H2O]是一种盛产于秘鲁的优质氮磷肥料;钴(Co)是质子数为27的元素,它的中子数为33的核素可用于癌症的放射性治疗。下列有关说法正确的是
①钴不是主族元素;②![]() Cl2不能长期稳定地存在;③Mg的原子结构示意图为
Cl2不能长期稳定地存在;③Mg的原子结构示意图为 ;④鸟粪石中两种阳离子为Mg2+、NH4+
;④鸟粪石中两种阳离子为Mg2+、NH4+
A.①②③④B.仅①②④C.仅②③④D.仅①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容条件下,可逆反应:![]() ,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是( )(Qc表示浓度熵)
,在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是( )(Qc表示浓度熵)
容器 | 体积 | 起始物质 | 平衡时C的物质的量 | 平衡时B的体积分数 | 平衡常数 |
甲 | 1L |
| 1mol |
|
|
乙 | 1L |
|
|
|
|
丙 | 2L |
|
|
|
|
A.在建立平衡的过程中,甲的Qc逐渐减小,乙和丙的Qc逐渐增大
B.![]()
C.升高甲的温度,可使![]()
D.![]() ,
,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病.治疗高血脂的新药I的合成路线如图所示:

已知:a.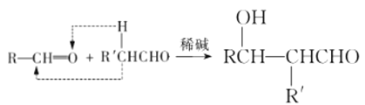 ;
;
b.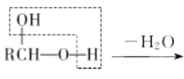 RCHO
RCHO
请回答下列问题:
(1)反应①所需试剂、条件分别是____。
(2)A→B的化学方程式为____。
(3)G的结构简式为____。
(4)化合物W的相对分子质量比化合物C大14。且满足下列条件.W的可能结构有___种。
①遇FeCl3溶液显紫色 ②属于芳香族化合物 ③能发生银镜反应
其中核磁共振氢谱显示有5种不同化学环境的氢.且峰面积比为2:2:2:1:1的结构简式为___
(5)设计用甲苯和乙醛为原料制备![]() 的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A
的合成路线,其他无机试剂任选(合成路线常用的表示方式为:A![]() B……
B……![]() 目标产物)____。
目标产物)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.晋朝人常璇在《华阳国志》里有这样一段话:临邛县“有火井,夜时光映上昭。民欲其火,先以 家火投之。顷许如雷声,火焰出,通耀数十里。以竹筒盛其火藏之,可拽行终日不灭也……”,请回答下列问题。
(1)话中描述的物质是一种最简单的有机物—甲烷,其结构式为________________。
(2)写出“顷许如雷声,火焰出”涉及的化学方程式:__________________。
(3)甲烷不仅可以直接用来燃烧,还是重要的化工原料,它可以与水在高温条件下反应制得水煤气(CO 和H2O),反应的化学方程式为___________,反应得到的水煤气中CO和H2的质量比为____________
Ⅱ.(4)支链上只有一个乙基且相对分子质量最小的烷烃的分子式为____________________。
(5)分子中含有25个共价键且一氯代物只有一种的烷烃的结构简式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
(1)已知:反应i:N2(g)+3H2(g)2NH3(g) △H=-92.4kJ/mol
反应ii:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ/mol
则氨气完全燃烧生成氮气和水蒸气的热化学方程式_____。
(2)已知反应i断开1mol化学键所需的能量见下表:
N≡N | H—H | N—H | |
键能/kJ·mol-1 | 945 | 436 | ? |
则断开1molN-H键所需的能量是_______kJ
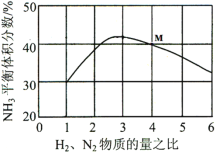
(3)如图表示反应i在500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中M点数据计算N2的平衡体积分数______;该反应的化学平衡常数K的表达式______。
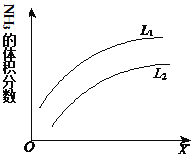
(4)如图是合成氨反应平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是______(填“温度”或“压强”);判断L1、L2的大小关系并说明理由_______。
(5)电化学气敏传感器可用于检测环境中NH3的含量,其工作原理如图所示:
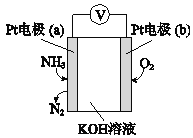
①反应消耗NH3和O2的物质的量之比为____。
②a极的电极反应式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com