
��1��������SO2�������ᵼ����ˮ�к��У��ѧʽ������ ��Σ��ֲ��ͽ���������ŷŵ�SO2β���ñ���Na2SO3��Һ���տɵõ���Ҫ����ԭ��NaHSO3����Ӧ�Ļ�ѧ����ʽΪ ��
��2����֪NaHSO3��ˮ��Һ�����ԣ��Ƚ�����SO32����HSO3����H2SO3�������ӵ�Ũ�ȣ� >����������������>������������������
��3��SO2�ǿ������������ָ��֮һ������SO2��ԭKIO3����I2�ķ�Ӧ�ⶨ������SO2������ÿ����0.01mol I2���μӷ�Ӧ��SO2Ϊ�� ����mol��
��4����֪25��ʱ��Ksp(BaSO4)��1.1��10-10��Ksp (BaCO3)��2.6��10-9������˵������ȷ����
A��25��ʱ����BaSO4����Һ�м������ˮ��Ksp(BaSO4)����
B��25��ʱ����BaSO4����Һ�м���Na2CO3��Һ��BaSO4������ת��ΪBaCO3
C����Na2SO4�м������BaCl2��Һ����Һ��c(SO42��)����Ϊ��
��1��H2SO4��H2SO3��2�֣��� SO2+Na2SO3+H2O��2NaHSO3��3�֣�
��2��c(HSO3��)>c(SO32��)>c(H2SO3) ��3�֣�
��3��0.05mol ��3�֣� ��4��BC ����1.5�֣���3�֣�
���������������1��������SO2�������ᵼ����ˮ�к���H2SO3���������Ἣ�ױ������������ᣬ������ˮ�к��е�������H2SO4��H2SO3�������ŷŵ�SO2β���ñ���Na2SO3��Һ���տɵõ���Ҫ����ԭ��NaHSO3����Ӧ�Ļ�ѧ����ʽΪSO2+Na2SO3+H2O��2NaHSO3��
��2����֪NaHSO3��ˮ��Һ�����ԣ���˵��HSO3���ĵ���̶ȴ���HSO3����ˮ��̶ȣ���SO32����HSO3����H2SO3�������ӵ�Ũ�ȴ�С��ϵ��c(HSO3��)��c(SO32��)��c(H2SO3)��
��3��SO2��ԭKIO3����I2���ڷ�Ӧ��SԪ�صĻ��ϼ۴ӣ�4�������¶ȣ�6�ۣ�ʧȥ2�����ӡ���Ԫ�صĻ��ϼ۴ӣ�5�۽��͵�0�ۣ��õ�5�����ӣ�����ݵ��ӵ�ʧ�غ��֪ÿ����0.01mol I2���μӷ�Ӧ��SO2Ϊ ��
��
��4���ܶȻ�����ֻ���¶��й�ϵ������25��ʱ����BaSO4����Һ�м������ˮ��Ksp(BaSO4)���䣬ѡ��A��ȷ��ֻҪ��Һ��c(Ba2��)��c(CO32��)����Ksp (BaCO3)����������̼�ᱵ����������25��ʱ����BaSO4����Һ�м���Na2CO3��Һ��BaSO4�п���ת��ΪBaCO3��ѡ��B����ȷ�����ᱵ����Һ�д����ܽ�ƽ�⣬������Na2SO4�м������BaCl2��Һ����Һ��c(SO42��)�����ܽ���Ϊ�㣬ѡ��C����ȷ����ѡBC��
���㣺����SO2��Σ����SO2β��������������������Һ������Ũ�ȴ�С�Ƚϡ�������ԭ��Ӧ�ļ��㡣�ܶȻ�������Ӧ�ú��й��ж�
�������������е��Ѷȵ����⣬���������ǿ�����۽̲Ļ���֪ʶ���������С���ע�ض�ѧ������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ����ּ������ѧ��������û���֪ʶ���ʵ�����������������������ѧ���������������淶�Ĵ���������Ҳ����������ѧ���Ļ���������ʶ��ע��֪ʶ���ܽ�ͻ��ۡ�


 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������0. 1 mol/L�����¼�����Һ����H2SO4��Һ��NaHSO4��Һ��CH3COOH��Һ��HCl��Һ��HCN��Һ��NH3��H2O���������¼�����Һ�ĵ����(���Ѿ������ռԭ���ܵİٷ���)���±�(��֪H2SO4�ĵ�һ����������ȫ��)���ش���������:
| ��H2SO4��ҺHSO4- | ��NaHSO4��ҺHSO4- | ��CH3COOH | ��HCl��Һ |
| 10% | 29% | 1.33% | 100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�Ӻ�ˮ����ȡþ������������þ����Ҫ��Դ����������ȡþ�Ĺ������漰�ļ������ʵ��ܶȻ�����������ѧ��֪ʶ�ش����м������⣺
| ���� | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| �ܶȻ� | 2.8��10�C9 | 6.8��10�C6 | 5.5��10�C6 | 1.8��10�C11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����£���ijһԪ��HA��NaOH��Һ�������ϣ�������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH�����±���
| ʵ���� | HA���ʵ���Ũ��(mol��L-1) | NaOH���ʵ���Ũ��(mol��L-1) | �����Һ��pH |
| �� | 0.1 | 0.1 | pH��9 |
| �� | c | 0.2 | pH��7 |
| �� | 0.2 | 0.1 | pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������ǿ�ᣬ��ѧ�ν�������ˮ��Һ�п�����ȫ���롣����ʵ�ǣ�������ˮ�еĵ�һ����������ȫ�ģ��ڶ������벢����ȫ����������Ϊ:H2SO4=H++HSO4-��HSO4- H+ + S042-��
H+ + S042-��
��ش������й�����:
��1��Na2SO4��Һ��_(������ԡ��������ԡ��������ԡ�)����������_
(�����ӷ���ʽ��ʾ)��
��2��H2SO4��Һ��BaC12��Һ��Ӧ�����ӷ���ʽΪ_ ��
��3����0��l0mol��L-1��Na2SO4��Һ�У���������Ũ�ȹ�ϵ��ȷ����_ (��д���)��
| A��c(Na+)=c(SO42-)+c��HSO4һ)+c(H2SO4) |
| B��c(OH-)="c(" HSO4-)+c(H+) |
| C��c( Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| D��c( Na+)=2c(SO42-)+2c(HSO4-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ�������̿�Ϊԭ�ϣ������ս������е�SO2�Ʊ�MnSO4��H2O���������£�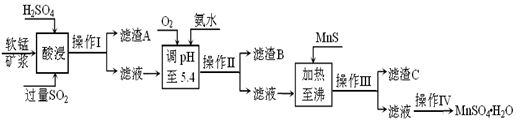
ij���̿����Ҫ�ɷ�ΪMnO2��������Si(16.27%)��Fe(5.86%)��Al(3.42%)��Zn(2.68%)��Cu��0.86%����Ԫ�صĻ����������̷�����Ӧ��MemOn+H+��Me��2n/m��++H2O��Me��ʾFe�� Al�� Zn�� Cu�ȡ�25��ʱ����������������������������ʽ��ȫ����ʱ��Һ��pH���±���
| ������ | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ��-0.42 | ��2.5 | ��7 | ��7 |
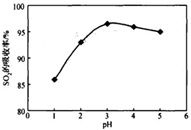
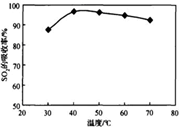
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
[14��]��֪��I2��2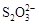

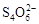 ��2I�D��������ʵ��ܶȻ��������±���
��2I�D��������ʵ��ܶȻ��������±���
| ���� | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2��10��20 | 2.6��10��39 | 1.7��10��7 | 1.3��10��12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��ʽ���������и�С�⣺
��1��ij�¶�ʱ�����0.01 mol/L��NaOH��ҺpHΪ11������¶���ˮ�����ӻ�����Kw
��2���ڴ��¶��£���pH��a��NaOH��ҺVa L��pH��b������Vb L��ϡ�
�������û����ҺΪ���ԣ���a��12��b��2����Va��Vb��
�������û����Һ��pH��10����a��12��b��2����Va��Vb��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ijͬѧ��0.10 mol/L��HCl��Һ�ⶨδ֪Ũ�ȵ�NaOH��Һ����ʵ��������£�
| A������ʽ�ζ�����ȡ20.00 mL HCl��Һע����ƿ��ͬʱ�μ�2-3�η�̪��Һ�� |
| B����0.10 mol/L��HC!��Һ��ϴ��ʽ�ζ��ܣ� |
| C���ѵζ���������ˮϴ���� |
| D��ȡ�¼�ʽ�ζ��ܣ��ô���NaOH��Һ��ϴ������NaOH��Һע���ʽ�ζ���������̶ȡ�0������20 cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ�棻 |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com