
【题目】按要求填空
(1)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知:N≡N键的键能是948.9kJmol﹣1 , H﹣H键的键能是436.0kJmol﹣1;由N2和H2合成1mol NH3时可放出46.2kJ的热量.N﹣H键的键能是
(2)由氢气和氧气反应生成1mol水蒸气,放热241.8KJ.写出该反应的热化学方程式:① .
已知常温下NO与O2反应生成1molNO2的焓变为﹣57.07KJ,1molNO2与H2O反应生成HNO3溶液和NO的焓变为﹣46KJ,写出NO与O2及水生成HNO3溶液的热化学方程式② .
(3)某温度下纯水中的c(H+)=2×10﹣7mol/L,则此时c(OH﹣)=mol/L,该纯水的pH(填“>7”、“<7”、“=7”).若温度不变,滴入稀硫酸使c(H+)=5×10﹣6mol/L,则c(OH﹣)=mol/.
(4)纳米MgO可用于尿素与氯化镁合成.某小组研究该反应在温度为378~398K时的反应时间、反应物配比等因素对其产率的影响.请完成以下实验设计表:
编号 | 温度/K | 反应时间/h | 反应物物质的量配比 | 实验目的 |
① | 378 | 3 | 3:1 | 实验②和④探究 |
② | 378 | 4 | 4:1 | |
③ | 378 | 3 | ||
④ | 398 | 4 | 4:1 |
【答案】
(1)391.6kJ?mol﹣1
(2)H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJ/mol;4NO(g)+3O2(g)+2H2O(g)=4HNO3(aq)△H=﹣618.42KJ/mol
O2(g)═H2O(g)△H=﹣241.8kJ/mol;4NO(g)+3O2(g)+2H2O(g)=4HNO3(aq)△H=﹣618.42KJ/mol
(3)2×10﹣7;<7;8×10﹣9
(4)温度对产率的影响;4:1;③
【解析】解:(1)据题意,0.5mol氮气和1.5mol氢气反应生成1mol氨气时放出46.2KJ的热量,又△H=反应物的键能﹣生成物的键能,1mol氨气中有3molN﹣H键,设其键能为x,则有0.5×948.9+1.5×436.0﹣3x=﹣46.2,
可解得x=391.6,所以N﹣H键的键能为391.6kJ/mol,
所以答案是:391.6 kJmol﹣1;
(2.)氢气和氧气反应生成1mol水蒸气放热241.8kJ,该反应的热化学方程式为:H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJ/mol,常温下NO与O2反应生成1molNO2的焓变为﹣57.07KJ,热化学方程式为:NO(g)+
O2(g)═H2O(g)△H=﹣241.8kJ/mol,常温下NO与O2反应生成1molNO2的焓变为﹣57.07KJ,热化学方程式为:NO(g)+ ![]() O2(g)=NO2(g)△H=﹣57.07KJ/mol ①,1molNO2与H2O反应生成HNO3溶液和NO的焓变为﹣46KJ,NO2(g)+
O2(g)=NO2(g)△H=﹣57.07KJ/mol ①,1molNO2与H2O反应生成HNO3溶液和NO的焓变为﹣46KJ,NO2(g)+ ![]() H2O(l)=
H2O(l)= ![]() HNO3(aq)+
HNO3(aq)+ ![]() NO(g),△H=﹣46KJ/mol ②,依据盖斯定律(①+②)×6得到热化学方程式:4NO(g)+3O2(g)+2H2O(g)=4HNO3(aq)△H=﹣618.42KJ/mol,
NO(g),△H=﹣46KJ/mol ②,依据盖斯定律(①+②)×6得到热化学方程式:4NO(g)+3O2(g)+2H2O(g)=4HNO3(aq)△H=﹣618.42KJ/mol,
所以答案是:H2(g)+ ![]() O2(g)═H2O(g)△H=﹣241.8kJ/mol,4NO(g)+3O2(g)+2H2O(g)=4HNO3(aq)△H=﹣618.42KJ/mol;
O2(g)═H2O(g)△H=﹣241.8kJ/mol,4NO(g)+3O2(g)+2H2O(g)=4HNO3(aq)△H=﹣618.42KJ/mol;
(3.)纯水中 C(OH﹣)=C(H+)=2×10﹣7 mol/L Kw=C(H+)C(OH﹣)=2×10﹣7×2×10﹣7=4×10﹣14 , 水呈中性,PH<7,若温度不变,滴入稀硫酸使c(H+)=5×10﹣6mol/L,C(OH﹣)= ![]() =
= ![]() =8×10﹣9 mol/L,
=8×10﹣9 mol/L,
所以答案是:2×10﹣7 , <7,8×10﹣9;
(4.)实验根据控制变量法进行对比试验,研究温度、反应时间、反应物配比对氧化镁产率的影响.
实验①和③,温度相同,反应时间相同,应研究反应物配比对氧化镁产率的影响,③中反应物配比应为4:1;
实验②和④,反应时间相同,反应物配比相同,温度不同,应是探究温度对产率的影响;
③中反应物配比应为4:1,实验②和③,温度相同、反应物配比相同,反应时间不同,探究反应时间对产率的影响.
所以答案是:4:1;温度对产率的影响;③;
【考点精析】利用反应热和焓变对题目进行判断即可得到答案,需要熟知在化学反应中放出或吸收的热量,通常叫反应热.


科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)在25℃下,向浓度均为0.1molL﹣1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成沉淀(填化学式),生成该沉淀的离子方程式为 . 已知25℃时Ksp[Mg(OH)2]=1.8×10﹣11 , Ksp[Cu(OH)2]=2.2×10﹣20 .
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时, ![]() = . [Ksp(AgBr)=5.4×10﹣13 , Ksp(AgCl)=2.0×10﹣10].
= . [Ksp(AgBr)=5.4×10﹣13 , Ksp(AgCl)=2.0×10﹣10].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是( ) 
A.放电时左侧电解质储罐中的离子总浓度增大
B.充电时电极a连接电源的负极
C.放电时负极的电极反应式为Zn﹣2e﹣═Zn2+
D.阳离子交换膜可阻止Br2与Zn直接发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( ) 
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO47H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%). 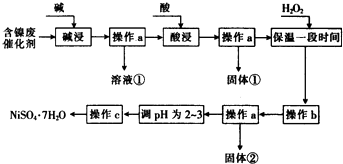
部分阳离子以氢氧化物形式沉淀时的pH如下:
沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
Al(OH)3 | 3.8 | 5.2 |
Fe(OH)3 | 2.7 | 3.2 |
Fe(OH)2 | 7.6 | 9.7 |
Ni(OH)2 | 7.1 | 9.2 |
(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是(填化学式).
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是
(5)产品晶体中有时会混有少量绿矾(FeSO47H2O),其原因可能是(写出一点即可).
(6)NiS047H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向2.0L恒容密闭容器中充入1.0mol PCl5 , 在温度为T时发生如下反应PCl5(g)PCl3(g)+Cl2(g)△H=+124kJmol﹣1 . 反应过程中测定的部分数据见下表:
时间t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
回答下列问题:
(1)反应在前50s的平均速率v(PCl5)= , 该反应的△S0(填“<”、“>”或“=”).
(2)温度为T时,该反应的化学平衡常数= .
(3)上述反应到达平衡状态时,PCl3的体积分数为 .
要提高平衡时PCl3的体积分数,可采取的措施有 .
A.温度不变,压缩容器体积增大压强 B.使用高效催化剂
C.温度和体积不变,减小PCl5的起始量 D.体积不变,提高反应温度
(4)在温度为T时,若起始时向容器中充入0.5mol PCl5和a mol Cl2平衡时PCl5的转化率仍为20%,则a= .
(5)在热水中,五氯化磷完全水解,生成磷酸(H3PO4),该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生课外活动小组,模拟呼吸面具中的反应原理,设计用如图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0~50 mL),供量气用,乙管可上下移动调节液面高低。实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。
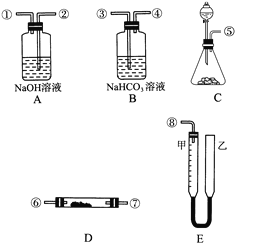
试回答:
(1)图中各装置接口连接顺序是________(填各接口的编号,其中连接胶管及夹持装置均省略)。
(2)装置C中放入的反应物是________和________。
(3)装置A的作用是______________,装置B的作用是____________。
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数及求其差值的过程中,应注意________和________。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时立刻读数
c.读数前应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组对过量炭粉与氧化铁反应的气体产物成分进行研究.
(1)提出假设
①该反应的气体产物是CO2 .
②该反应的气体产物是CO.
③该反应的气体产物是 .
(2)设计方案
如图所示,将一定量的氧化铁在隔绝空气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比.
查阅资料
氮气不与碳、氧化铁发生反应.实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气.请写出该反应的离子方程式: .
(3)实验步骤
①按图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气.冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g.
步骤②、④中都分别通入N2 , 其作用分别为 .
(4)数据处理
试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式: .
(5)实验优化 学习小组有同学认为应对实验装置进一步完善.
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是 .
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com