
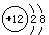 ���ʴ�Ϊ��
���ʴ�Ϊ��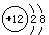 ��
��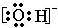 ���ʴ�Ϊ��
���ʴ�Ϊ��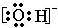 ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
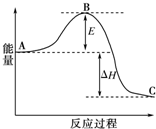 Ϊ�˺������û�ѧ�ܣ�ȷ����ȫ���������������Ҫ��ֿ��ǻ�ѧ��Ӧ�ķ�Ӧ�ȣ�����ȡ��Ӧ��ʩ����ѧ��Ӧ�ķ�Ӧ��ͨ����ʵ����вⶨ��Ҳ�ɽ����������㣮
Ϊ�˺������û�ѧ�ܣ�ȷ����ȫ���������������Ҫ��ֿ��ǻ�ѧ��Ӧ�ķ�Ӧ�ȣ�����ȡ��Ӧ��ʩ����ѧ��Ӧ�ķ�Ӧ��ͨ����ʵ����вⶨ��Ҳ�ɽ����������㣮| 1 |
| 2 |
| 1 |
| 2 |
| ��ѧ�� | H-H | N-H | N��N |
| ����/kJ?mol-1 | 436 | 391 | 945 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������þ��Һ������������Һ��Ӧ��SO42-+Ba2+=BaSO4��SO42- |
| B��H2SO4��Һ��Ba��OH��2��Һ��Ӧ��Ba2++OH-+H++=BaSO4��+H2O |
| C��ͭƬ������������Һ�У�Cu+2Ag+�TCu2++2Ag |
| D������ʯ��ˮ�м������� Ca��OH��2+2H+=Ca2++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ħ��������98g |
| B����״���£�22.4L��O2������32g |
| C��2gH2����ԭ����ĿΪ1mol |
| D����ԭ�ӵ�Ħ�����������������ԭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��C2O3��CO2�����ڷǽ��������� |
| B��C2O3��CO����ȫȼ�ղ��ﶼ��CO2 |
| C��C2O3��CO���Ǽ��������� |
| D��C2O3��CO�����л�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Aռ�������B�� |
| B��A�����ʵ�����B�� |
| C��A���ܶȱ�BС |
| D��A��Ħ��������B�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
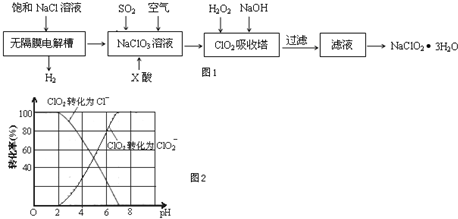
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������������Ӧ���е������ɣ����Զ����û���Ӧ |
| B����������ǿ����˳��ΪKClO3��KBrO3��Cl2��Br2 |
| C����Ӧ���л�ԭ���������������ʵ���֮��Ϊ5��1 |
| D������lmol��ԭ����Ӧ���������õ����ӵ����ʵ���Ϊ2mol |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com