
| A、硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓SO42- |
| B、H2SO4溶液与Ba(OH)2溶液反应:Ba2++OH-+H++=BaSO4↓+H2O |
| C、铜片插入硝酸银溶液中:Cu+2Ag+═Cu2++2Ag |
| D、澄清石灰水中加入盐酸 Ca(OH)2+2H+=Ca2++2H2O |


科目:高中化学 来源: 题型:
| A、中性溶液的pD=7.0 |
| B、含0.01 mol的NaOH的D2O溶液1 L,其pD=12.0 |
| C、溶有0.01 mol DCl的水溶液1 L,其pD=2.0 |
| D、在100 mL 0.2 mol?L-1的DCl重水溶液中,加入100 mL 0.2 mol?L-1的NaOD的重水溶液,其pD=7.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化剂仅是CuSO4,FeS2仅是还原剂 | ||
| B、当生成7molCu2S时,共转移电子14mol | ||
| C、产物中SO42-全部是氧化产物 | ||
D、该反应中1molCuSO4能氧化
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16gO2中含有NA个氧气分子 |
| B、1mol/LCaCl2溶液中含有2molCl- |
| C、1mol锌与足量盐酸反应产生H21mol |
| D、常温常压下,22.4LCO2含有NA个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气跟水反应:Cl2+H2O=2H++Cl-+ClO- |
| B、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
| C、碳酸钠溶液中加入少量稀盐酸:CO32-+H+=HCO3- |
| D、铜与稀盐酸反应:Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、次氯酸钙的化学式 CaClO |
| B、次氯酸的电离HClO=H++Cl-+O2- |
| C、硫酸的电离H2SO4=H2++SO42- |
D、镁的原子结构示意图: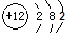 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com