
����Ŀ��Ϊ�о�ͭ��Ũ����ķ�Ӧ��ij��ѧ��ȤС���������ʵ�顣
ʵ��I����Ӧ����Ķ���̽����������ͼװ�����̶�װ������������ʵ����

��1��Fװ�õ��ձ��з�����Ӧ�����ӷ���ʽ�� ��
��2��ʵ������У���֤��Ũ��������Ԫ�ص�������ǿ����Ԫ�ص������� ��
��3��ʵ�����ʱ����ȥ���оƾ���֮ǰ������ɵ�ʵ������� ��
��4��ʵ�������֤��Aװ���Թ��з�Ӧ���ò����Ƿ���ͭ���ӵIJ��������� ��
ʵ��II����Ӧ����Ķ���̽��
��5����ͭ��Ũ���ᷴӦ�Ĺ����У������к�ɫ���ʳ��֣��Һ�ɫ����ΪCu2S������Cu2S�ķ�ӦΪaCu+bH2SO4![]() cCu2S+dCuSO4+eH2O����a��b= ��
cCu2S+dCuSO4+eH2O����a��b= ��
��6��Ϊ��һ��̽���ú�ɫ���ʵijɷ֣����������������������ϡ�
����1��
����/mol��L��1 | ��ɫ���ʳ��ֵ��¶�/�� | ��ɫ������ʧ���¶�/�� |
14 | Cu Ƭ�������������� | |
15 | Լ150 | Լ236 |
16 | Լ140 | Լ250 |
18 | Լ120 | ����ʧ |
����2��X-���߾������������ͭ��Ũ���ᷴӦ���ɵĺ�ɫ����ΪCu2S��CuS��Cu7S4�е�һ�ֻ��֡������������Ͽɵó������½�������ȷ�� ��
A��ͭ��Ũ���ᷴӦʱ���漰�ķ�Ӧ���ܲ�ֹһ��
B������Ũ��ѡ���ʵ����ɱ����������г��ֺ�ɫ����
C���÷�Ӧ����������֮һ������Ũ�� �� 15 mol/L
D������Ũ��Խ��ɫ����Խ����֡�Խ����ʧ
���𰸡���1��SO2 + 2 OH�� = SO32�� + H2O
��2��D������������E��Ʒ����Һ��ɫ
��3�����ͭ˿���ر�K1��K2
��4������A�Թ�����Һ��ȴ�����º���������ˮ�����ձ��У�������������ȴҺ��������Һ����ɫ����֤��
��5��5��4��6��ACD
��������
�����������1����ͼ��֪���ŵ�����Fװ���й���NaOH��Һ��Ŀ�������ն����SO2�������������ƺ�ˮ����SO2 + 2 OH�� = SO32�� + H2O����2�����D������������E��Ʒ����Һ��ɫ��˵��Ũ������ͭ�ڼ����·�Ӧ���ɵ����岻������������SO2����Ũ�����н���Ԫ�ز���+1�۵������+6�۵���3�����ͭ˿��ֹͣ��Ӧ����Դͷ�Ϸ�ֹ��SO2�����ɣ���װ������������������Ϊ�˷�ֹC��Eװ�õ�Һ�嵹���������Ӳ�ʲ����ܣ�����ر�K1��K2��Ȼ���ٳ�ȥ���оƾ��ƣ���4��װ��A������Һ��Ϊ����ͭ��Ũ����Ļ���Ϊ�˼��������Ƿ�Cu2+���ҷ�ֹҺ�屩�У�Ӧ����A�Թ�����Һ��ȴ�����º���������ˮ�����ձ��У�������������ȴҺ��������Һ����ɫ����֤������5������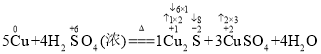 ����÷�Ӧ�����ĵ�Cu��H2SO4��ϵ��֮�Ȼ����ʵ���֮��Ϊ5��4����6��A��ͭ��Ũ���ᷴӦʱ���漰�ķ�Ӧ��Cu+2H2SO4(Ũ)
����÷�Ӧ�����ĵ�Cu��H2SO4��ϵ��֮�Ȼ����ʵ���֮��Ϊ5��4����6��A��ͭ��Ũ���ᷴӦʱ���漰�ķ�Ӧ��Cu+2H2SO4(Ũ)![]() CuSO4+SO2��+2H2O��5Cu +4H2SO4
CuSO4+SO2��+2H2O��5Cu +4H2SO4 ![]() 1Cu2S + 3 CuSO4 + 4H2O�ȣ�A��ȷ��B��Ũ��Ϊ14mol��L��1ʱ�������ֺ�ɫ���ʣ�B��ȷ��C���ɱ�����Ϣ��֪��Ũ��Ϊ15mol��L��1��16mol��L��1��18mol��L��1��������������������÷�Ӧ����������֮һ������Ũ�� �� 15 mol/L�����ֹ��ɾͺܲ����ܣ���Ϊ����ȱ��17mol��L��1�������C����D���ɱ�����Ϣ��֪��Ũ����ԽŨ�����ֺ�ɫ���ʵ��¶�ԽС������ʧ���¶�Խ�ߣ�Ũ�ȼ�С�����ֺ�ɫ���ʵ��¶�Խ�ߣ�����ʧ���¶�Խ�ͣ�D��ȷ����ѡABD��
1Cu2S + 3 CuSO4 + 4H2O�ȣ�A��ȷ��B��Ũ��Ϊ14mol��L��1ʱ�������ֺ�ɫ���ʣ�B��ȷ��C���ɱ�����Ϣ��֪��Ũ��Ϊ15mol��L��1��16mol��L��1��18mol��L��1��������������������÷�Ӧ����������֮һ������Ũ�� �� 15 mol/L�����ֹ��ɾͺܲ����ܣ���Ϊ����ȱ��17mol��L��1�������C����D���ɱ�����Ϣ��֪��Ũ����ԽŨ�����ֺ�ɫ���ʵ��¶�ԽС������ʧ���¶�Խ�ߣ�Ũ�ȼ�С�����ֺ�ɫ���ʵ��¶�Խ�ߣ�����ʧ���¶�Խ�ͣ�D��ȷ����ѡABD��


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҺ̬����������Է�������Ϊ106������ӽṹ�к���һ���������������ֽṹ��ͬ���칹�干�У� ��
A. 2�� B. 5�� C. 4�� D. 3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ������������Ӱ��ܴ����п϶����Լӿ컯ѧ��Ӧ���ʵĴ�ʩ�ǣ� ��
A��ʹ�ô��� B���ı�Ũ�� C�������¶� D�������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����

A����ͼ�ɱ�ʾˮ�ֽ�����е������仯
B����2C(s)+O2(g)=2CO(g) ��=��221.0kJ/mol����̼��ȼ����Ϊ110.5kJ/mol
C����Ҫ���ȵķ�Ӧһ�������ȷ�Ӧ���������ܷ����ķ�Ӧһ���Ƿ��ȷ�Ӧ
D����֪I����ӦH2(g)+Cl2(g)=2HCl(g) ��=��akJ/mol
II�� ![]()
��a��b��c�������㣬��Ͽ�1mol H��Cl�����������Ϊ����a��b��c��kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CoCl2��6H2O��һ������Ӫ��ǿ��������ҵ������ˮ�ܿ�[��Ҫ�ɷ�ΪCo2O3��Co(OH)3����������Fe2O3��Al2O3��MnO��]��ȡCoCl2��6H2O�Ĺ�������������

��֪���� ����Һ�к��е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Al3+����
�� CoCl2��6H2O�۵�Ϊ86�棬������110��120��ʱ��ʧȥ�ᾧˮ������ˮ�Ȼ��ܡ�
�� ����������������������ʽ����ʱ��Һ��pH���±�������������Ũ��Ϊ��0.01 mol/L��
������ | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
��1��ˮ�ܿ����Ԥ����ʱ����Na2SO3������Ҫ������(�û�ѧ����ʽ˵��) ��
��2��д��NaClO3�ڽ���Һ�з�����Ҫ��Ӧ�����ӷ���ʽ ������������Һ���м��˹�����NaClO3�����ܻ������ж����壬д�����ɸ��ж���������ӷ���ʽ ��
��3����ϵ�в������а���3������ʵ����������� �� ���ˡ�
��4������Һ��Na2CO3��pH��5.2 ʱ��������Һ�н��������� ����ȡҺ�к��е���Ҫ������������ ��
��5��ΪѰ�Һ��ʵ���ȡ��������ij����ȡ���Բ������ӵ���ȡ������ҺpH �Ĺ�ϵ����ͼ��ʾ����д���й���ȡ���ɣ���˵���������Ƿ����ø���ȡ��������ȡ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijͬѧ��500 mL����ƿ����0.10 mol��L��1Na2CO3��Һ�IJ��裺
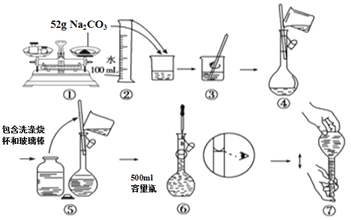
��ͬѧ�Ĵ�����
A. �٢ݢ� B. �ڢܢ� C. �٢� D. �ݢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2 L���ܱ�������ͨ���������巢����ѧ��Ӧ����Ӧ�и����ʵ����ʵ����仯����ͼ��ʾ���Ը÷�Ӧ���ƶϺ������ǣ� ��

A. �÷�Ӧ�Ļ�ѧ����ʽΪ3B��4D![]() 6A��2C
6A��2C
B. ��Ӧ���е�1 sʱ��v��A����v��D��
C. ��Ӧ���е�6 sʱ��B��ƽ����Ӧ����Ϊ0.05 mol/��L��s��
D. ��Ӧ���е�6 sʱ�������ʵķ�Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧʽֻ�ܱ�ʾһֱ���ʵ��ǣ� ��
A��C3H8 B��C4H10 C��C5H12 D��C2H4Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ܱ������У��ֱ����������ȵ�N2��O2�������壬���ǵ��¶Ⱥ��ܶȾ���ͬ������˵������ȷ������ ��
A����������N2<O2
B������Ħ�������N2<O2
C�������ѹǿ��N2<O2
D�������N2<O2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com