
【题目】下列叙述正确的是( )
A. 铁与稀H2SO4反应时,加入少量CuSO4溶液,可使反应速率加快
B. 构成原电池的正极和负极必须是两种不同的金属
C. 在铁上镀铜时,金属铜作阴极
D. 用惰性电极电解CuSO4溶液,溶液的pH不变
科目:高中化学 来源: 题型:
【题目】一个由n条多肽链组成的蛋白质分子共有m个氨基酸,该蛋白质分子完全水解共需多少个水分子( )
A. n个 B. m个 C. (m+n)个 D. (m-n)个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置进行化学反应X+2Y===2Z能量变化情况的研究。当往U形管中滴加试剂Y时,看到试管中甲处下降,乙处上升。下列关于该反应的叙述正确的是( )
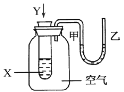
①该反应为放热反应
②生成物的总能量比反应物的总能量高
③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来
A.①②③ B.①③ C.①② D.③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。下列说法不正确的是
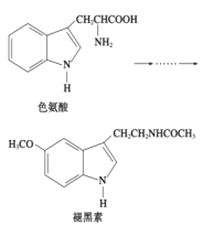
A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点
B.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出
C.在一定条件下,色氨酸可发生缩聚反应
D.褪黑素与色氨酸结构相似,也具有两性化合物的特性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不能说明醋酸是弱电解质的是
A. 醋酸溶液导电性差 B. 醋酸溶液中存在醋酸分子
C. 醋酸钠溶液呈碱性 D. 0.1 mol/L醋酸溶液的pH=2.9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2。符合上述转化关系的A、C可能是

①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2
A.只有②③④⑥ B.除①外 C.除⑤外 D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A.足量铁在氯气中反应,1 mol铁失去的电子数为3 NA
B.6.4 g Cu与足量硫充分反应后,转移电子数为0.2 NA
C.密闭容器中2 mol NO与1 mol O2充分反应后,产物的分子数为NA
D.常温常压下,0.1 mol NH3与0.1 mol HCl充分反应后所得产物含0.1 NA个分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】数十年来,化学工作者对碳的氧化物做了广泛深入的研究并取得了一些重要成果。如利用CO2和CH4重整可制合成气(主要成分为CO、H2),已知重整过程中部分反应的热化学方程式为:
I、CH4(g)=C(s)+2H2(g) △H=+75.0kJ·mol-1
II、CO2(g)+H2(g)=CO(g)+H2O(g) △H=+41.0kJ·mol-1
III、CO(g)+H2(g)=C(s)+H2O(g) △H=-131.0kJ·mol-1
(1)反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的△H = kJ·mol-1。
(2)固定n(CO2)=n(CH4),改变反应温度,CO2和CH4的平衡转化率见图甲。


①同温度下CO2的平衡转化率 (填“大于”或“小于”)CH4的平衡转化率,其原因是 。
②高温下进行该反应时常会因反应I生成“积碳”(碳单质),造成催化剂中毒,高温下反应I能自发进行的原因是 。
(3)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如图乙所示,该反应的化学方程式为 。
(4)CO常用于工业冶炼金属,右图是在不同温度下CO还原四种金属氧化物达平衡后气体中lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。下列说法正确的是 。
A.工业上可以通过增高反应装置来延长矿石和CO接触的时间,减少尾气中CO的含量
B.CO不适宜用于工业冶炼金属铬(Cr)
C.工业冶炼金属铜(Cu)时较低的温度有利于提高CO的利用率
D.CO还原PbO2的反应ΔH>0
(5)在载人航天器中应用电化学原理,以Pt为阳极,Pb(CO2的载体)为阴极,KHCO3溶液为电解质溶液,还原消除航天器内CO2同时产生O2和新的能源CO,总反应的化学方程式为:2CO2![]() 2CO+O2,则其阳极的电极反应式为 。
2CO+O2,则其阳极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com