
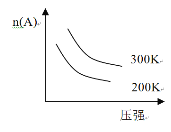
【题目】如下图所示,不能适用于下列可逆反应的是
A.3A(g)+B(g)![]() 2C(g);ΔH<0
2C(g);ΔH<0
B.A(g)+3B(s)+2C(g)![]() 3D(g);ΔH<0
3D(g);ΔH<0
C.C(s)+D(g)![]() A(g)+B(g)ΔH>0
A(g)+B(g)ΔH>0
D.2C(g)![]() 2A(g)+B(g)ΔH>0
2A(g)+B(g)ΔH>0
【答案】B
【解析】
试题分析:由图可知,温度越高A的物质的量越大,说明升高温度平衡向生成A的方向移动,而压强越大A的物质的量越小,说明增大压强平衡向消耗A的方向移动。A.正反应为气体体积减小的放热反应,升高温度平衡逆向移动,A的物质的量增大,增大压强平衡正向移动,A的物质的量减小,与图像相符合,A正确;
B.正反应为气体体积不变的放热反应,增大压强平衡不移动,A的物质的量不变,与图像不符合,B错误;
C.正反应为气体体积增大的吸热反应,升高温度平衡正向移动,A的物质的量增大,增大压强平衡逆向移动,A的物质的量减小,与图像相符合,C正确;
D.正反应为气体体积增大的吸热反应,升高温度平衡正向移动,A的物质的量增大,增大压强平衡逆向移动,A的物质的量减小,与图像相符合,D正确,答案选B。


科目:高中化学 来源: 题型:
【题目】工业上制备纯硅的热化学方程式如下:SiCl4(g)+2H2(g) ![]() Si(s)+4HCl(g)ΔH=+Q kJ·mol-1 (Q>0);某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是 ( )
Si(s)+4HCl(g)ΔH=+Q kJ·mol-1 (Q>0);某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是 ( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则在平衡时,吸收热量为Q kJ
C.将反应的温度由T1升高至T2,则对应温度下的平衡常数K1>K2
D.当反应吸收热量为0.25Q kJ时,生成的HCl恰好与1 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.稀硫酸和铜粉反应可制备硫酸铜
B.碘化钾与浓硫酸反应可制备碘化氢
C.过氧化钠与二氧化碳反应可制备氧气
D.铝箔在氯气中燃烧可制备无水三氯化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当光束通过下列每组分散系时,不能通过观察丁达尔效应进行区分的是
A.H2SiO3胶体和NACl溶液 B.FeCl3溶液和Fe(OH)3胶体
C.豆浆和蔗糖溶液 D.CuSO4溶液和NA2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向浓度相等、体积均为50ml的A、B两份氢氧化钠溶液中分别通入一定量的二氧化碳后,再稀释至100ml。
(1)向氢氧化钠溶液中通入一定量的二氧化碳后,溶液中溶质的可能组成有:①______;②_______;
③_______;④_______。
(2)向稀释后的溶液中逐滴加入0.1mol/L的盐酸溶液,产生二氧化碳的体积(标准状况)与所加盐酸溶液的体积关系如图所示。
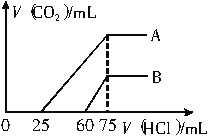
①A曲线表明,向原溶液中通入二氧化碳后,所得溶质与HCl反应产生二氧化碳的最大体积是_______mL(标准状况)。
②B曲线表明,向原溶液中通入二氧化碳后,所得溶液中溶质的化学式为___________。
③原氢氧化钠溶液中NaOH的物质的量浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池总反应的离子方程式是:Zn+Cu2+═Zn2++Cu,依据此反应设计原电池的正确组合是( )
选项 | 正极 | 负极 | 电解质溶液 |
A | Cu | Zn | 稀盐酸 |
B | C | Zn | 硫酸铜溶液 |
C | Cu | Zn | 氯化铜溶液 |
D | Cu | Zn | 硝酸铜溶液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com