
【题目】我国化学侯德榜改革国外的纯碱生产工艺,生产流程如图所示,下列说法不正确的是

A. 在沉淀池中应先通入氨气,在通入二氧化碳气体
B. 在过滤后的母液中加入氯化钠粉末、通入氨气,搅拌,经冷却结晶后可得氯化铵晶体
C. 循环1中X是二氧化碳
D. 该反应原理: NH3+CO2+H2O=HCO3-+NH4+
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】硝酸银是一种无色晶体,常用于照相、制镜、印刷、医药等。其水溶液和固体常被保存在棕色试剂瓶中。硝酸银不稳定,受热分解生成固体、NO2 和 O2 。为了验证 AgNO3 受热分解的产物,某同学设计了以下实验,实验所用的装置如图(图中加热、夹持仪器等均略去):
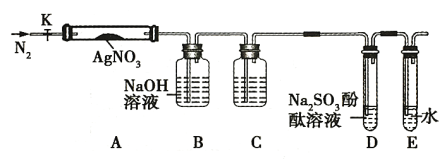
实验步骤:
a.仪器连接后,放入AgNO3固体之前,关闭K,微热硬质玻璃管A;
b.称取 AgNO3 固体1.7g 置于A中,先通一段时间N2,再关闭K,用酒精灯加热硬质玻璃管A;
c.待样品完全分解,装置A冷却至室温,称量,测得剩余固体的质量为1.08 g。
请回答下列问题:
(1)使用酒精灯对AgNO3固体加热的操作方法是_________________。
(2)步骤a的操作目的是__________________。
(3)步骤b中先通一段时间的N2的目的是_____________________。
(4)装置C瓶中盛装的药品名称为_____________(合理即可),装置D中可观察到的实验现象为__________________。
(5)根据实验现象和称量结果,请写出该装置中AgNO3固体受热分解的化学方程式__________________。
(6)从实验安全角度考虑该装置存在缺陷,应如何改进?__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究某铁碳合金与浓硫酸在加热条件下的反应的部分产物,并测定铁碳合金中铁元素的质量分数,某化学活动小组设计了如图所示的实验装置,并完成以下实验探究。
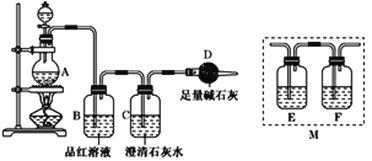
(1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;②______________。
(2)点燃酒精灯,反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是______________。
(3)装置B的作用是___________。
(4)甲同学观察到装置C中有白色沉淀生成,他得出了使澄清石灰水变浑浊的气体是二氧化碳。装置A中能产生二氧化碳的化学方程式为______。
(5)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B和C之间添加装置M。装置E、F中盛放的试剂分别是____________、____________。重新实验后观察到装置F中的现象是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是:( )
①金属钠、氢气都能在氯气中燃烧,生成白色的烟雾;②铜丝在氯气中燃烧,生成蓝绿色的氯化铜;③液氯就是氯气的水溶液,它能使干燥的有色布条褪色;④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
A.①B.①②C.①③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:4NH3+5O2═4NO+6H2O
(1)用双线桥法表示电子转移情况_____________
(2) 若有80gO2参加反应,则生成的氧化产物在标况下的体积是__________升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质。
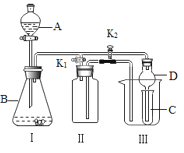
(1)利用I、Ⅱ装置可制取收集气体(K2关闭,K1打开)。
①下列各组物质中能直接利用这套装置进行实验的是_____ (填正确选项的标号)。
A.锌和稀硫酸 B.双氧水和二氧化锰
C.浓氨水和氧化钙 D.浓盐酸和二氧化锰
②在不改变I、II装置及位置的前提下,若要制取收集NO气体,可采取的改进方法是装置II内充满水;若要制取收集NO2气体,可采取的改进方法是:_______________________。
(2)利用I、III装置可验证物质的性质(K2打开,K1关闭)。
①若要证明氧化性:KMnO4>Cl2>Br2,则A中加浓盐酸,B中加KMnO4,C中发生的离子反应方程式___________________________________。
②若要证明乙炔为不饱和烃,则I中发生的化学反应方程式为:_________________。C中的现象为(假设乙炔纯净)________________________________。
(3)装置Ⅲ中使用球形干燥管D的作用为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列数量的各物质所含原子数按由大到小的顺序排列是________。
①0.5 mol氨气
②标准状况下22.4 L氦气
③4 ℃时9 mL水
④0.2 mol磷酸钠(Na3PO4)
(2)现有m g某气体,它是三原子分子,其摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,请用以上符号及相应数字填写下列空格。
①该气体的物质的量为________mol。
②该气体所含原子总数为________个。
③该气体在标准状况下的体积为________L。
④该气体完全溶于水形成V L溶液(不考虑反应),所得溶液的物质的量浓度为________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与水一样,甲醇也能微弱电离:2CH3OH(l)![]() CH3OH2++CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
CH3OH2++CH3O-,25℃时,K=2.0×10-17。若往一定量的甲醇中加入金属钠,则有关叙述正确的是( )
A. 金属钠与甲醇反应比金属钠与水反应更剧烈
B. 结合H+的能力CH3O-<OH-
C. 所得到溶液中K=c(CH3O-)×c(CH3OH2+)
D. 所得到溶液中c(Na+)=c(CH3OH2+) + c(CH3O-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com