
【题目】若NA表示阿伏伽德罗常数的值,则下列说法正确的是
A. 标准状况下,2.24L N2和O2的混合气体中分子数为0.1NA
B. 32g S8(分子结构: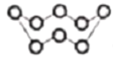 )中的共价键数目为8NA
)中的共价键数目为8NA
C. 3mol SO2和1mol O2于密闭容器中催化反应后分子总数为3NA
D. pH=1的H3BO3溶液中,含有H+的总数为0.3NA
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】氧化还原反应与基本反应类型的关系如图所示,则下列化学反应属于氧化还原反应但不包含在1,2,4范围内的是

A.Cl2+2KI=I2 +2KCl
B.NH4HCO3=NH3↑+CO2↑+H2O↓
C.2FeCl2+Cl2=2FeCl3
D.3NO2+H2O=2HNO3 +NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列水解的离子方程式中书写正确的是
A. S2-+ H2O = HS-+OH- B. CH3COO- + H2O![]() CH3COOH + OH-
CH3COOH + OH-
C. Al3++ H2O =Al(OH)3 D. CO32-+ 2H2O![]() H2CO3+ 2OH-
H2CO3+ 2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知胆矾溶于水时溶液温度降低,室温下将1mol无水硫酸铜制成溶液时放出热量为Q1kJ,又知胆矾分解的热化学方程式为CuSO45H2O(s)═CuSO4(s)+5H2O(l)△H=+Q2kJmol-1则Q1、Q2的关系为
A. Q1<Q2 B. Q1>Q2 C. Q1=Q2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】著名的获得诺贝尔奖的狄尔斯—阿德尔反应,是由共轭双烯与烯烃或炔烃反应生成六元环的反应。如:
 (可表示为
(可表示为![]() ),实际是个加成反应。
),实际是个加成反应。
工业上常用下列流程制取重要化学原料![]() (M)。
(M)。

流程中的A为天然橡胶的单体,分子式为C5H8。
(1)A的名称是______,B的结构简式是______。
(2)A的属于炔烃的同分异构体一共有____种,A与B反应生成的另一种含六元环的化合物的结构简式为________。
(3)②反应的类型为_____,③反应的化学方程式为:________。
(4)按下列要求写出B的两种同分异构体的结构简式:__________。
(Ⅰ)能发生银镜反应;(Ⅱ)分子结构中含有两个甲基;(Ⅲ)能发生水解反应
(5)由丙烯制得B经如下流程:

参照流程中的前两步和最后一步的书写方法写出其他中间步骤的流程:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①标准状况下,6. 02×1023个分子所占的体积约是22. 4 L
②0. 5 mol H2所占体积为11. 2 L
③标准状况下,1 mol H2 O的体积为22.4 L
④标准状况下,28 g CO与N2的混 合气体的体积约为22. 4 L
⑤各种气体的气体摩尔体积都 约为22. 4 L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤B.④⑥C.③④⑥D.①④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种用途广泛的无机化工原料,一种以氧化铜矿(CuO,含有Fe2O3、Al2O3、SiO2杂质)为原料制备Cu2O的流程如图所示:

已知氨浸过程中仅发生的反应为:CuO+4NH3·H2O= [Cu(NH3)4]2++2OH-+3H2O
回答下列问题:
(1)氨浸之前需将矿物粉碎、过筛,目的是_______________________________。
(2)氨浸时的温度一般不超过30℃,主要原因是__________________。按此工艺,能否用NaOH溶液代替氨水?__________________(填“能”或“否”)。
(3)蒸馏过程中会生成一种黑色固体,则此过程中发生反应的化学方程式为____________。
(4)电解过程中阳极的电极反应式为_________________。
(5)Cu(OH)2也可与NH3·H2O反应,已知常温下:
Cu(OH)2(s)+4NH3·H2O(aq)![]() [Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
[Cu(NH3)4]2+(aq)+2OH-(aq)+4H2O(l) K1=4.4×10-7
Cu2+(aq)+4NH3·H2O(aq)![]() [Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
[Cu(NH3)4]2+(aq)+4H2O(l) K2=2.0×1013
则常温下Ksp[Cu(OH)2]=________________。
(6)为了尽量减少流程中所用原料的种类,还原过程可用气体A代替气体B,在加热条件下生成两种单质,该反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种重要的二元弱酸,还是一种重要的还原剂。草酸及草酸盐在工农业生产及科学研究领域均有广泛应用。
(1)请设计实验证明草酸为二元酸___________________________。
(2)已知草酸氢钾(KHC2O4)溶液显酸性,请结合必要的化学用语解释KHC2O4溶液显酸性的原因 ________。
(3)利用草酸及草酸盐的性质可测定人体血液中钙离子的浓度。方法如下:抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸,再用已知浓度的酸性KMnO4溶液滴定,使草酸转化成CO2逸出,根据消耗的KMnO4溶液的体积即可测定血液样品中Ca2+的浓度。
①写出草酸与酸性KMnO4溶液反应的离子方程式______________。
②抽取血样10.00mL,经过上述处理后得到草酸,再用硫酸酸化的0.010mol/L KMnO4溶液滴定。在向滴定管中注入KMnO4标准溶液前,滴定管需要检漏、____和___。确定反应达到终点的现象是__。
③滴定结束共消耗12.00mL KMnO4溶液。则血液样品中Ca2+离子的浓度为______mg/mL。
④下列操作可能使所测定结果偏高的是_________。
A.酸式滴定管未用标准液润洗就直接注入酸性高锰酸钾溶液
B.滴定前盛放待测液的锥形瓶用蒸馏水洗净后未干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.滴定结束后读取标准液体积时,俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。由题干及图形可知,V1∶V2=________时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为__________mol/L。若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液______;氨水(NH3·H2O)___________。

(2)用惰性电极进行电解下列电解质溶液。
①电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为___________
②MnO2可做超级电容器材料,电解MnSO4溶液可制得MnO2,其阳极的电极反应式_________________
(3)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为: 7.1 10-4, 2.98 10-8。将0.1mol/L的亚硝酸稀释100倍,c(H+)将_______(填“不变”、“增大”、“减小”)。写出HNO2、HClO、NaNO2、NaClO四种物质之间发生的复分解反应的离子方程式_______________。
(4)酸HX和碱AOH恰好完全中和时溶液的pH等于7,酸HY和碱BOH恰好完全中和时溶液的pH也等于7,酸HX和碱BOH恰好完全中和时溶液的pH小于7,请推断
①以上酸碱中必为弱电解质的是_______________
②比较两种酸HX和HY的酸性强弱 ___________>___________
(5)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xS![]() Na2Sx,正极的电极反应式为_________。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的__________
Na2Sx,正极的电极反应式为_________。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的__________
倍。

(6)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.0![]() 10-38、1.0
10-38、1.0![]() 10-11,向浓度均为0.1 mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是________。(已知lg 2=0.3)
10-11,向浓度均为0.1 mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是________。(已知lg 2=0.3)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com