
| ||
| 1.12L |
| 22.4L/mol |
| 27.4g |
| 2 |
| 5.3g |
| 106g/mol |
| V |
| 22.4 |
| ||
| 1.12L |
| 22.4L/mol |
| 27.4g |
| 2 |
| 5.3g |
| 106g/mol |
| V |
| 22.4 |
| 0.2mol |
| 0.1L |


 ��ĩ���ƾ�ϵ�д�
��ĩ���ƾ�ϵ�д� ���ɿ��ñ���ϵ�д�
���ɿ��ñ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
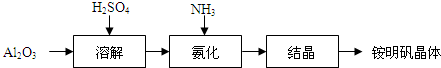
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
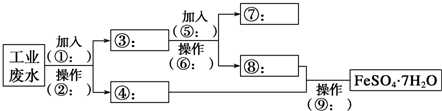
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ü�ʽ�ζ�����ȡһ������Ĵ���״�����ƿ�� |
| B����ȡ4.0gNaOH��1000mL����ƿ��ˮ���̶ȣ����1.00 mol?L-1NaOH����Һ |
| C����NaOH��Һ�ζ��״ף�ʹ�÷�̪��ָʾ������Һ��ɫǡ������ɫ��Ϊdz��ɫ���Ұ�����ڲ���ɫʱ��Ϊ�ζ��յ� |
| D���ζ�ʱ�۾�Ҫע���ŵζ�����NaOH��Һ��Һ��仯����ֹ�ζ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��2 | B��1��3 |
| C��3��1 | D��2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
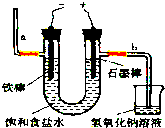
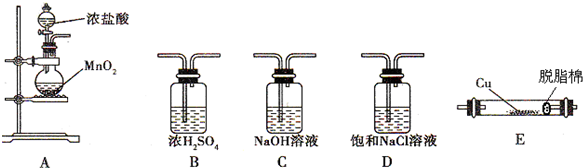
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
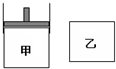 ����ֻ�ܱ��������ң���������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ���������ܱ��ֺ��ݣ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��M��N�Ļ�����壬��ʹ�����ݻ���ȣ�����ͼ��ʾ�����ڱ���400���������ʹ֮�������·�Ӧ��2M��g��+N��g��?2Q��g�������ﵽƽ�⣮����˵����ȷ���ǣ�������
����ֻ�ܱ��������ң���������һ�������ƶ��Ļ�����ʹ�����ڱ��ֺ�ѹ���������ܱ��ֺ��ݣ���ʼʱ�������������зֱ��������ʵ����������Ϊ2��1��M��N�Ļ�����壬��ʹ�����ݻ���ȣ�����ͼ��ʾ�����ڱ���400���������ʹ֮�������·�Ӧ��2M��g��+N��g��?2Q��g�������ﵽƽ�⣮����˵����ȷ���ǣ�������| A���������ﵽƽ��ʱ�����ʱ����������� |
| B��ƽ��ʱ��������M��ת���ʱ�������С |
| C��ƽ���������������ͨ����������ĵ����ʵ�����������������л�ѧƽ�����淴Ӧ�����ƶ����������л�ѧƽ�ⲻ�ƶ� |
| D��ƽ���������������ͨ������ʵ�����ԭ��Ӧ���壬�ﵽƽ��ʱ���������Ļ��������Q�����������С���������Ļ��������Q������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����H1��0����H2��0 |
| B����H3��0����H4��0 |
| C����H3=��H1-��H2 |
| D����H4=2��H5-3��H3 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com