
【题目】A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去). 
(1)若A为强碱溶液,其焰色反应显黄色,C常用作食品添加剂,请回答下列问题:
①物质的量浓度相同的B、C水溶液的pH前者(填大于或小于)后者.
②反应Ⅲ的离子方程式是 .
③现有B和C的固体混合物ag,加热至质量不再改变时剩余固体为bg,则B的质量分数为 .
(2)若C、D均为金属单质,向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则:①反应 III的离子方程式是 .
②实验室中储存B溶液时应加入 .
③检验溶液A中金属阳离子的方法是 .
(3)若D为强电解质、B为难溶于水的沉淀,
①则A和C反应的离子方程式
②符合条件的D物质可能是下列物质中的(填序号).
a.硫酸 b.醋酸 c.氢氧化钠 d.氨水 e.氯化钡 f.硝酸镁.
【答案】
(1)大于;HCO3﹣+OH﹣=H2O+CO32﹣;![]() ×100%
×100%
(2)2Fe3++Fe=3Fe2+;铁与盐酸;取少量溶液于试管中,滴入KSCN溶液,溶液呈血红色
(3)Al3++3AlO2﹣+6H2O=4Al(OH)3↓;ac
【解析】解:(1)若A为强碱,其焰色反应显黄色,应为NaOH,C常用作食品添加剂,结合转化关系可知B为Na2CO3 , C为NaHCO3 , D为CO2 , ①物质的量浓度相同的B、C水溶液,碳酸钠溶液中碳酸根离子水解程度大于碳酸氢根离子,得到溶液的pH碳酸钠溶液大,所以答案是:大于;②反应Ⅲ为NaHCO3和NaOH的反应,反应的离子方程式是HCO3﹣+OH﹣=H2O+CO32﹣ , 所以答案是:HCO3﹣+OH﹣=H2O+CO32﹣;③B为Na2CO3 , C为NaHCO3 , 现有B和C的固体混合物ag,加热至质量不再改变时剩余固体为bg,混合物中碳酸氢钠分解产生的水和二氧化碳的质量为(a﹣b)g,根据关系2NaHCO3~H2O+CO2 , 可求得混合物中NaHCO3的质量为 ![]() =
= ![]() (a﹣b)g,Na2CO3的质量为ag﹣
(a﹣b)g,Na2CO3的质量为ag﹣ ![]() (a﹣b)g,所以Na2CO3的质量数为
(a﹣b)g,所以Na2CO3的质量数为 ![]() ×100%=
×100%= ![]() ×100%,所以答案是:
×100%,所以答案是: ![]() ×100%;(2)向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,说明A中含有Cl﹣,连续加入D可置换出金属单质,说明A中含有的金属元素为变价金属,应为Fe,则A为FeCl3 , B为FeCl2 , C为Fe,D为活泼性比Fe强的金属,①反应 III是铁离子和铁反应生成亚铁离子,反应的离子方程式是:2Fe3++Fe=3Fe2+ , 所以答案是:2Fe3++Fe=3Fe2+;②由于FeCl2具有还原性且易水解,保存时应加入盐酸抑制水解,加入铁粉防止氧化,所以答案是:铁与盐酸;③检验FeCl3溶液中含有铁离子的方法是:取少量溶液于试管中,向溶液中滴加少量KSCN溶液,溶液呈血红色,所以答案是:取少量溶液于试管中,滴入KSCN溶液,溶液呈血红色;(3)①若D为强电解质、B为难溶于水的沉淀,难溶于水的沉淀时应为Al(OH)3 , A为Al3+ , C为AlO2﹣ , A和C反应的离子方程式是Al3++3AlO2﹣+6H2O=4Al(OH)3↓,所以答案是:Al3++3AlO2﹣+6H2O=4Al(OH)3↓;②Al(OH)3既能与强酸反应,也能与强碱反应,则D可为硫酸或NaOH,
×100%;(2)向A溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,说明A中含有Cl﹣,连续加入D可置换出金属单质,说明A中含有的金属元素为变价金属,应为Fe,则A为FeCl3 , B为FeCl2 , C为Fe,D为活泼性比Fe强的金属,①反应 III是铁离子和铁反应生成亚铁离子,反应的离子方程式是:2Fe3++Fe=3Fe2+ , 所以答案是:2Fe3++Fe=3Fe2+;②由于FeCl2具有还原性且易水解,保存时应加入盐酸抑制水解,加入铁粉防止氧化,所以答案是:铁与盐酸;③检验FeCl3溶液中含有铁离子的方法是:取少量溶液于试管中,向溶液中滴加少量KSCN溶液,溶液呈血红色,所以答案是:取少量溶液于试管中,滴入KSCN溶液,溶液呈血红色;(3)①若D为强电解质、B为难溶于水的沉淀,难溶于水的沉淀时应为Al(OH)3 , A为Al3+ , C为AlO2﹣ , A和C反应的离子方程式是Al3++3AlO2﹣+6H2O=4Al(OH)3↓,所以答案是:Al3++3AlO2﹣+6H2O=4Al(OH)3↓;②Al(OH)3既能与强酸反应,也能与强碱反应,则D可为硫酸或NaOH,
所以答案是:ac.


科目:高中化学 来源: 题型:
【题目】在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO42﹣=0.2mol/L,当加等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的浓度是( )
A.0.2 mol/L
B.0.25 mol/L
C.0.45 mol/L
D.0.225 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O.实验过程如图1: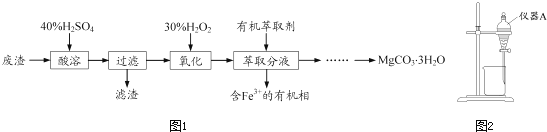
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(S)+2H+(aq)═Mg2+(aq)+CO2(g)+H2O(l)△H=﹣50.4kJmol﹣1
Mg2SiO4(s)+4H+(aq)═2Mg2+(aq)+H2SiO3(s)+H2O(l)△H=﹣225.4kJmol﹣1
酸溶需加热的目的是;所加H2SO4不宜过量太多的原因是 .
(2)加入H2O2氧化时发生发应的离子方程式为 .
(3)用图2所示的实验装置进行萃取分液,以除去溶液中的Fe3+ .
①实验装置图中仪器A的名称为 .
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,、静置、分液,并重复多次.
(4)请补充完整由萃取后得到的水溶液制备MgCO33H2O的实验方案:边搅拌边向溶液中滴加氨水, , 过滤、用水洗涤固体2﹣3次,在50℃下干燥,得到MgCO33H2O.
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单原子的原子结构可用下图的表示方法形象表示,其中●表示质子或电子,○表示中子,则有关①②③的叙述正确的是( ) 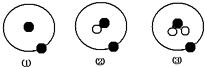
A.①②③是化学性质不同的粒子
B.①不是核素,②③才是核素
C.①②③具有相同的质量数
D.①②③互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 钠、铁均是银白色金属,熔点高,硬度大
B. 实验室中,通常将钠保存在四氯化碳中
C. 钠在空气中燃烧产生黄色火焰
D. 高温时,铁与水蒸气反应生成氧化铁与氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A.已知2H2(g)+O2(g)=2H2O(g);△H=﹣483.6 kJmol﹣1氢气的燃烧热为241.8 kJmol﹣1
B.已知NaOH(ag)+HCl(aq)=NaCl(aq)+H2O(l);△H=﹣57.4 kJmol﹣1 , 则含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7kJ/mol的热量
C.已知C(石墨,s)=C(金刚石,s);△H>0 则石墨比金刚石稳定
D.己知C(s)+O2(g)=CO2(g);△H1C(s)+1/2O2(g)=CO(g);△H2 , 则△H1>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2 , X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法正确的是( )
A.气态氢化物的沸点:W<T<R
B.离子半径:T﹣>R2﹣
C.最高价氧化物对应的水化物碱性:Y>X
D.XR2、WR2两化合物含有的化学键的类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O
将2.56g铜放入14mL浓硝酸中,随着铜的不断减少,反应生成的气体颜色逐渐变浅.当铜片完全消失时,收集到干燥的NO、NO2混合气体,换算成标准状况下体积为1.344L(忽略气体的溶解及转化).请回答下列问题:
(1)反应中被还原的HNO3的物质的量是mol.
(2)生成气体中NO与NO2的体积比是
(3)该浓HNO3的物质的量浓度≥molL﹣1 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com