
【题目】(实验化学)某课外活动小组学生模拟呼吸面具中的原理(过氧化钠与潮湿二氧化碳反应),设计用下图所示的仪器来制取氧气并测量氧气的体积.如图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水.甲管有刻度(0~50mL),供量气用;乙管可上下移动,以调节液面高低. 
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水试回答:
(1)上述装置的连接顺序是(填各接口的编号,其中连接胶管及夹持装置均省略): .
(2)装置C中放入的反应物是和 .
(3)装置A的作用是 , 装置B的作用是 .
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意和(填写字母编号).
a.视线与凹液面最低数相平b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平d.读数时不一定使甲、乙管液面相平.
【答案】
(1)53467218(6、7可颠倒)
(2)大理石;盐酸
(3)吸收氧气中未反应的二氧化碳;吸收中混有的HCl
(4)a;c
【解析】解:(1)仪器C可以用来制取二氧化碳,连接3用来除去HCl,4连接6可使二氧化碳与过氧化钠反应生成氧气,然后连接2可除去未反应的二氧化碳,最后连接8测量气体的体积,所以顺序为53467218(6、7可颠倒),
所以答案是:53467218(6、7可颠倒);(2)只有仪器C可以用来制取二氧化碳,制气原料应该采用大理石和盐酸,可在C中加止水夹,可控制反应的进行,
所以答案是:大理石;盐酸;(3)仪器C可以用来制取二氧化碳,此法制得的二氧化碳中会含有少量氯化氢,须通过装有碳酸氢钠溶液的洗气瓶,以除去这些氯化氢,净化后的二氧化碳通过过氧化钠来制取氧气,为了除去生成的氧气中混有未反应的二氧化碳,可以使它们通过仪器A,所以答案是:吸收氧气中未反应的二氧化碳;吸收中混有的HCl;(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数.求其差值的过程中,应注意:①读数时要调节E中甲乙的液面使其同一高度;②读数时视线要与凹液面最低处相平,所以答案是:a、c.


科目:高中化学 来源: 题型:
【题目】某元素X,它的原子最外层电子数是次外层电子数的2倍,则X在周期表中位于
A. 第二周期IVA族 B. 第三周期IVA族
C. 第二周期VIA族 D. 第三周期VIA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃、101 kPa下,如下图所示,石墨的燃烧热为一393.51 kJ·mol-1,金刚石的燃烧热为一395.4kJ·mol-1。下列表达正确的是

A. 金刚石比石墨稳定
B. C(s、石墨)=C(s、金刚石) △H=+1.9 kJ/mol
C. △H1<△H2
D. 如果使用催化剂,△H1和△H2都变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于ⅣA族元素,下列叙述中不正确的是( )
A. CO2在常温下是气体,SiO2在常温下是固体
B. C、Si、Ge的最外层电子数都是4,次外层电子数都是8
C. CO2和SiO2都是酸性氧化物,在一定条件下都能和氧化钙反应
D. 该族元素的主要化合价是+4和+2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS 等)来制备,其工艺流程如下:

回答下列问题:
(1)“浸泡除铝”时,发生反应的离子反应方程式为_________________________;
(2)“溶解”时放出的气体为_______________ (填化学式);
(3)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH 1”时,溶液pH范围为______________________;
(4)在空气中加热Ni(OH)2可得NiOOH,请写出此反应的化学方程式_____________;

(5)金属铬在溶液中有多种存在形式, CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol/L的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示,用离子方程式表示Na2CrO4溶液中的转化反应________________,根据A点数据计算出该转化反应的平衡常数为______________,温度升高,溶液中CrO42—的平衡转化率减小,则该反应的△H____0(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1mol/L氨水溶液的pH =a,下列能使溶液pH =(a -1)的措施是
A. 将溶液稀释到原体积的10倍B. 加入适量的氯化铵固体
C. 加入等体积0.1 mol/L烧碱溶液D. 加入等体积0.1 mol/L盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( ) 
A.简单离子的半径:X<Z<M
B.Y,R两种元素的气态氢化物稳定性:Y>R
C.最高价氧化物对应水化物的酸性:R<N
D.由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是
A. Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++12HCO3-+2OH-=CaCO3 ↓+CO32-+H2O
B. 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+3H2O
C. 将饱和FeC3溶液滴入沸水中制胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
D. 以铜为电极电解饱和食盐水:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化物是一类重要化合物,在炸药、磁性化合物研究、微量元素测定方面越来越引起人们的重视,其中氢叠氮酸(HN3)是一种弱酸,分子结构示意图可表示为:
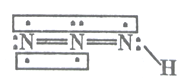
联氨被亚硝酸氧化时便可生成氢叠氮酸(HN3):N2H4+HNO2=2H2O+HN3,它的酸性类似于醋酸,微弱电离出H+和N3-。试回答下列问题:
(1)从成键原子的电负性角度,HN3中含有的共价键类型为_______________,分子的极性为_____________。
(2)叠氮化物能与Fe3+、Cu2+、Co3+等形成配合物,如:Co[(N3)(NH3)5]SO4,在该配合物中钴显_________价,根据价层互斥理论可知SO42-空间形状为______________,写出钴原子在基态时的核外电子排布式_____________。
(3)由叠氮化钠(NaN3)热分解可得纯N2:2NaN3(s)=2Na(l)+3N2(g),有关说法正确的是__________(选填序号)
A.NaN3与KN3结构类似,前者晶格能较小
B.钠晶胞结构如图![]() ,晶胞中分摊2个钠原子
,晶胞中分摊2个钠原子
C.氮的第一电离能大于氧
D.氮气常温下很稳定,是因为氮的电负性小
(4)与N3-互为等电子体的分子有___________________ (举2例)
(5)人造立方氮化硼的硬度仅次于金刚石而远远高于其他材料,因此它与金刚石统称为超硬材料。立方氮化硼晶胞如图所示,试分析:
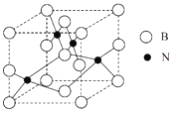
①该晶体的类别为____________晶体。
②晶体中每个N同时吸引________个B。
③设该晶体的摩尔质量为Mg·mol-1,晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶体中两个距离最近的B之间的距离为___________cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com