
【题目】将不可再生的天然气、石油、煤等化石燃料转化利用、变废为宝已成为当务之急。
(1)根据键能数据估算CH4+4F2=CF4+4HF的反应热ΔH= 。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
(2)甲醇、二甲醚(CH3OCH3)被称为21世纪的新型燃料,均可利用CO和H2反应合成。
①某燃料电池以二甲醚为原料,熔融碳酸盐为电解质,其负极反应如下:
CH3OCH3+6CO![]() -12e-=8CO2+3H2O。写出该燃料电池的正极反应式: 。
-12e-=8CO2+3H2O。写出该燃料电池的正极反应式: 。
②废水中含甲醇对水质会造成污染,Co3+可将甲醇氧化为CO2。某同学以Pt作电极电解酸性含甲醇废水与CoSO4混合液模拟工业除污原理,其阳极反应式为 。
(3)某企业采用如图所示原理处理化石燃料开采、加工过程产生的H2S废气。
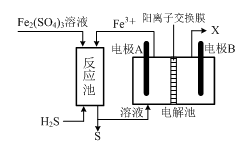
①电解池中电极A、B均为惰性电极,其中A为电解池的 极;电极B所得到的物质X的分子式为 。
②反应池中发生的离子反应方程式为 。
【答案】(1)–1940 kJ·mol-1
(2)①2CO2+O2+4e-=2CO![]() (或将各计量数扩大3倍)②Co2+-e-=Co3+
(或将各计量数扩大3倍)②Co2+-e-=Co3+
(3)①阳 H2②H2S+2Fe3+=2Fe2++S↓+2H+
【解析】
试题分析:(1)根据键能数据,焓变等于反应物的总键能-生成物的总键能,CH4+4F2=CF4+4HF的反应热ΔH=414×4+155×2-489×4-565×4=–1940 kJ·mol-1;(2)①原电池正极发生还原反应,某燃料电池以二甲醚为原料,熔融碳酸盐为电解质正反应为![]() ,其负极反应CH3OCH3+6CO
,其负极反应CH3OCH3+6CO![]() -12e-=8CO2+3H2O。该燃料电池的正极反应式=总反应-负极反应,正极反应式CO2+O2+4e-=2CO
-12e-=8CO2+3H2O。该燃料电池的正极反应式=总反应-负极反应,正极反应式CO2+O2+4e-=2CO![]() ;②阳极发生氧化反应,阳极反应式为Co2+-e-=Co3+;(3)根据图示,A极有Fe3+生成,A是阳极,B是阴极发生还原反应,
;②阳极发生氧化反应,阳极反应式为Co2+-e-=Co3+;(3)根据图示,A极有Fe3+生成,A是阳极,B是阴极发生还原反应,![]() ,B所得到的 物质X的分子式为H2;②根据图示反应池中发生的离子反应方程式为H2S+2Fe3+=2Fe2++S↓+2H+。
,B所得到的 物质X的分子式为H2;②根据图示反应池中发生的离子反应方程式为H2S+2Fe3+=2Fe2++S↓+2H+。


科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某氨基酸(CxHyNzOp)的分子组成。取m g 该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。按下图所示装置进行实验。

请回答下列问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是__________________
(2)以上装置中需要加热的仪器有_________________(用字母填空,下同)。操作时应先点燃_______处的酒精灯。
(3)A装置中发生反应的化学方程式是_____________________。
(4)装置D的作用是___________________________。
(5)读取N2的体积时,应注意
①______________________
②______________________
③______________________
(6)实验中测得N2的体积为V mL(标准状况)。为确定此氨基酸的化学式,还需要的有关数据是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
A.向NaAlO2溶液中通入足量CO2,有白色沉淀产生,说明碳酸的酸性强于氢氧化铝
B.用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,说明溶液中不含有K+
C.在KI淀粉溶液中滴入氯水变蓝,再通入SO2,蓝色褪去,说明SO2具有漂白性
D.向某FeCl2溶液中,加入Na2O2粉末出现红褐色沉淀,说明原FeCl2已氧化变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯水中含有多种成分,因而具有多种性质,根据氯水分别与下图中四种物质发生的反应填空(a、b、c、d重合部分代表物质间可反应,且氯水足量)。

(1)能证明氯水具有漂白性的是_____(填“a”“b”“c”或“d”)。
(2)c过程中的现象是______________
b过程中发生反应的离子方程式为__。
(3)a过程中发生反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中铝制品比铁制品耐腐蚀的原因是( )
A.铝的活泼性不如铁B.铝与空气中的氧气不易发生化学反应
C.铝易在空气中形成致密的氧化膜D.铝的密度比铁的密度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸是一种重要的化工原料。实验室合成苯甲酸的原理、有关数据及装置示意图如下:


名称 | 性状 | 熔点/℃ | 沸点/℃ | 密度(g/mL) | 水溶性 |
甲苯 | 无色易挥发液体 | -95 | 110.6 | 0.8669 | 不溶 |
苯甲酸 | 白色晶体 | 112.4 | 248 | 1.2659 | 微溶 |
苯甲酸在水中的溶解度表:
温度/℃ | 25 | 50 | 95 |
溶解度/g | 0.344 | 0.849 | 6.8 |
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈瓶中加入2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加入8.5g KMnO4(过量),继续搅拌约4~5 h,直至反应完全,停止加热和搅拌,静置。
二、分离提纯
将反应混合液放在冰水浴中冷却,然后用稀硫酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,干燥,得到粗产品。
三、测定纯度
称取m g产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3指示剂,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)仪器a的名称是____________,其作用为_________________________。
(3)分离提纯阶段产品减压过滤时用冷水洗涤的原因是______________________________。
(4)进一步提纯苯甲酸粗产品的操作是_____________。
(5)测定纯度阶段,所选的指示剂为_________,滴定终点的现象是________________。若m=1.200 g,滴定时用去0.1200 mol/L标准KOH溶液20.00 mL,则所得产品中苯甲酸的纯度(质量分数)为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新鲜水果、蔬菜、乳制品中富含的维生素C,具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下:
下列说法正确的是( )
A. 上述反应为取代反应
B. 维生素C不可溶于水,可溶于有机溶剂
C. 维生素C在酸性条件下水解只得到1种产物
D. 脱氢维生素C的分子式为C6H8O6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【浙江教育绿色评价联盟2017届高三3月适应性试卷】下图分别代表NaCl、金刚石、干冰、石墨结构的一部分。下列说法正确的是( )

A. NaCl晶体只有在熔融状态下离子键被完全破坏,才能形成自由移动的离子
B. 金刚石中存在的化学键只有共价键,不能导电
C. 干冰中的化学键只需吸收很少的热量就可以破坏,所以干冰容易升华
D. 石墨中碳原子的最外层电子都参与了共价键的形成,故熔点很高、硬度很大。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com