
【题目】自然界水体中的碳元素主要以碳酸盐、碳酸氢盐和有机物形式存在。水体中有机物含量是水质的重要指标,常用总有机碳衡量(总有机碳=![]() )。
)。
某学生兴趣小组用如下实验方法测定采集水样的总有机碳。

步骤1:量取50 mL水样,加入足量硫酸,加热,通N2,并维持一段时间(装置见右图,夹持类仪器省略)。
步骤2:再向水样中加入过量的K2Cr2O7溶液(可将有机物中的碳元素氧化成CO2),加热,充分反应,生成的CO2完全被100 mL 0.205 mol·L-1的Ba(OH)2溶液吸收。
步骤3:将吸收CO2后的浊液过滤并洗涤沉淀,再将洗涤得到的滤液与原滤液合并,加水配制成500 mL溶液。量取25.00 mL溶液于锥形瓶中,加入指示剂,并滴加0.050 00 mol·L-1的H2C2O4溶液,发生反应:Ba(OH)2+H2C2O4===BaC2O4↓+2H2O,恰好完全反应时,共消耗H2C2O4溶液20.00 mL。
(1)步骤1的目的是________。
(2)计算水样的总有机碳(以mg·L-1表示),并写出计算过程。____________
(3)用上述实验方法测定的水样总有机碳一般低于实际值,其原因可能是__________________________________________。
(4)高温燃烧可将水样中的碳酸盐、碳酸氧盐和有机物所含碳元素转化为CO2,结合高温燃烧的方法,改进上述实验。
①请补充完整改进后的实验方案:取V L的水样,分为两等份;将其中一份水样高温燃烧,测定生成CO2的物质的量为n1 mol;____________________________________,测定生成CO2的物质的量为n2 mol。
②利用实验数据计算,所取水样的总有机碳为________mg·L-1(用含字母的代数式表示)。
【答案】 将水样中的CO![]() 和HCO
和HCO![]() 转化为CO2,并将CO2完全赶出 n(H2C2O4)=
转化为CO2,并将CO2完全赶出 n(H2C2O4)=![]() =1.000×10-3 mol,与H2C2O4反应的Ba(OH)2的物质的量n1[Ba(OH)2]=n(H2C2O4)=1.000×10-3 mol与CO2反应的Ba(OH)2的物质的量n2[Ba(OH)2]=
=1.000×10-3 mol,与H2C2O4反应的Ba(OH)2的物质的量n1[Ba(OH)2]=n(H2C2O4)=1.000×10-3 mol与CO2反应的Ba(OH)2的物质的量n2[Ba(OH)2]= ![]() -1.000×10-3 mol×
-1.000×10-3 mol×![]() =5.000×10-4 mol,由水样中有机物转化而成CO2的物质的量,n(CO2)=n2[Ba(OH)2]=5.000×10-4 mol,水样中有机物所含碳元素的物质的量n(C)=n(CO2)=5.000×10-4 mol,水样的总有机碳=
=5.000×10-4 mol,由水样中有机物转化而成CO2的物质的量,n(CO2)=n2[Ba(OH)2]=5.000×10-4 mol,水样中有机物所含碳元素的物质的量n(C)=n(CO2)=5.000×10-4 mol,水样的总有机碳=![]() =120 mg·L-1 加热过程中,损失了部分易挥发有机物 向另一份水样中加入足量硫酸,加热,通N2,维持一段时间
=120 mg·L-1 加热过程中,损失了部分易挥发有机物 向另一份水样中加入足量硫酸,加热,通N2,维持一段时间 ![]()
【解析】(1)碳酸盐与稀硫酸反应生成二氧化碳,则步骤1的目的是将水样中的CO32-和HCO3-转化为CO2,并将CO2完全赶出。(2)n(H2C2O4)=![]() =1.000×10-3mol,与H2C2O4反应的Ba(OH)2的物质的量n1[Ba(OH)2]=n(H2C2O4)=1.000×10-3mol。与CO2反应的Ba(OH)2的物质的量n2[Ba(OH)2]=
=1.000×10-3mol,与H2C2O4反应的Ba(OH)2的物质的量n1[Ba(OH)2]=n(H2C2O4)=1.000×10-3mol。与CO2反应的Ba(OH)2的物质的量n2[Ba(OH)2]=![]() -1.000×10-3 mol×
-1.000×10-3 mol×![]() =5.000×10-4 mol,由水样中有机物转化而成CO2的物质的量,n(CO2)=n2[Ba(OH)2]=5.000×10-4 mol,水样中有机物所含碳元素的物质的量n(C)=n(CO2)=5.000×10-4 mol,水样的总有机碳=
=5.000×10-4 mol,由水样中有机物转化而成CO2的物质的量,n(CO2)=n2[Ba(OH)2]=5.000×10-4 mol,水样中有机物所含碳元素的物质的量n(C)=n(CO2)=5.000×10-4 mol,水样的总有机碳=![]() =120 mg·L-1;(3)由于加热过程中损失了部分易挥发有机物,因此测定的水样总有机碳一般低于实际值。(4)由于碳酸盐能与酸反应生成二氧化碳,则另一种方案为向另一份水样中加入足量硫酸,则根据碳原子守恒可知所取水样的总有机碳为
=120 mg·L-1;(3)由于加热过程中损失了部分易挥发有机物,因此测定的水样总有机碳一般低于实际值。(4)由于碳酸盐能与酸反应生成二氧化碳,则另一种方案为向另一份水样中加入足量硫酸,则根据碳原子守恒可知所取水样的总有机碳为![]() =
=![]() mg·L-。
mg·L-。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】有机物H (结构简式为 )是合成高分子化合物M的单体,H可以通过有机物A (分子式为C7H8O) 和丙酮为原料来进行合成,E为中间产物(结构简式为
)是合成高分子化合物M的单体,H可以通过有机物A (分子式为C7H8O) 和丙酮为原料来进行合成,E为中间产物(结构简式为 )其合成路线如图:
)其合成路线如图:

己知:![]()
请回答下列问题:
(1)A的名称为_________,G 中含氧官能团的名称是________________;①的反应类型是__________。
(2)检验有机物A中官能团的方法为______________________________。
(3)高分子化合物M 的结构简式为____________________。
(4)反应③的化学反应方程式为______________________________。
(5)有机物C有多种同分异构体,其中苯环上只有两个侧链的芳香酯的同分异构体有__________种
(6)已知: ,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成
,以2-溴丙烷和乙烯为原料,选用必要的无机试剂合成![]() ,此合成路线为
,此合成路线为 ,请完成接下来的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上下注明试剂和反应条件)。____________
,请完成接下来的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上下注明试剂和反应条件)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PASNa(二水合对氨基水杨酸钠)是抗结核药,其结构简式如图化合物1所示,下列说法正确的是( ) 
A.化合物1和化合物2均能使酸性KMnO4溶液褪色
B.化合物1的核磁共振氢谱测出5个谱峰
C.PASNa与足量盐酸反应生成如上图化合物2
D.通入足量CO2能将图化合物3转化为PASNa
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分: ![]()
(1)①用酸性高锰酸钾溶液检验甲和乙中含有碳碳双键,方案是否可行(填“可 行”或“不可行”).
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 .
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物): 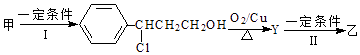
步骤Ⅰ的反应类型为 , Y的结构简式 , 设计步骤Ⅰ的目的是 .
(3)1mol乙最多可与 mol H2发生加成反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容密闭容器中,当下列物理量不再变化时,可表明反应:A(g)+B(g)![]() C(g)+D(g) 已达化学平衡状态的是( )
C(g)+D(g) 已达化学平衡状态的是( )
A. 混合气体的压强 B. B的物质的量浓度 C. 混合气体的密度 D. v(A)正 = v(D)正
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.2000molL ﹣1的氢氧化钠溶液(指示剂为酚酞),滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 18.00mL |
(1)根据以上数据可以计算出盐酸的物质的量浓度为molL﹣1 .
(2)达到滴定终点的标志是 .
(3)以下操作造成测定结果偏高的原因可能是 .
A.配制标准溶液的氢氧化钠中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E.未用标准液润洗碱式滴定管.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com