
【题目】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出___kJ热量。
(2)如图装置中仪器A的名称___,作用是___;仪器B的名称___,作用是___;碎泡沫塑料的作用是___。
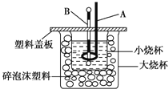
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是___。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会___(填“偏大”、“偏小”或“无影响”)。
【答案】11.46 环形玻璃搅拌 搅拌,使溶液充分混合 温度计 测量温度 减少实验过程中的热量损失 实验中不可避免的有少量热量损失 偏小
【解析】
(1)根据H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJmol-1可知生成1molH2O放出热量为57.3kJ,然后根据水的物质的量与热量成正比求出热量;
(2)根据常见仪器的用途来解答;
(3)若保温效果不好,有热量散失;
(4)根据弱电解质电离吸热分析。
(1)由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJmol-1可知生成1molH2O放出热量为57.3kJ,而0.1molBa(OH)2配成稀溶液与足量稀硝酸反应可得0.2molH2O,所以放出的热量为57.3kJ×0.2=11.46kJ;
(2)仪器A的名称是环形玻璃搅拌棒,其作用是搅拌,使溶液充分混合;仪器B的名称是温度计,其作用是测量温度;
(3)若保温效果不好,有热量散失,求得的中和热数值将会减小,但中和热为负值,所以中和热的△H大于-57.3kJmol-1;
(4)NH3H2O为弱碱,电离过程为吸热过程,用相同浓度和体积的氨水(NH3H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列说法不正确的是![]()
A.酸雨样品露天放置一段时间,酸性增强,是因为发生了氧化还原反应
B.纳米铁粉可将地下水中的![]() 转化为
转化为![]() ,是因为纳米铁粉具有还原性
,是因为纳米铁粉具有还原性
C.将草木灰与![]() 混合施用,可更好为植物全面提供N、P、K三种营养元素
混合施用,可更好为植物全面提供N、P、K三种营养元素
D.生活中常用可溶性铝盐净水,可加速水中悬浮物沉降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列化合物:①NaCl ②NaOH ③HCl ④NH4Cl ⑤CH3COONa ⑥CH3COOH ⑦NH3H2O ⑧H2O,回答下列问题.
(1)NH4Cl溶液显酸性,用离子方程式表示原因 ,其溶液中离子浓度大小顺序为 。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH﹣)= ,在pH=3的CH3COOH溶液中,水电离出来的c(H+)= 。
(3)若将等pH、等体积的②NaOH和⑦NH3H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m n。(填“<”、“>”或“=”)
(4)若前五种溶液的物质的量浓度相同,用序号排出这五种溶液pH由大到小的顺序 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 表示放热反应,
表示放热反应,![]() 表示吸热反应
表示吸热反应
B.在化学反应中发生物质变化的同时,不一定发生能量变化
C.![]() 的大小与热化学方程式中化学计量数有关
的大小与热化学方程式中化学计量数有关
D.生成物释放的总能量大于反应物吸收的总能量时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
a.化石燃料在任何条件下都能充分燃烧
b.化石燃料在燃烧过程中能产生污染环境的CO、![]() 等有害气体
等有害气体
c.直接燃烧煤不如将煤进行深加工后再燃烧的效果好
d.固体煤变为气体燃料后,燃烧效率更低
A.adB.bcdC.bcD.acd
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
CO2(g)+H2(g) ΔH<0。CO和H2O的浓度变化如图所示。
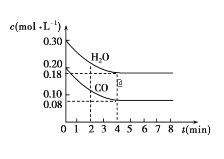
请解答下列各题:
(1)0~4min内的平均反应速率v(CO)=___mol/(L·min),v(H2)=___mol/(L·min),v(CO2)=___mol/(L·min)。
(2)请你在图中标出CO2和H2的浓度变化。___
(3)T℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表。
时间(min) | 0 | 2 | 3 | 4 | 5 | 6 |
CO | 0.200 | 0.138 | c1 | c1 | 0.116 | 0.096 |
H2O | 0.300 | 0.238 | c2 | c2 | 0.216 | 0.266 |
CO2 | 0 | 0.062 | c3 | c3 | 0.084 | 0.104 |
H2 | 0 | 0.062 | c4 | c4 |
①表中3min~4min之间,反应处于___状态;c1___0.08mol/L(填“大于”、“小于”或“等于”)。
②反应在4min~5min之间,平衡向逆反应方向移动,可能的原因是___(单选),表中5min~6min之间数值发生变化,可能的原因是___(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列两题:
(1)向硫酸锌水溶液中滴加适当浓度的氨水至过量,发生两步主要反应。简述实验现象并写出两步主要反应的离子方程式__________。
(2)1976年中子衍射实验证实:trans-[Co(en)2Cl2]2Cl·HCl·2H2O晶体中只存在3种离子,X+、含钴的A+和Cl-。X+中所有原子共面,有对称中心和3个相互垂直的镜面。(en是乙二胺的缩写符号)。 画出A+及其立体异构体的结构简图__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酞菁钴被广泛应用于光电材料、光动力学光敏材料等方面。酞菁钴(II)结构如图所示(Co均形成单键,部分化学键未画明)。下列说法错误的是( )
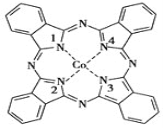
A.酞菁钴(II)中三种非金属元素的电负性大小顺序为N>C>H
B.酞菁钴(II)中碳原子的杂化方式只有sp2杂化
C.1号和3号N原子的VSEPR模型均为平面三角形
D.2号和4号N原子与Co(Ⅱ)是通过配位键结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定是一种重要的定量实验方法:
I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
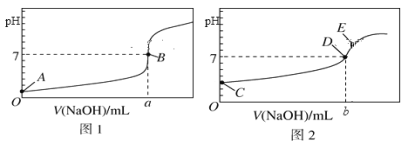
(1)滴定盐酸的曲线是图__________(填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________(电离度=![]() ×100%)。
×100%)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________mol/L。
Ⅱ. 现使用酸碱中和滴定法测定市售白醋中醋酸的浓度
(1)实验步骤:
①量取10.00 mL市售白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀得待测白醋溶液。
②用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
③读取盛装0.1000 mol/L NaOH 溶液的碱式滴定管的初始读数。
④滴定。当___________________时,停止滴定,并记录NaOH溶液的最终读数。
⑤重复②、③、④步骤3次。
数据记录如下:
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(2)数据处理:
根据实验数据计算,可得市售白醋中醋酸的浓度为_________ mol/L
(3)误差在本实验的滴定过程中,下列操作会使实验结果偏大的是_________。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前平视读数,滴定后俯视读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com