
【题目】滴定是一种重要的定量实验方法:
I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
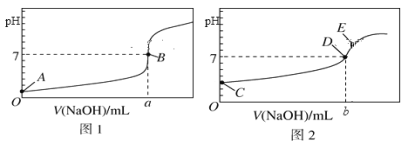
(1)滴定盐酸的曲线是图__________(填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________(电离度=![]() ×100%)。
×100%)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________mol/L。
Ⅱ. 现使用酸碱中和滴定法测定市售白醋中醋酸的浓度
(1)实验步骤:
①量取10.00 mL市售白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀得待测白醋溶液。
②用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
③读取盛装0.1000 mol/L NaOH 溶液的碱式滴定管的初始读数。
④滴定。当___________________时,停止滴定,并记录NaOH溶液的最终读数。
⑤重复②、③、④步骤3次。
数据记录如下:
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(2)数据处理:
根据实验数据计算,可得市售白醋中醋酸的浓度为_________ mol/L
(3)误差在本实验的滴定过程中,下列操作会使实验结果偏大的是_________。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前平视读数,滴定后俯视读数
【答案】1 1% > 9.9×10-7 溶液由无色恰好变为浅红色,并在半分钟内不褪色 0.075 ab
【解析】
I.(1)等浓度的盐酸和醋酸溶液中pH:HCl<CH3COOH,根据未滴定NaOH溶液时A点和C点pH大小判断盐酸反应曲线;
(2)等浓度的盐酸和醋酸溶液中,盐酸是一元强酸、pH=1,则c(CH3COOH)=c(HCl)=0.1mol/L,结合电离度公式计算电离度;
(3)醋酸、盐酸、NaOH溶液的初始浓度相同,均为0.1000mol/L,盐酸与NaOH恰好反应时pH=7,a=20.00mL;醋酸与NaOH恰好反应时生成醋酸钠,溶液显碱性,要使溶液呈中性,则必须醋酸过量,即b<20.00mL;根据电荷关系计算;
II.(1)④用酚酞作指示剂,如溶液颜色突变且半分钟内不变色,可说明达到滴定终点;
(2)计算消耗标准液体积,求出其平均体积,依据c(待测)= 计算待测液浓度,根据醋酸的浓度计算出该市售白醋的含酸量;
计算待测液浓度,根据醋酸的浓度计算出该市售白醋的含酸量;
(3)根据c(待测)= 分析不当操作对V(标准)的影响,以此判断浓度的误差。
分析不当操作对V(标准)的影响,以此判断浓度的误差。
I.(1)醋酸是弱酸、部分电离,HCl是强酸,完全电离,所以等浓度的盐酸和醋酸的酸性:HCl>CH3COOH,等浓度的盐酸和醋酸溶液中pH:HCl<CH3COOH,由图可知,当V(NaOH)=0时,A点pH=1,C点pH=3,所以图1为滴定盐酸的曲线;
(2)盐酸和醋酸溶液浓度相等,盐酸是一元强酸、pH=1,则c(CH3COOH)=c(HCl)=0.1mol/L,C点pH=3,即0.1mol/L醋酸溶液中c(H+)=0.001mol/L,所以滴定前CH3COOH的电离度=![]() ×100%==1%;
×100%==1%;
(3)醋酸、盐酸、NaOH溶液的初始浓度均为0.1000mol/L,a=20.00mL时盐酸与NaOH恰好反应,醋酸与NaOH恰好反应时生成醋酸钠,溶液显碱性,要使溶液呈中性,则必须醋酸过量,即b<20.00mL,所以a>b;醋酸与NaOH反应的溶液中存在电荷守恒关系为:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(Na+)-c(CH3COO-)=c(OH-)-c(H+)=(10-6-10-8)mol/L=9.9×10-7mol/L;
Ⅱ.(1)④选择酚酞作指示剂,用NaOH标准溶液滴定CH3COOH时,开始溶液为无色,随着NaOH的滴入,溶液的酸性逐渐减弱,当滴入最后一滴氢氧化钠溶液时,溶液由无色恰好变成浅红色,且半分钟内不褪色说明滴定达到终点;
(2)四次消耗的标准液的体积中第一次数据误差大,舍去,所以消耗标准液平均体积为15.00mL,根据c(待测)= =0.075mol/L;
=0.075mol/L;
(3)a.碱式滴定管在滴定时未用标准NaOH溶液润洗,导致标准液浓度偏低、消耗标准液体积偏大,依据c(待测)= 分析可知,V(标准)偏大,使测定结果偏大,a符合题意;
分析可知,V(标准)偏大,使测定结果偏大,a符合题意;
b.碱式滴定管尖嘴部分有气泡,滴定后消失,导致消耗标准液体积偏大,依据c(待测)= 分析可知,V(标准)偏大,使测定结果偏大,b符合题意;
分析可知,V(标准)偏大,使测定结果偏大,b符合题意;
c.锥形瓶中加入待测白醋溶液后,再加入少量水,对消耗标准液体积不产生影响,依据c(待测)= 分析可知,对测定结果无影响,c不符合题意;
分析可知,对测定结果无影响,c不符合题意;
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出,导致消耗标准液体积偏小,依据c(待测)= 分析可知,V(标准)偏小,使测定结果偏低,d不符合题意;
分析可知,V(标准)偏小,使测定结果偏低,d不符合题意;
e.滴定前平视读数,滴定后俯视读数,导致消耗标准液体积偏小,依据c(待测)= 分析可知,V(标准)偏小,则测定结果偏低,e不符合题意;
分析可知,V(标准)偏小,则测定结果偏低,e不符合题意;
故合理选项是ab。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出___kJ热量。
(2)如图装置中仪器A的名称___,作用是___;仪器B的名称___,作用是___;碎泡沫塑料的作用是___。
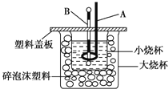
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是___。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得中和热的数值会___(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法正确的是
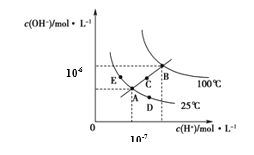
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到C点,可采用温度不变时在水中加入适量H2SO4 的方法
C.若从A点到D点,可采用在水中加入少量NaOH的方法
D.若处在B点温度时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温下气体反应达到化学平衡,平衡常数K=c(A)·c2(B)/[c2(E)·c(F)],恒容时,若温度适当降低,F的浓度增加,下列说法正确的是( )
A. 增大c(A)、c(B),K增大
B. 降低温度,正反应速率增大
C. 该反应的焓变为负值
D. 该反应的化学方程式为2E(g)+F(g)![]() A(g)+2B(g)
A(g)+2B(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A. 铝粉投入NaOH溶液中:2Al+2OH-===2AlO2-+H2↑
B. Na与CuSO4溶液反应:Cu2++2Na===2Na++Cu
C. 向AlCl3溶液中加入足量的氨水:Al3++3OH-===Al(OH)3↓
D. Ba(OH)2溶液与稀硫酸反应:Ba2++2OH-+2H++SO42-===BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 将pH均为a的NaOH溶液和氨水分别加水稀释100倍,pH分别变为b和c,则a、b、c的大小关系为b>c>a
B. 常温下0.1 molL-1 KHA溶液的pH=3,则该溶液中C(A2- )<c(H2A)
C. 室温时 M(OH)2(s)![]() M2+(aq)+2OH-(aq) Ksp=a,则当 c(M2+)=b molL-1 时,溶液的pH为14 +
M2+(aq)+2OH-(aq) Ksp=a,则当 c(M2+)=b molL-1 时,溶液的pH为14 +![]() 1g
1g![]()
D. 0.1 molL-1 Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法表达错误的是
A.中和滴定时盛待测液的锥形瓶中有少量水对滴定结果无影响
B.“NO2球”浸入冷水中颜色变浅:2NO2(g)(红棕色)![]() N2O4(g)(无色)ΔH<0
N2O4(g)(无色)ΔH<0
C.在酸碱中和滴定实验中,装标准液的滴定管若不润洗,则实验结果偏高
D.甲烷的燃烧热为ΔH=-890.3kJ·mol-1,则甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)==CO2(g)+2H2O(g)ΔH=-890.3kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是
A.室温下,测得氯化铵溶液pH<7,证明一水合氨是弱碱:![]() +2H2O=NH3·H2O+H3O+
+2H2O=NH3·H2O+H3O+
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH+2H2O=2![]() +3H2↑
+3H2↑
C.用碳酸氢钠溶液检验水杨酸中的羧基: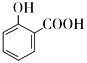 +2
+2![]() →
→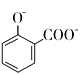 +2H2O+2CO2↑
+2H2O+2CO2↑
D.用高锰酸钾标准溶液滴定草酸:2![]() +16H++5
+16H++5![]() =2Mn2++10CO2↑+8H2O
=2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用手持技术探究氢氧化铝制备实验电导率(电导率越大表示导电能力越强)的变化,浓度均为0.5 mol·L-1 的氢氧化钠和氨水分别滴定0.01 mol·L-1硫酸铝溶液,电导率变化曲线如图所示,下列说法错误的是
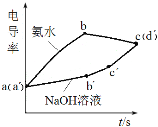
A.a(a)点溶液pH<7
B.bc段电导率下降是因为生成了Al(OH)3沉淀
C.ab段和bc段使用碱的体积比约为3:1
D.b点溶液:c(H+)<2c(SO42-)+c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com