
【题目】镁铝碱式碳酸盐MgaAlb(OH)c(CO3)d·xH2O是一种不溶于水的新型无机阻燃剂,其受热分解产物中的MgO、Al2O3熔点较高且都不燃烧,有阻燃作用。
完成下列填空:
(1).组成镁铝碱式碳酸盐的三种非金属元素的原子半径从小到大的顺序是______________。碳原子最外层电子排布式是_______________________________,铝原子核外有_________种能量不同的电子。
(2).将MgaAlb(OH)c (CO3)d·x H2O表示成氧化物的形式:2aMgO·bAl2O3·2dCO2·((______))H2O;焦炭与石英高温下在氮气流中发生如下反应,工业上可由此制得一种新型陶瓷材料氮化硅(Si3N4) :3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g) + Q (Q>0)
Si3N4(s)+6CO(g) + Q (Q>0)
(3).该反应中,氧化产物是________________________。若测得反应生成4.48 L CO气体(标准状况下),则转移的电子的物质的量为_____________。
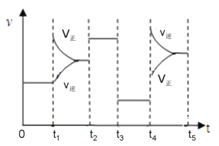
(4).该反应的平衡常数表达式K=_____________________________;若升高温度,K值____________(填“增大”、“减小”或“不变”)。该反应的速率与反应时间的关系如图所示,t4时刻引起正逆速率变化的原因是___________________________(写出一种即可)。
【答案】 H<O<C 2s22P2 5 (2x+c) 一氧化碳 0.4mol [c(CO)]6/[c(N2)]2 减小 升高温度(加压、缩小容器体积等)
【解析】(1)组成镁铝碱式碳酸盐的三种非金属元素为C、H、O,H原子半径最小,同一周期,从左到右,原子半径逐渐减小,因此原子半径从小到大的顺序为H<O<C;C为6号元素,碳原子最外层电子排布式是2s22p2;Al核电荷数为13,具有3个电子层,最外层电子数为3,核外电子排布式为:1s22s22p63s23p1,具有1s、2s、2p、3s、3p共5种能量不同的电子,故答案为:H<O<C;2s22p2;5。
(2)MgaAlb(OH)c(CO3)dxH2O写出氧化物形式为:aMgO![]() Al2O3dCO2
Al2O3dCO2![]() H2O或2aMgObAl2O32dCO2(c+2x)H2O,故答案为:c+2x。
H2O或2aMgObAl2O32dCO2(c+2x)H2O,故答案为:c+2x。
(3)根据方程式3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g),反应中C元素化合价升高,被氧化,氧化产物为CO;生成6molCO时,转移电子的物质的量是12mol,当生成4.48L(即0.2mol)CO气体(标准状况下),转移电子0.4mol,故答案为:一氧化碳;0.4mol。
Si3N4(s)+6CO(g),反应中C元素化合价升高,被氧化,氧化产物为CO;生成6molCO时,转移电子的物质的量是12mol,当生成4.48L(即0.2mol)CO气体(标准状况下),转移电子0.4mol,故答案为:一氧化碳;0.4mol。
(4)3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g) + Q (Q>0),该反应的平衡常数表达式K=
Si3N4(s)+6CO(g) + Q (Q>0),该反应的平衡常数表达式K=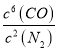 ;正反应为放热反应,升高温度,平衡逆向移动,K值减小。根据反应的速率与反应时间的关系图可知,t 4时刻逆反应速率和正反应速率均增大,但逆反应反应速率大于正反应速率,平衡逆向移动,说明改变的条件为升高温度,故答案为:
;正反应为放热反应,升高温度,平衡逆向移动,K值减小。根据反应的速率与反应时间的关系图可知,t 4时刻逆反应速率和正反应速率均增大,但逆反应反应速率大于正反应速率,平衡逆向移动,说明改变的条件为升高温度,故答案为: 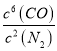 ;减小;升高温度。
;减小;升高温度。


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:

(1)写出上述实验过程中所用试剂(写化学式):
试剂②_____________________;试剂③_____________________。
(2)判断试剂①已过量的方法是:___________________________________。
(3)用离子方程式表示加入试剂②的作用:________________________
(4)操作①是利用半透膜进行分离提纯。
操作①的实验结果:淀粉_________(填“能”或“不能”)透过半透膜;SO42-__________(填“能”或“不能”)透过半透膜;
请用实验证明上述结果,完成下表(可不填满,也可增加)______:
限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸
编号 | 实验操作 | 预期现象和结论 |
① | ||
② |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期元素,其原子半径、化合价等信息见下表。

有关这四种元素的说法一定正确的是
A. X与W形成的化合物的电子式可表示为![]()
B. Y的氢化物能与W的氢化物反应,所得产物只含有共价键
C. X、Y能分别与氧元素形成多种氧化物
D. Z处于元素周期表中第三周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖.他的操作如下:取少量纯蔗糖加水配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟、冷却;在冷却后的溶液中加入银氨,在水浴中加热.实验结果没有银镜产生.其原因是( )
A.蔗糖尚未水解
B.蔗糖水解的产物中没有葡萄糖
C.加热时间不够
D.煮沸后的溶液中没有加碱,以中和作催化剂的酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是( )
A.BF3是三角锥形分子
B.NH![]() 的电子式:
的电子式: ,离子呈平面形结构
,离子呈平面形结构
C.CH4分子中的4个C﹣H键都是氢原子的1s轨道与碳原子的p轨道形成的s﹣p σ键
D.CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个s﹣sp3σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,

请参照元素A~H在表中的位置,用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为_______________________________。
(2)B、C、D的第一电离能由大到小的顺序为_____________________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________________。
(4)E、F的最高价氧化物的水化物相互反应的离子方程式:__________________。
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有______________;与CO分子互为等电子体的分子和离子分别为________和________,根据等电子理论推测CO分子的结构式可表示成________,一个CO分子中有________个σ键,________个π键。
(6)根据价电子对互斥理论预测D和H所形成的HD的空间构型为_________形。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子化合物G的一种合成路线如下:

已知:①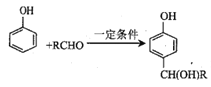 ;
;
②D溶液显酸性
③浓硫酸能与酚类物质发生取代反应,在苯环上引入-SO2H
回答下列问题:
(1)E分子中的含氧官能团名称为____________________________。
(2)下列关于化合物B的说法不正确的是______________ (填标号)。
①苯环上一氯代物有2种
②分子式为C8H10O2
③既能与FeCl3溶液发生显色反应又能与溴水发生加成反应
④1mol化合物B与足量金属钠反应生成标准状况下氢气22.4L
(3)A→B的反应类型是______________,D→E的目的是____________________________,F的化学名称为____________________________。
(4)写出F→G的化学方程式__________________________________________。
(5)某烃的含氧衍生物X符合下列条件的同分异构体有种______________ (不含立体异构)。
①氧原子数与B相同但相对分子质量比B少36
②能发生水解反应
其中核磁共振氢谱只有2组峰的是__________________________ (写结构简式)
(6)写出用苯酚、![]() 为原料(其他无机试剂任选)制备化合物
为原料(其他无机试剂任选)制备化合物![]() 的合成路线。____________________
的合成路线。____________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com