
【题目】下表为元素周期表的一部分,

请参照元素A~H在表中的位置,用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为_______________________________。
(2)B、C、D的第一电离能由大到小的顺序为_____________________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________________。
(4)E、F的最高价氧化物的水化物相互反应的离子方程式:__________________。
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有______________;与CO分子互为等电子体的分子和离子分别为________和________,根据等电子理论推测CO分子的结构式可表示成________,一个CO分子中有________个σ键,________个π键。
(6)根据价电子对互斥理论预测D和H所形成的HD的空间构型为_________形。
【答案】 Na>Al>O N>O>C ![]() Al(OH)3+OH-===[Al(OH)4]- CH4、CH3OH N2 CN—(或C
Al(OH)3+OH-===[Al(OH)4]- CH4、CH3OH N2 CN—(或C![]() 或NO+) C≡O 1 2 正四面体
或NO+) C≡O 1 2 正四面体
【解析】根据元素在周期表中的位置可知,A、B、C、D、E、F、G、H分别为H、C、N、O、Na、Al、Si、Cl。
(1) 同周期从左到右,原子半径逐渐减小,同主族,从上到下,原子半径逐渐增大,
D、E、F的原子半径由大到小的顺序为Na>Al>O,故答案为:Na>Al>O;
(2) 同一周期元素中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第IIA族、第VA族元素的第一电离能大于相邻元素。B、C、D的第一电离能由大到小的顺序为N>O>C,故答案为:N>O>C;
(3) H、O、Na、Cl中的某些元素可形成既含离子键又含极性共价键的化合物,如氢氧化钠,次氯酸钠等,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(4)氢氧化钠和氢氧化铝反应的离子方程式为Al(OH)3 + OH-== AlO2- +2H2O,故答案为:Al(OH)3 + OH-== AlO2- +2H2O;
(5)化合物CH4为正四面体结构,采取sp3杂化;CO为直线结构,采取sp杂化;CH3OH可以看出甲烷中的氢原子被羟基取代的产物,碳原子采取sp3杂化;与CO分子互为等电子体的分子和离子分别为N2、CN—或C22-;根据等电子理论推测CO分子的结构与氮气相似,结构式为C≡O;一个CO分子中有1个σ键,2个π键,故答案为:CH4、CH3OH;N2、CN—或C22-;C≡O;1;2;
(6)ClO4-中Cl的价层电子对数=4+![]() ×(7+1-4×2)=4,采取sp3杂化,空间构型为正四面体形,故答案为:正四面体。
×(7+1-4×2)=4,采取sp3杂化,空间构型为正四面体形,故答案为:正四面体。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】下列关于化石燃料的加工说法正确的是( )
A.煤干馏主要得到焦炭、煤焦油、粗氨水和焦炉气
B.石油裂化主要得到乙烯
C.石油分馏是化学变化,可得到汽油、煤油
D.煤的气化是在高温下煤和水蒸气作用转化为可燃性气体的过程,属于物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝碱式碳酸盐MgaAlb(OH)c(CO3)d·xH2O是一种不溶于水的新型无机阻燃剂,其受热分解产物中的MgO、Al2O3熔点较高且都不燃烧,有阻燃作用。
完成下列填空:
(1).组成镁铝碱式碳酸盐的三种非金属元素的原子半径从小到大的顺序是______________。碳原子最外层电子排布式是_______________________________,铝原子核外有_________种能量不同的电子。
(2).将MgaAlb(OH)c (CO3)d·x H2O表示成氧化物的形式:2aMgO·bAl2O3·2dCO2·((______))H2O;焦炭与石英高温下在氮气流中发生如下反应,工业上可由此制得一种新型陶瓷材料氮化硅(Si3N4) :3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g) + Q (Q>0)
Si3N4(s)+6CO(g) + Q (Q>0)
(3).该反应中,氧化产物是________________________。若测得反应生成4.48 L CO气体(标准状况下),则转移的电子的物质的量为_____________。
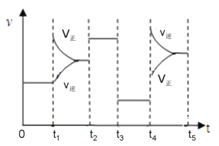
(4).该反应的平衡常数表达式K=_____________________________;若升高温度,K值____________(填“增大”、“减小”或“不变”)。该反应的速率与反应时间的关系如图所示,t4时刻引起正逆速率变化的原因是___________________________(写出一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20,其中C、E是金属元素;A和E属同一族,且A为非金属元素,它们原子的最外层电子排布为ns1,B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是________(写元素符号)。
(2)写出C元素基态原子的电子排布式__________________________________。
(3)用轨道表示式表示D元素原子的价电子排布__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关蒸馏的说法不正确的是
A.能将粗盐提纯B.能将四氯化碳和溴进行分离
C.操作时需加入几块沸石,以防暴沸D.部分蒸馏需要使用温度计便于控制温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气及其化合物在生产生活中有重要的应用。
(1)可用O2将HCl转化为Cl2:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。已知相关化学键的键能如下表所示
化学键 | H-Cl | O=O | Cl – Cl | H-O |
E(kJ·mol-1 | a | b | c | d |
则该反应的△H=______________。(用含a、b、c、d的代数式表示)
(2)氯气是有机合成中的重要试剂,丙烯(CH2=CHCH3)和Cl2在一定条件下发生如下反应: CH2=CHCH3 (g)+Cl2(g) ![]() CH2=CHCH2Cl(g)+HCl(g)。一定压强下,该反应在不同温度、不同投料比时,达平衡时Cl2的转化率如图所示(T12< T3)
CH2=CHCH2Cl(g)+HCl(g)。一定压强下,该反应在不同温度、不同投料比时,达平衡时Cl2的转化率如图所示(T12< T3)
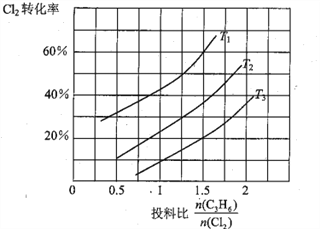
①该反应的△H______________0(填“>”或“<”)
②下列措施能增大丙烯的平衡转化率的是______________ (填标号)。
A.降低温度 B.减小容器的体积
C.使用新型催化剂 D.从容器中移走氯化氢
③T1时,在容积为5L的密闭容器中充入0.15mol丙烯和0.10 molCl2,10min时达到平衡,则v(Cl2)为______________mol·〔L·min)-1,平衡常数K为______________,保持温度不变,减小投料比![]() ,K值将______________ (填“增大”“减小”或“不变”);若起始时向该容器中充入0.30mol丙烯、0.20 molCl2、0.15 mol CH2=CHCH2Cl和0.30 molHCl,判断反应进行的方向并说明理由____________________________。
,K值将______________ (填“增大”“减小”或“不变”);若起始时向该容器中充入0.30mol丙烯、0.20 molCl2、0.15 mol CH2=CHCH2Cl和0.30 molHCl,判断反应进行的方向并说明理由____________________________。
④上述反应在低于某温度时,CH2=CHCH2Cl的产率快速下降,可能的原因是____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com