
【题目】下列反应属于吸热反应的是( )
A.甲烷在空气中燃烧
B.碳酸钙受热分解
C.镁条溶于盐酸
D.过氧化钠与水反应
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列四种X溶液,均能跟盐酸反应,其中反应最快的是( )
A.10℃20 mL 3mol/L的X溶液
B.20℃30 mL 2molL的X溶液
C.20℃10 mL 4mol/L的X溶液
D.10℃10 mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖.他的操作如下:取少量纯蔗糖加水配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟、冷却;在冷却后的溶液中加入银氨,在水浴中加热.实验结果没有银镜产生.其原因是( )
A.蔗糖尚未水解
B.蔗糖水解的产物中没有葡萄糖
C.加热时间不够
D.煮沸后的溶液中没有加碱,以中和作催化剂的酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,

请参照元素A~H在表中的位置,用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为_______________________________。
(2)B、C、D的第一电离能由大到小的顺序为_____________________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________________。
(4)E、F的最高价氧化物的水化物相互反应的离子方程式:__________________。
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有______________;与CO分子互为等电子体的分子和离子分别为________和________,根据等电子理论推测CO分子的结构式可表示成________,一个CO分子中有________个σ键,________个π键。
(6)根据价电子对互斥理论预测D和H所形成的HD的空间构型为_________形。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铁常用于检测硒、污水处理等。制备FeCl2的方法有多种。
(1)在一定量的盐酸中,逐渐加入一定量的铁屑,若二者恰好完全反应。再向溶液中加入_____________然后保存溶液。
(2)用H2还原无水FeCl3制取FeCl2,装置如下:
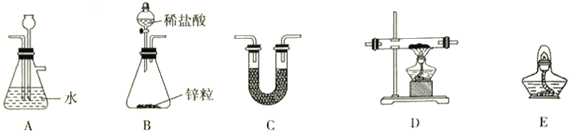
已知:FeCl2、FeCl3易吸水。
①H2还原无水FeCl3制取FeCl2的化学方程式为__________________________________。
②上述仪器的连接顺序为(可多次使用)______________,C中盛放的试剂是___________________。
(3)按下图装置,用162.5g无水氯化铁和225g氯苯,控制反应温度在一定范围加热3h。冷却,分离提纯得到粗产品。反应为2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl。
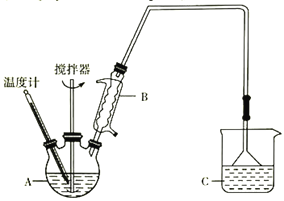
已知:
C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯 | ||
熔点/℃ | -45 | 53 | _________ | _________ |
沸点/℃ | 132 | 173 | _________ | _________ |
①仪器A的名称是____________;下列装置可以代替装置C的是_____________(填字母)。

②反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl中,氧化产物是_________________________。
③反应的温度最好控制在_______________左右。
④反应结束后,冷却实验装置,将仪器A 内物质经过过滤洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是_________________________。
⑤通过烧杯中的现象变化就可以监控氯化铁的转化率。若要监控氯化铁转化率达到或超过80%,则烧杯中试剂为加有酚酞且理论上至少含_______gNaOH的溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近全球多个国家爆发大规模流感,中药良好的预防和治疗作用再次进入科学家的视野。食用香料肉桂具有良好的预防作用,其有效成分之一肉桂酸结构简式如图所示。下列说法不正确的是
![]()
A. 肉桂酸的化学式为C9H8O2
B. 肉桂酸能发生加成反应、取代反应
C. 肉桂酸的结构中含有4个碳碳双键
D. 肉桂酸能使溴水、酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图表示的一些物质或概念间的从属关系中正确的是
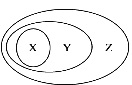
X | Y | Z | |
A | 水 | 单质 | 纯净物 |
B | 非金属氧化物 | 酸性氧化物 | 氧化物 |
C | 电解质 | 化合物 | 纯净物 |
D | 化合反应 | 氧化还原反应 | 化学反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,将2molCO与5molH2的混合气体充入容积为2L的密闭容器中,在催化剂的作用下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
(1)经过5min后,反应达到平衡,此时转移电子6mol。该反应的平衡常数为_______。V(H2)=_____mol/(L·min)。若保持体积不变,再充入2mulCO和1.5mol CH3OH,此时v(正)___ v(逆)(填“>”“<”或“=”)。
(2)在其他条件不变的情况下,再增加2molCO与5molH2,达到新平衡时,CO的转化率____(填“增大”“减小”或“不变”)。
(3)下列不能说明该反应已达到平衡状态的是__________
a.CH3OH的质量不变 b.混合气体的平均相对分子质量不再改变
c.V逆(CO)=2V正(H2) d.混合气体的密度不再发生改变
(4)在一定压强下,容积为VL的容器充入amolCO与2amolH2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
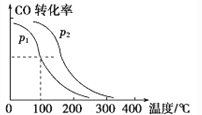
则p1_____p2(填“大于”“小于”或“等于”,下同),△H_____0。该反应在_______(填“高温”或“低温”)下能自发进行。
(5)能使该反应的反应速率增大,且平衡向正反应方向移动的是_____。
a.及时分离除CH3OH气体 b.适当升高温度
c.增大H2的浓度 d.选择高效催化剂
(6)下面四个选项是四位学生在学习化学反应速率与化学反应限度以后,联系化工生产实际所发表的看法,你认为不正确的是_______。
a.化学反应速率理论可指导怎样在一定时间内快出产品
b.有效碰撞理论可指导怎样提高原料的转化率
c.勒夏特列原理可指导怎样使用有限原料多出产品
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com