
【题目】下列有关蒸馏的说法不正确的是
A.能将粗盐提纯B.能将四氯化碳和溴进行分离
C.操作时需加入几块沸石,以防暴沸D.部分蒸馏需要使用温度计便于控制温度
科目:高中化学 来源: 题型:
【题目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:

(1)写出上述实验过程中所用试剂(写化学式):
试剂②_____________________;试剂③_____________________。
(2)判断试剂①已过量的方法是:___________________________________。
(3)用离子方程式表示加入试剂②的作用:________________________
(4)操作①是利用半透膜进行分离提纯。
操作①的实验结果:淀粉_________(填“能”或“不能”)透过半透膜;SO42-__________(填“能”或“不能”)透过半透膜;
请用实验证明上述结果,完成下表(可不填满,也可增加)______:
限选试剂:1mol/L AgNO3溶液、1mol/L BaCl2溶液、1mol/L Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸
编号 | 实验操作 | 预期现象和结论 |
① | ||
② |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推断正确的是( )
A.BF3是三角锥形分子
B.NH![]() 的电子式:
的电子式: ,离子呈平面形结构
,离子呈平面形结构
C.CH4分子中的4个C﹣H键都是氢原子的1s轨道与碳原子的p轨道形成的s﹣p σ键
D.CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个s﹣sp3σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,

请参照元素A~H在表中的位置,用化学用语回答下列问题:
(1)D、E、F的原子半径由大到小的顺序为_______________________________。
(2)B、C、D的第一电离能由大到小的顺序为_____________________________。
(3)A、D、E、H中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______________________。
(4)E、F的最高价氧化物的水化物相互反应的离子方程式:__________________。
(5)在B所形成的化合物CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有______________;与CO分子互为等电子体的分子和离子分别为________和________,根据等电子理论推测CO分子的结构式可表示成________,一个CO分子中有________个σ键,________个π键。
(6)根据价电子对互斥理论预测D和H所形成的HD的空间构型为_________形。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家制造出由4个氧原子构成的氧分子,并用质谱仪探测后证实了它的存在.若该氧分子具有空间对称结构,下列关于该氧分子的说法正确的是( )
A.是氧元素的一种同位素
B.是氧气的同素异形体,分子内含有共价键
C.是一种新的氧化物
D.是臭氧的同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近全球多个国家爆发大规模流感,中药良好的预防和治疗作用再次进入科学家的视野。食用香料肉桂具有良好的预防作用,其有效成分之一肉桂酸结构简式如图所示。下列说法不正确的是
![]()
A. 肉桂酸的化学式为C9H8O2
B. 肉桂酸能发生加成反应、取代反应
C. 肉桂酸的结构中含有4个碳碳双键
D. 肉桂酸能使溴水、酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高分子化合物G的一种合成路线如下:

已知:①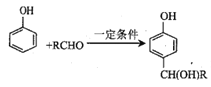 ;
;
②D溶液显酸性
③浓硫酸能与酚类物质发生取代反应,在苯环上引入-SO2H
回答下列问题:
(1)E分子中的含氧官能团名称为____________________________。
(2)下列关于化合物B的说法不正确的是______________ (填标号)。
①苯环上一氯代物有2种
②分子式为C8H10O2
③既能与FeCl3溶液发生显色反应又能与溴水发生加成反应
④1mol化合物B与足量金属钠反应生成标准状况下氢气22.4L
(3)A→B的反应类型是______________,D→E的目的是____________________________,F的化学名称为____________________________。
(4)写出F→G的化学方程式__________________________________________。
(5)某烃的含氧衍生物X符合下列条件的同分异构体有种______________ (不含立体异构)。
①氧原子数与B相同但相对分子质量比B少36
②能发生水解反应
其中核磁共振氢谱只有2组峰的是__________________________ (写结构简式)
(6)写出用苯酚、![]() 为原料(其他无机试剂任选)制备化合物
为原料(其他无机试剂任选)制备化合物![]() 的合成路线。____________________
的合成路线。____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化亚铁易被氧化,制取过程要隔绝空气。现用铁屑、稀硫酸、氢氧化钠溶液制备氢氧化亚铁并观察其颜色,改进装置如下:
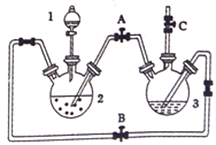
(1)稀硫酸应放在_____________(填写仪器名称)中。
(2)本实验通过关闭开关________、打开开关_________,将仪器中的空气排尽后,后续实验就可观察到氢氧化亚铁的颜色。试分析实验开始时排尽装置中空气的理由___________________。
(3)在FeSO4溶液中加入(NH4)2SO4固体可制备莫尔盐晶体[(NH4)2SO4·FeSO4·6H2O](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①为洗涤(NH4)2SO4·FeSO4·6H2O粗产品,下列方法中最合适的是___________
a.用冷水洗 b.先用冷水洗,后用无水乙醇洗
c.用30%的乙醇溶液洗 d.用90%的乙醇溶液洗
②为了测定产品的纯度,称取ag产品溶于水,配制成500mL溶液。每次取待测液20.00mL,用浓度为bmol/L的酸性KMnO4溶液滴定,实验结果记录如下:
实验次数 | 第一次 | 第二次 | 第三次 |
消耗酸性高锰酸钾溶液体积/mL | 20.02 | 19.98 | 20.52 |
滴定过程中发生反应的离子方程式为______________。滴定终点的现象是__________________________。通过实验数据计算的该产品纯度为_____________(用字母a、b表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com