
【题目】NaBH4是一种常见的还原剂。一种以H2、Na、硼酸三甲酯[B(OCH3)3]为原料,生产NaBH4的工艺流程如下:
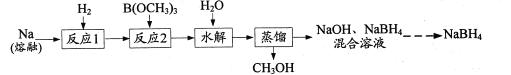
(1)下列措施能提高“反应1”的化学反应速率的有______(填字母)。
A.充分搅拌熔融钠
B.将熔融钠充分分散在石蜡油中
C.反应前排尽装置中的空气
(2)在浓硫酸作用下,B(OCH3)3可由B(OH)3和CH3OH发生酯化反应制得。浓H2SO4的作用是_____。
(3)“反应2”在240℃条件下进行,生成的产物是NaBH4和CH3ONa,写出该反应的化学方程式:____ 。“反应2”所用B(OCH3)3需充分干燥,原因是______。
(4)反应NaBH4+2H2O=NaBO2+4H2 可用于制取H2。一定浓度的NaBH4催化制氢的半衰期(溶液中NaBH4消耗一半时所需的时间)与溶液pH的关系如图所示:
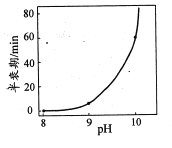
①NaBH4与水反应所得溶液呈碱性,原因是____。
②随着反应的进行,生成H2的速率逐渐减慢,原因是_______。
【答案】AB 催化剂、吸水剂 ![]() 防止NaH与水发生反应 NaBO2水解,使溶液呈碱性 反应物的浓度逐渐减小,溶液的碱性逐渐增大
防止NaH与水发生反应 NaBO2水解,使溶液呈碱性 反应物的浓度逐渐减小,溶液的碱性逐渐增大
【解析】
由工艺流程可知,Na和H2反应生成NaH,NaH和![]() 反应生成
反应生成![]() 和
和![]() ,
,![]() 水解得到NaOH和
水解得到NaOH和![]() ,蒸馏分离
,蒸馏分离![]() ,以此分析。
,以此分析。
(1)提高化学反应速率的方法有增加反应物浓度,升高温度,增加接触面积等,
A.充分搅拌熔融钠,增大接触面积,可以提高化学反应速率,故A正确;
B.将熔融钠充分分散在石蜡油中,增大接触面积,可以提高化学反应速率,故B确;
C. 反应前排尽装置中的空气,防止氢气不存发生爆炸,与化学反应速率无关,故C错误;
故答案选:AB。
(2)浓硫酸在反应中起到催化剂的作用,还能吸收生成的水分,使平衡正移;
故答案为:催化剂、吸水剂
(3)NaH和![]() 在240℃反应生成
在240℃反应生成![]() 和
和![]() ,则化学方程式为:
,则化学方程式为:![]() ,NaH易与水反应,因此为防止NaH与水发生反应“反应2”所用B(OCH3)3需充分干燥;
,NaH易与水反应,因此为防止NaH与水发生反应“反应2”所用B(OCH3)3需充分干燥;
故答案为:![]() ;防止NaH与水发生反应;
;防止NaH与水发生反应;
(4)HBO2为弱酸NaBO2水解呈碱性,NaBH4与水反应生成NaBO2溶液呈碱性,
故答案为:NaBO2水解,使溶液呈碱性;
(5)由图像可知pH越大,半衰期越长,则反应越慢,随着反应的进行,反应物浓度减小,反应速率降低,
故答案为:反应物的浓度逐渐减小,溶液的碱性逐渐增大。


科目:高中化学 来源: 题型:
【题目】全钒液流电池是一种新型储能电池,具有充放电可逆性高、能量转化效率高等优点,其结构如图所示,放电时电极a发生氧化反应。下列说法错误的是
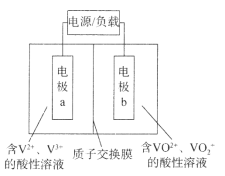
A.充电时电极a应连接电源的负极
B.放电时电极b发生的反应为![]() +e-+2H+=VO2++H2O
+e-+2H+=VO2++H2O
C.放电时电极a附近溶液pH不发生变化
D.充电时H+从质子交换膜右侧向左侧移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列离子晶体立体构型示意图如下图所示。


(1)以M代表阳离子,以N代表阴离子,写出各离子晶体的组成表达式。
A.__________,B:________,C:________,D:__________________________。
(2)已知FeS2晶体(黄铁矿的主要成分)具有A的立体结构。
①FeS2晶体中具有的化学键类型是__________________________________________。
②若晶体结构A中相邻的阴、阳离子间的距离为acm,且用NA代表阿伏加德罗常数,则FeS2晶体的密度是________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)上海白龙港污水处理厂升级改造,处理废水时加入明矾可作为混凝剂以吸附水中的杂质,利用漂白粉可用来杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学反应方程式是___________,其中___________是漂白粉的有效成分;
(2)生产硅酸盐水泥和普通玻璃都需要用到的主要原料是__________(填名称);
(3)在雷电作用下,大气中游离态的氮会少量转化为化合态的氮并随雨水落下,这是自然中固定氮的途径之一。用化学方程式表示上述过程。________,_______,______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.H2SiO3![]() SiO2
SiO2 ![]() SiCl4
SiCl4
B.Cu![]() Cu(NO3)2(aq)
Cu(NO3)2(aq) ![]() Cu(NO3)2(s)
Cu(NO3)2(s)
C.ClCH2-CH2Cl![]() HOCH2-CH2OH
HOCH2-CH2OH ![]() HOOC-COOH
HOOC-COOH
D.Al![]() Al2O3
Al2O3![]() NaAlO2(aq)
NaAlO2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以含银废液{主要含[Ag(NH3)2]+、[Ag(S2O3)2]3-}为原料制取硝酸银晶体,其实验流程如下:

已知:①“沉银”所得AgCl中含有少量PbCl2、Ag2S。
②Zn2+在浓氨水中以[Zn(NH3)4]2+形式存在。
③PbCl2、AgNO3的溶解度曲线如图所示:

(1)“滤液”中的主要阳离子为___(填化学式)。
(2)“除杂”分为两步:先除去PbCl2,再除去Ag2S。
①在不同温度下,AgCl、Ag2S均难溶于水。 除去PbCl2的操作为______,热水洗涤。
②向热水洗涤所得固体中加入浓硝酸和稀盐酸,边加热边充分搅拌,使Ag2S转变为AgCl。加入浓硝酸的目的是_______。
(3)室温下,可逆反应AgCl+2NH3·H2O[Ag(NH3)2]++Cl-+2H2O的平衡常数K=___。{Ksp(AgCl)= 1.8×10-10,Ag++2NH3·H2O[Ag(NH3)2]++2H2O的平衡常数为1.1×107}
(4)“还原”过程中发生反应的离子方程式为_____ 。
(5)粗银经水洗后,经多步处理可制备硝酸银晶体。请补充完整由以水洗后粗银为原料,制备硝酸银晶体的实验方案:________,过滤,________,将产生的气体和空气混合后通入NaOH溶液进行尾气处理,将所得AgNO3溶液_______,过滤,将所得晶体置于烘箱 (120℃)干燥,密封包装。(实验中须使用的试剂:稀硫酸、稀硝酸、BaC12溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积2L的密闭容器中加入反应物N2、H2,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
2NH3(g)。反应过程中的部分数据如下表所示,下列说法正确的是
物质的量/ mol 时间/min | n(N2) | n(H2) | n(NH3) |
0 | 1.0 | 1.2 | 0 |
2 | 0.9 | ||
4 | 0.75 | ||
6 | 0.3 |
A. 0~2 min内,NH3的反应速率为0.1 mol·Lˉ1·minˉ1
B. 2 min时, H2的物质的量0.3 mol
C. 4 min时,反应已达到平衡状态,此时正、逆反应的速率都为0
D. 4~6 min内,容器内气体分子的总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、实验室里用乙醇和浓硫酸反应生成乙烯,乙烯再与溴反应制1,2 -二溴乙烷。在制备过程中部分乙醇被浓硫酸氧化,产生CO2、SO2,并进而与溴反应生成HBr等酸性气体。
(1)用下列仪器,以上述三种物质为原料制备1,2一二溴乙烷。如果气体流向为从左到右,正确的连接顺序是(短接口或橡皮管均已略去):B经A①插人A中,D接A②;A③接_______接_____接_____接______。
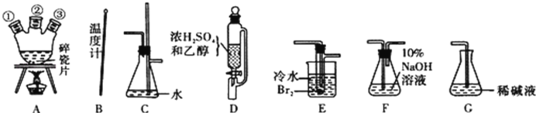
(2)装置C的作用是________________;
(3)在反应管E中进行的主要反应的化学方程式为____________________;
Ⅱ、某兴趣小组同学在实验室用加热l-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,设计了如下图所示的实验装置(其中的夹持仪器没有画出)。

请回答下列问题:
(1)两个装置中都用到了冷凝管,A装置中冷水从_________(填字母代号)进入,B装置中冷水从________(填字母代号)进入。
(2)制备操作中,加入的浓硫酸事先稍须进行稀释,其目的是________。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成 c.水是反应的催化剂
(3)为了进一步提纯1-溴丁烷,该小组同学查得相关有机物的有关数据如下表:
物质 | 熔点/℃ | 沸点/℃ |
1-丁醇 | -89.5 | 117.3 |
1-溴丁烷 | -112.4 | 101.6 |
丁醚 | -95.3 | 142.4 |
1-丁烯 | -185.3 | -6.5 |
则用B装置完成此提纯实验时,实验中要迅速升高温度至_________收集所得馏分。
(4)有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH2CH2CH3”,来确定副产物中是否存在丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)。请评价该同学设计的鉴定方案是否合理?________为什么?答:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮(N)、硝(P)、砷(As)等第VA族元素的化合物在研究和生产中有重要用途,请回答下列问题:
(1)基态砷原子的价电子排布图为________________,第三周期元素的原子中,第一电离能大于磷原子的有________________种。
(2)氮族元素氯化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的氢化物(RH3)性质可能有________________(填序号)。
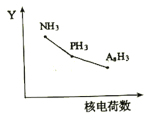
A.稳定性B.沸点时C.R-H键之间的键角D.分子间作用力E.还原性
(3)经测定发现,某种N2O5固体由NO2+和NO3-两种离子组成,阳离子中N原子的杂化方式是________________杂化,阴离子的空间构型为________________。
(4)乙二胺(H2N-CH2-CH2-NH2)与CuCl2溶液可形成配离子(结构如图)。
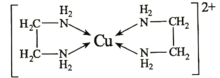
Cu2+的配位数为________________,1mol该配离子中含σ键为________________mol,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,其原因是________________。
(5)通常认为Cu3N是离子晶体,其晶格能可通过图1的Born-Haber循环计算得到。通过图1中数据________________(填“能”或“不能”)计算出Cu原子的第一电离能,Cu3N晶格能为________________kJ·mol-1。
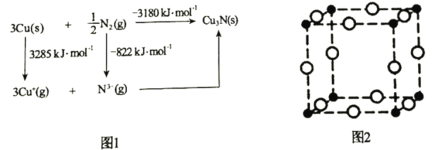
(6)Cu3N晶胞如图2所示,Cu+的半径为apm,N3-的半径为bpm,Cu3N晶胞的密度为________________g·cm-3(列出计算式即可,阿伏加德罗常数的值用NA表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com