
【题目】“垃圾是放错了位置的资源”,应该分类回收。其中塑料袋、废纸、旧橡胶制品属于
A. 无机物 B. 有机物 C. 盐 D. 非金属单质
 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
【题目】工业上用菱锰矿(MnCO3)[含FeCO3、SiO2、Cu2(OH)2CO3等杂质]为原料制取二氧化锰,其流程示意图如下: 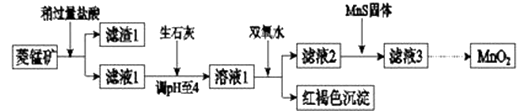
已知:生成氢氧化物沉淀的pH
Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
注:金属离子的起始浓度为0.1mol/L,回答下列问题:
(1)含杂质的菱锰矿使用前需将其粉碎,主要目的是 . 盐酸溶解MnCO3的化学方程式是 .
(2)向溶液1中加入双氧水时,反应的离子方程式是 .
(3)滤液2中加入稍过量的难溶电解质MnS,以除去Cu2+ , 反应的离子方程式是 .
(4)将MnCl2转化为MnO2的一种方法是氧化法.其具体做法是用酸化的NaClO3溶液将MnCl2氧化,该反应的离子方程式为:Mn2++ClO3﹣+=++ .
(5)将MnCl2转化为MnO2的另一种方法是电解法.
①阳极生成MnO2的电极反应式是 .
②若直接电解MnCl2溶液,生成MnO2的同时会产生少量Cl2 . 检验Cl2的操作是 .
③若在上述MnCl2溶液中加入一定量的Mn(NO3)2粉末,则无Cl2产生.其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出),请回答下列问题: 
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 , 反应④的化学方程式为 .
(2)若A是常见的变价金属的单质,D、F是气态单质,反应④可以在光照条件下发生.反应①和反应②在水溶液中进行,反应②的离子方程式是
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 . 标准状况下3.36L物质E与含氢氧化钠10.0g的溶液充分反应,所得溶液中溶质成分为(写出化学式和对应的物质的量).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取物质的量浓度相等的CuCl2、FeCl3的混合溶液40mL平分于两只试管,向其中一只试管加入足量AgNO3溶液生成14.35g 沉淀,向另一只试管加入1.12g 还原铁粉充分反应后该试管溶液中存在的金属阳离子及其物质的量浓度是( )
A.Fe2+ 2mol/L、Cu2+ 0.5mol/L
B.Fe2+ 1mol/L、Fe3+ 1mol/L
C.Fe2+ 0.5mol/L、Cu2+ 0.25mol/L
D.Fe2+ 1.5mol/L、Cu2+ 0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为: 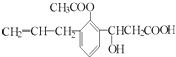 ,则此有机物可发生的反应类型有( )
,则此有机物可发生的反应类型有( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和.
A.①②④⑤⑥⑦⑧
B.②③④⑤⑥⑧
C.②③④⑤⑥⑦⑧
D.①②③④⑤⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:NH ![]() 、Ba2+、Na+、H+、SO
、Ba2+、Na+、H+、SO ![]() 、NO
、NO ![]() 、OH﹣、HCO
、OH﹣、HCO ![]() .将这四种溶液分别标记为A、B、C、D,进行如下实验: ①C溶液滴入另外三种溶液中,均无明显现象;
.将这四种溶液分别标记为A、B、C、D,进行如下实验: ①C溶液滴入另外三种溶液中,均无明显现象;
②D和B反应生成的气体能被A吸收;
③A和D反应生成的气体能被B吸收.
试回答下列问题:
(1)D的化学式是 , 判断理由是 .
(2)写出其余几种物质的化学式:A , B , C .
(3)写出实验②中有关反应的离子方程式 .
(4)写出实验③中有关反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用化学知识回答下列问题:
(1)R原子的3p轨道上只有一个未成对电子,则R原子可能是、;(填元素符号)Y原子的核电荷数为33,其外围电子排布是 , 其在元素周期表中的位置是 , 是属于区的元素.
(2)H2O分子内的O﹣H键、分子间的范德华力和氢键从强到弱依次为 .
(3)与CO分子互为等电子体的分子和离子分别为和(填化学式).
(4)![]() 的沸点比
的沸点比 ![]() 高,原因是 .
高,原因是 .
(5)H+可与H2O形成H3O+ , H3O+中O原子采用杂化,H3O+的空间构型是 . H3O+中H﹣O﹣H键角比H2O中H﹣O﹣H键角大,原因为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com