
【题目】直接乙醇燃料电池(DEFC) 具有无毒、来源丰富等优点,其装置如下图所示。装置工作时,下列说法错误的是
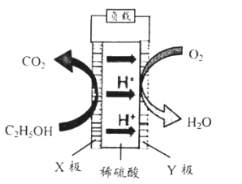
A.化学能转化为电能B.稀硫酸为该电池的电解质溶液
C.电子由Y极流出经负载流向X极D.电池反应为C2H5OH+ 3O2→2CO2+ 3H2O
【答案】C
【解析】
乙醇燃料电池,O2在酸性介质中生成H2O,化合价降低,Y极做原电池的正极,电极反应式:O2+4H++4e-=2H2O;乙醇转化成CO2,化合价升高,X极做负极,电极反应式:C2H5OH+3H2O-12e-=2CO2+12H+,电池总反应为:C2H5OH+ 3O2→2CO2+ 3H2O。
A.原电池是化学能转化成电能的装置,A正确;
B.该电池的电解质溶液为酸性,可为稀硫酸,B正确;
C.由分析可知,Y是原电池正极,X是负极,电子从负极流出,流向正极,故电子由X极流出经负载流向Y极,C错误;
D.电池总反应为:C2H5OH+ 3O2→2CO2+ 3H2O,D正确;
答案选C。


 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】依据事实,回答下列问题。
(1)在 25℃、101 kPa 时,1.0 g C8H18(l,辛烷)燃烧生成CO2(g)和H2O(l),放出48.40kJ的热量,则C8H18(l)的燃烧热为_____kJ/mol
(2)已知N2(g)+2O2(g)=2NO2(g) ΔH=+67.7kJ/mol,N2H4(g)+O2(g)= N2(g)+2H2O (g) ΔH=-534kJ/mol,根据盖斯定律写出肼(N2H4)与 NO2完全反应生成氮气和气态水的热化学方程式____________。
(3)某反应过程中的能量变化如图所示,则该反应是___________反应(填“放热”或“吸热”),判断依据是____________________。

(4)已知:2NH3 (g)+3Cl2(g) =N2 (g) +6HCl(g) ΔH=–462 kJmol-1
N2(g)![]() 2N(g)
2N(g)
Cl2(g)![]() 2Cl(g)
2Cl(g)
则断开1 mol H–N键与断开1 mol H-Cl键所需能量相差约为_____kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化碱法是工业上制备Na2S2O3的方法之一,反应原理:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(该反应ΔH>0),某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O流程如下:

(1)吸硫装置如图所示:

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是____________,表明SO2吸收效率低的实验现象是B中_________。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是________、________。(写出两条)
(2)Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取ag KIO3(化学式量:214)固体配成溶液,加入过量KI固体和H2SO4溶液,滴加指示剂,用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为VmL。则c(Na2S2O3)=_________ mol·L-1。(只列出算式,不作运算)已知:![]() +I2=
+I2=![]() +2I-
+2I-
(3)某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的Na2S2O3浓度可能 ____(填“无影响”、“偏低”或“偏高”),原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是元素周期表中6种元素的相关信息,其中Q、W、X位于同一周期。
元素 | 信息 |
Q | 单质是稳定的半导体材料,用于制造芯片 |
W | 最高化合价为+7价 |
X | 最高价氧化物对应的水化物在本周期中碱性最强 |
Y | 焰色反应为紫色(透过蓝色钴玻璃片) |
Z | 地壳中含量最高的金属元素,其合金可用于制造飞机外壳 |
M | 原子结构示意图为 |
(1)Q元素所在周期表的位置为_____。
(2)W单质的电子式为_____。
(3)Z的单质与X的最高价氧化物对应的水化物反应的离子方程式为_____。
(4)Y的金属性强于X,请结合原子结构解释其原因_____。
(5)下列对于M及其化合物的推断中,正确的是_____(填序号)。
①M的最低负化合价与W的最低负化合价相同
②M的氢化物的稳定性弱于W的氢化物的稳定性
③M的单质可与X和W形成的化合物的水溶液发生置换反应
(6)与M位于同一主族,电子层数比M多一层的元素在生活中的用途是_____(写出一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钾(K)资源丰富,成本低廉,用其制作的钾离子电池有着超越锂离子电池的发展前景。我国科研人员在钾离子电池的研发上做出了巨大的贡献。如图是我国某科研团队研制的一种钾离子电池充电时的示意图,下列说法不正确的是( )

A.放电时,外电路电子由电极a流向电极b
B.钾离子电池电解液一般选择有机溶剂,但会有一定的安全隐患
C.充电时,每当外电路中转移1mole-,正极材料会“释放”39gK+
D.充电时,电极b上的电极反应式为:WS2+xK++xe-=KxWS2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是( )
A. 100 mL 1 mol·L-1FeCl3溶液中所含Fe3+的数目为0.1NA
B. 常温常压下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
C. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
D. 标准状况下,124 g P4中所含P—P键数目为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应 A(g)+3B(s)2C(g)+2D(g),在不同条件下的化学反应速率如下,其中表示的反应速率最快的是( )
A.v(A)=0.5mol·L-1·min-1B.v(B)=1.0 mol·L-1·min-1
C.v(D)=0.4 mol·L-1·min-1D.v(C)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种用电催化N2还原法制取NH3的反应机理如图所示,其中*表示吸附在催化剂表面的物种。下列说法正确的是
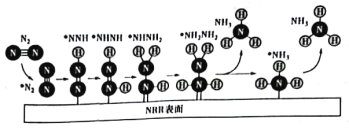
A.两个氮原子上的加氢过程是分步进行的
B.析氢反应(H++ H+→H2)不会影响NH3的合成
C.NH3从催化剂表而脱附不利于NH3的合成
D.电催化法是一步即能把N2还原为NH3的高效还原法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应可获得新型能源二甲醚(![]() )。下列说法不正确的是
)。下列说法不正确的是
①![]()
![]()
②![]()
![]()
③![]()
![]()
④![]()
![]()
A. 反应①、②为反应③提供原料气
B. 反应③也是![]() 资源化利用的方法之一
资源化利用的方法之一
C. 反应![]() 的
的![]()
D. 反应![]() 的
的![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com