
| A. | ①③④⑤ | B. | ③⑤⑥ | C. | ①②④⑦ | D. | ②⑤⑥⑦ |
分析 ①离子一定带电,质子数一定不等于电子数,而分子呈电中性,质子数一定等于电子数;
②同种元素可以形成不同的物质,组成混合物的元素也可能只有一种元素;
③二氧化硅属于酸性氧化物,不能与水反应,二氧化氮与水反应生成硝酸,但二氧化氮不属于酸性氧化物;
④煤的气化和液化均属化学变化;
⑤酸性氧化物可能为金属氧化物,如Mn2O7等,
⑥只含一种元素的物质属于单质,不可能发生化学变化;
⑦氯化钙的潮解属物理变化.
解答 解:①离子一定带电,质子数一定不等于电子数,而分子呈电中性,质子数一定等于电子数,所以质子数和电子数均相同的两种微粒不可能是一种分子和一种离子,故①错误;
②同种元素可以形成不同的物质,组成混合物的元素也可能只有一种元素,如金刚石与石墨,氧气和臭氧,故②错误;
③二氧化硅属于酸性氧化物,不能与水反应,二氧化氮与水反应生成硝酸,但二氧化氮不属于酸性氧化物,故③正确;
④水的汽化、液化属于物理变化,但煤的气化和液化均属化学变化,故④错误;
⑤碱性氧化物一定是金属氧化物,但酸性氧化物可能为金属氧化物,如Mn2O7等,故⑤正确;
⑥只含一种元素的物质属于单质,不可能发生化学变化,故⑥正确;
⑦Na2CO3•10H2O的风化失去结晶水,属于化学变化,但氯化钙的潮解属物理变化,故⑦错误,
故选:B.
点评 本题考查基本概念,需要学生熟练掌握基础知识,注意利用列举法与反例法解答,难度不大.


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X的某种单质是一种新型自来水消毒剂 | |
| B. | 简单离子半径:W->R2->X2->S3+ | |
| C. | R、Z不可能形成离子化合物 | |
| D. | 字母所代表的元素中最高价氧化物的水化物酸性最强的是Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验时酸或碱溅到眼中,应立即用水冲洗,并不断眨眼,不能用手搓揉眼睛 | |
| B. | 检验硫酸亚铁铵溶液中Fe2+的方法是:先滴加新制氨水后滴加KSCN溶液 | |
| C. | 证明钢铁吸收氧腐蚀的方法是:在镀锌铁皮上滴1~3滴含酚酞的饱和食盐水,静置1~2min,观察现象 | |
| D. | 用新制氢氧化铜悬浊液不能鉴别乙醇溶液和葡萄糖溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 实验目的 | 方法及操作 |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 鉴别二甲醚和乙醇 | 利用质谱法 |
| ③ | 检验乙醇在浓硫酸催化下的消去产物 | 将产物通入酸性KMnO4溶液 |
| ④ | 检验溴乙烷中的溴元素 | 将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,再滴加AgNO3溶液 |
| ⑤ | 鉴别苯、四氯化碳、丙醛 | 分别滴加溴水 |
| A. | ①⑤ | B. | ②③ | C. | ①④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1Na2C2O4溶液与0.1 mol•L-1HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)+c(Cl-)=c(Na+)+c(H+). |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 第一电离能 | 氧化性 | 沸点 | 非金属性 |
| N>S | Fe3+>Al3+ | NH3<H2O | 16O=18O |
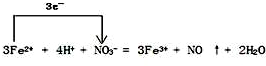 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇分子中的官能团是酚羟基 | |
| B. | 使用K2Cr2O7酸性溶液检测酒驾,是利用了乙醇的氧化性 | |
| C. | 乙醇可以发生取代、消去和氧化反应 | |
| D. | 将75%的乙醇与98%的浓硫酸混合液迅速加热至170°C以制取乙烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com