
【题目】已知丁基有4种,据此不必试写,即可判定C5H10O的醛应有( )
A. 3种 B. 4种 C. 5种 D. 6种
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
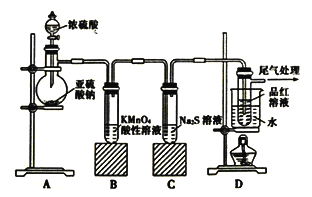
请回答下列问题:
(1)实验过程中,装置B中的现象是________________,原因是(用离子方程式表示)_____________。
(2)实验过程中,装置C中现象说明SO2具有的性质是_____________________。
(3)装置D中品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,可观察到的现象为__________。
(4)是否能将分液漏斗中的浓H2SO4换作浓HNO3,理由是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积相同的三个密闭容器中,加入一定量的物质发生反应,相关数据如下:
CO2(g)+H2(g)△H=﹣41kJ/mol,相同温度下,在体积相同的三个密闭容器中,加入一定量的物质发生反应,相关数据如下:
容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||||
CO | H2O | CO2 | H2 | Ar[ | ||
① | 1 | 4 | 0 | 0 | 0 | 放出热量:32.8 kJ |
② | 0 | 3 | 1 | 1 | 0 | 热量变化:Q1 |
③ | 0.5 | 3.5 | 0.5 | 0.5 | 1 | 热量变化:Q2 |
下列说法中,不正确的是( )
A.容器①中反应达平衡时,CO的转化率为80%
B.热量数值:Q2 < Q1 =32.8 kJ
C.平衡时,三容器中CO2的浓度相等
D.容器③中反应开始时正反应的浓度商小于该反应平衡常数K
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2015北京理综化学】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11) ( )
A.该消毒液可用NaOH溶液吸收Cl2制备:Cl2 +2OH-=== Cl-+ ClO-+ H2O
B.该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C.该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2 ↑+ H2O
D.该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+ CH3COO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列有关对该溶液的判断不正确的是( )

A. 该溶液中肯定含有的离子是H+、NH4+、Al3+、SO42﹣
B. 肯定不含的阳离子是Mg2+、Fe3+
C. 要确定该溶液是否含有Na+,必须做焰色反应实验,看焰色是否为黄色
D. 该溶液中肯定含有的离子的物质的量之比为n(H+):n(NH4+):n(Al3+):n(SO42﹣)=2:3:1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,利用如图装置可实现有机物的储氢,下列有关说法正确的是( )
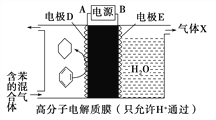
A. 苯在电极D放电时断开的化学键是极性键
B. 气体X在反应中通常体现还原性
C. 若阳极区的电解质溶液为稀硫酸,则电解一段时间后,阳极区溶液的pH增大
D. 电极D的电极反应式为C6H6+6H++6e-===C6H12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1molL-1的HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是( )
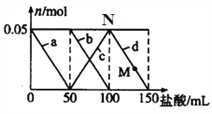
A. b和c曲线表示的是同一个离子反应
B. N点时生成的CO2为0.05mol
C. M点时Al(OH)3的质量等于3.9g
D. 原混合溶液中的CO32-与AlO2-的物质的量之比为1 :1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和铝是日常生活中用途广泛的金属。
I.(1)向NaAlO2溶液中滴加AlCl3溶液,生成白色胶状沉淀,则发生反应的离子方程式为_________________________。
(2)实验室常用还原性 Fe 粉与水蒸气反应的实验来研究 Fe 的还原性,则该反应的化学方程式为_________________________。
(3)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:__________________________。
II.已知合金A由两种常见金属组成。为测定其组成,某同学的实验流程如图所示:
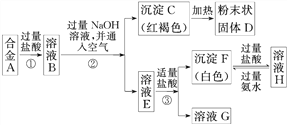
请回答:
(4)溶液E中所含的溶质是_________________(写化学式)
(5)合金A中的一种金属可以与粉末状固体D在高温下反应生成合金A中的另一种金属,请写出该反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为短周期内原子半径依次增大的元素,X、 Y、M、N分别由这四种元素中的两种组成的常见化合物,甲、 乙为其中两种元素对应的单质。若X与Y、甲与乙摩尔质量相同,Y与乙均为淡黄色固体,上述物质之间的转化关系如下图所示(部分反应物或生成物省略),则下列说法中不正确的是

A. 相对分子质量M>N,沸点N>M
B. 简单离子半径:C2—>B2—>D+>A+
C. A、C、D的常见氧化物相互之间一定能反应
D. D与其他元素均能形成离子化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com