
【题目】可逆反应A+3B![]() 2C+2D在4种不同条件下的反应速率(单位为mol·L-1·s-1)分别为①v(A)=0.15 ②v(B)=0.6 ③v(C)=0.4 ④v(D)=0.45该反应反应速率最快的条件是( )
2C+2D在4种不同条件下的反应速率(单位为mol·L-1·s-1)分别为①v(A)=0.15 ②v(B)=0.6 ③v(C)=0.4 ④v(D)=0.45该反应反应速率最快的条件是( )
A. ② B. ④ C. ①和④ D. ②和③
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】迷迭香酸是一种天然抗氧化剂,具有较强的抗氧化活性,能有效降低癌症和动脉硬化的风险。其结构简式为:
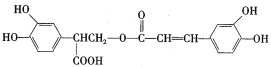
合成路线如下:
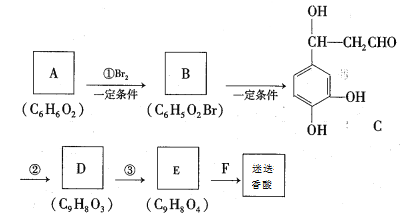
根据题意回答下列问题:
(1)A的结构简式为____________。
(2)①、②的反应类型分别是_____________、_____________。
(3)E的结构简式为__________________
(4)F在一定条件下发生缩聚反应的化学方程式为__________________________________
(5)写出一种与C互为同分异构体,且同时满足下列条件的有机的结构简式________________
①苯环上的一氯代物有2种
②1 mol该有机物能与1 molNaHCO3反应
③能与浓溴水反应,1 mol该有机物消耗3 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,在3支相同体积的试管中分别充有等体积混合的两种气体,它们是①NO和NO2,②NO2和O2,③NO和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3B.V1>V3>V2
C.V2>V3>V1D.V3>V1>V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时,醋酸溶液中存在下述关系:![]()
(1)当向该溶液中加入一定量盐酸时,上式中的数值是否发生变化_________ ?为什么_________?
(2)若醋酸的起始浓度为0.010 mol L-1,平衡时c(H+)是多少_________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。
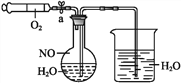
(1)打开止水夹,推动针筒活塞,使O2进入圆底烧瓶。关闭止水夹,首先观察到圆底烧瓶中的现象为_________,产生此现象的化学反应方程式为__。
(2)轻轻摇动圆底烧瓶,观察到圆底烧瓶中的现象为①___________;②________。产生此现象的化学反应方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,Na2CO3溶液中存在CO32-+H2O![]() HCO3-+OH-平衡。下列说法不正确的是
HCO3-+OH-平衡。下列说法不正确的是
A.稀释溶液,[c(HCO3-)·c(OH-)]/c(CO32-)增大
B.通入CO2,溶液pH减小
C.升高温度,平衡常数增大
D.加入NaOH固体,c(HCO3-)/c(CO32-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Y是合成药物查尔酮类抑制剂的中间体,可由X在一定条件下反应制得:

下列叙述正确的是( )
A. 反应过程中加入K2CO3,能提高X的转化率
B. Y与Br2的加成产物分子中不含手性碳原子
C. X和Y均能与新制的Cu(OH)2在加热条件下反应生成砖红色沉淀
D. 等物质的量的X、Y分别与H2反应,最多消耗H2的物质的量之比为3∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氨水的叙述正确的是( )
A.氨水显碱性,是因为氨水是一种弱碱
B.氨水和液氨成分相同
C.氨水中物质的量浓度最大的粒子是NH3(除水外)
D.1mol·L-1的氨水指在1L溶液中含NH3、NH3·H2O、NH4+物质的量之和为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过量排放含氮物质会污染大气或水体,研究氮及其化合物的性质及转化,对降低含氮物质的污染有着重大的意义。
Ⅰ.对NO与O2反应的研究。
(1)已知氮氧化物转化过程中的焓的变化如下图所示,写出 NO转化为NO2的热化学方程式__________。
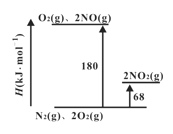
(2)2NO+O2![]() 2NO2的平衡常数表达式K=_______。其他条件不变,利用分子捕获器适当减少反应容器中NO2的含量,平衡常数K将_____(填“增大”、“减小”或“不变” )。
2NO2的平衡常数表达式K=_______。其他条件不变,利用分子捕获器适当减少反应容器中NO2的含量,平衡常数K将_____(填“增大”、“减小”或“不变” )。
(3)已知:2NO2(g)![]() N2O4(g) △H<0。在一定条件下,将2 mol NO和1 mol O2通入恒容密闭容器中进行反应,在不同温度下,测得平衡时体系中NO、O2、NO2的物质的量与温度的关系如下图所示。
N2O4(g) △H<0。在一定条件下,将2 mol NO和1 mol O2通入恒容密闭容器中进行反应,在不同温度下,测得平衡时体系中NO、O2、NO2的物质的量与温度的关系如下图所示。

①曲线c代表________的物质的量与温度的关系,x点对应的O2的转化率为________。
②根据上图可推测_________________。
A.2NO+O2![]() 2NO2的平衡常数:x点﹥y点
2NO2的平衡常数:x点﹥y点
B.y点时2NO+O2![]() 2NO2的反应速率:υ(正)﹤υ(逆)
2NO2的反应速率:υ(正)﹤υ(逆)
C.400~1200℃时,随着温度升高,N2O4体积分数不断增大
D.x点对应的NO的物质的量分数为4/11
Ⅱ.对废水中过量氨氮转化的研究。
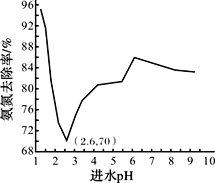
废水中过量的氨氮(NH3和NH4+)会导致水体富营养化。某科研小组用NaClO氧化法处理氨氮废水,将其转化为无污染物质,不同进水pH对氨氮去除率的影响如图所示。
已知:ⅰ.HClO的氧化性比NaClO强;
ⅱ.NH3比NH4+更易被氧化。
(4)pH=1.25时,NaClO与NH4+反应生成N2等无污染物质,该反应的离子方程式______。
(5)进水pH为1.25~6.00范围内,氨氮去除率随pH升高发生图中变化的原因是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com