
【题目】I.某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:
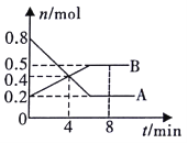
(1)该反应的化学方程式为___。
(2)若降低温度,则该反应的逆反应速率___。(填“加快”“减慢”或“不变”)。
(3)第4min时,正、逆反应速率的大小关系为:v(正)_v(逆)(填“>”、“<”或“=”)。
(4)反应至4min时,A的转化率为__。
(5)能判断该反应在一定温度下达到化学平衡状态的依据是__(填字母代号)。
A.v(A)=2v(B)
B.容器内压强不再发生变化
C.容器内气体密度不再发生变化
D.B的体积分数不再发生变化
E.容器内气体原子总数不再发生变化
F.相同时间内消耗2nmol的A的同时生成nmol的B
II.已知某可逆反应:aA(g)+bB(g)![]() cC(g)+dD(g)。请回答下列问题:
cC(g)+dD(g)。请回答下列问题:
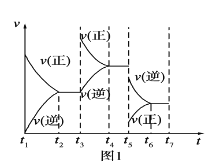

(1)根据实验测定结果,描绘出了该反应达到平衡状态时及改变外界条件后,反应速率与时间的关系图像(如图1所示),有利于提高D产量的变化过程是图像中的__段;引起该变化过程的外界条件是__。
(2)根据实验测定结果描绘出了图2。由此图像可以得出,升高温度,上述平衡将向__(填“正反应”、“逆反应”)方向移动,K值__(填“增大”、“减小”、“不变”);反应计量数之间的关系:a+b__c+d(填“大于”、“小于”、“等于”或“不确定”)。
【答案】2A(g)![]() B(g) 减慢 > 50% BD t3~t4 增大反应物浓度 逆反应 减小 大于
B(g) 减慢 > 50% BD t3~t4 增大反应物浓度 逆反应 减小 大于
【解析】
I、(1)由图可知,从反应开始,A的物质的量减少,B的物质的量增加,则A为反应物、B为生成物,开始至4min时,A减少0.8mol0.4mol=0.4mol,B增加0.4mol0.2mol=0.2mol,由物质的变化量之比等于化学计量数之比可知,A、B的化学计量数比为2:1,且后来达到平衡状态,则反应方程式为2A(g)![]() B(g);
B(g);
(2)降低温度,体系内活化分子数降低,运动速率降低,导致化学反应速率减慢;
(3)由图像可知,4min后,A的量还在减小,B的量还在逐渐增加,说明反应依旧在向正向进行,故v(正)>v(逆);
(4)0~4min,![]() n(A)=(0.8-0.4)mol=0.4mol,其转化率=
n(A)=(0.8-0.4)mol=0.4mol,其转化率=![]() =50%;
=50%;
(5)A、未标明该速率是正反应速率还是逆反应速率,无法据此判断该反应是否处于平衡状态,故A错误;
B、该反应在恒温恒容条件下进行,气体的物质的量之比=容器内压强之比,该反应属于气体非等体积反应,反应过程中,气体的物质的量会发生变化,当气体物质的量不变时,即容器内压强不再变化时,能够说明该反应达到平衡状态,故B正确;
C、该反应在反应过程中,气体的质量不变,且该反应是在恒容容器中进行,故气体的密度始终不变,故不能根据密度判断反应达到平衡状态,故C错误;
D、该反应正向进行过程中,B的体积分数逐渐增加,当B的体积分数不再发生变化时,可说明该反应达到平衡状态,故D正确;
E、根据原子守恒,该反应进行过程中,气体原子数目始终保持不变,故不能根据原子数目判断反应达到平衡状态,故E错误;
F、根据化学方程式计量数之比可知,任意时刻,消耗2nmol的A的同时生成nmol的B,故不能据此判断反应是否达到平衡状态,故F错误;
II、(1)根据图象知,t3改变条件瞬间,正反应速率增大、逆反应速率不变,平衡向正反应方向移动,说明增大反应物浓度;t5改变条件瞬间,正逆反应速率都减小,平衡向逆反应方向移动,改变条件应该是减小压强或降低温度,有利于提高D产量的变化过程是向正反应方向进行的过程,根据图象知利于提高D产量的变化过程是图象中的段t3~t4;改变的条件是增大反应物浓度;
(2)根据图象知,一定压强下,升高温度,C的体积分数减小,说明正反应是放热反应,升高温度平衡向逆反应方向移动,K值减小;相同温度下,增大压强,C的体积分数增大,平衡向正反应方向移动,则a+b>c+d。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(9分)某化学兴趣小组对生石灰与水反应是显著放热反应进行了实验探究,在除了用手触摸试管壁感觉发热外,还设计了下列几个可行性方案。
甲方案:将温度计与盛放有生石灰的小试管用橡皮筋捆绑在一起,放入有水的小烧杯中,用胶头滴管向小试管中缓缓滴入水,看到的现象是 ,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)

乙方案:将盛放有生石灰的小试管插入带支管的试管中,支管接①或②,用胶头滴管向小试管中缓缓滴入水,看到的现象是(接①) ,(接②) ,说明反应放热。
丙方案:用胶头滴管向盛放有生石灰且带支管的试管中滴加水,支管接的导管中盛适量无水硫酸铜粉末,看到的现象是 ,说明反应放热,其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可以证明2HI(g)![]() H2(g)+I2(g)已达平衡状态的是( )
H2(g)+I2(g)已达平衡状态的是( )
①单位时间内生成nmolH2的同时生成nmolHI
②一个H—H键断裂的同时有两个H—I键断裂
③温度和体积一定时,混合气体密度不再变化
④v(H2)=v(I2)=0.5v(HI)
⑤c(HI):c(H2):c(I2)=2:1:1
⑥温度和体积一定时,某一生成物浓度不再变化
⑦温度和体积一定时,容器内压强不再变化
⑧温度和压强一定时,混合气体的平均相对分子质量不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
A. ②③④⑤⑥B. ②⑥⑦⑧⑨
C. ①②⑥⑧D. ②⑥⑨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,现取三份100mL溶液进行如下实验:
,现取三份100mL溶液进行如下实验:
![]() 第一份加入
第一份加入![]() 溶液有沉淀产生;
溶液有沉淀产生;
![]() 第二份加足量NaOH溶液加热后,收集到气体
第二份加足量NaOH溶液加热后,收集到气体![]() ;
;
![]() 第三份加足量
第三份加足量![]() 溶液后,得干燥沉淀
溶液后,得干燥沉淀![]() ,经足量盐酸洗涤、干燥后,沉淀质量为
,经足量盐酸洗涤、干燥后,沉淀质量为![]() 根据上述实验,回答下列问题
根据上述实验,回答下列问题
(1)该溶液中一定存在的离子是______,可能存在的离子是______.
(2)求一定存在的离子中阳离子的浓度或浓度的取值范围______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不相符的是

A. 图甲表示反应:4CO(g)+2NO2(g)![]() N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
N2(g)+4CO2(g)ΔH <0,在其他条件不变的情况下,改变起始物CO的物质的量对此反应平衡的影响,则有T1>T2,K1>K2
B. 图乙表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,乙的压强比甲的压强大
3C(g)+D(g)的影响,乙的压强比甲的压强大
C. 图丙表示的反应是吸热反应,该图表明催化剂不能改变化学反应的焓变
D. 图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)![]() N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ![]() 。
。
A.![]() 溶于足量稀
溶于足量稀![]() :
:![]()
B.用食醋检验牙膏中碳酸钙的存在:![]()
C.![]() 酸性溶液放在空气中变质:
酸性溶液放在空气中变质:![]()
D.电解![]() 水溶液的离子方程式: 2Cl-+2H2O
水溶液的离子方程式: 2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沙罗特美是一种长效平喘药,其合成的部分路线如下:
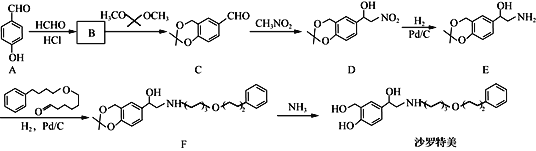
(1)F中的含氧官能团名称为____________。
(2)A的名称为____________。
(3)D→E的反应类型为____________,沙罗特美的分子式为____________。
(4)B的分子式为C8H8O3,与(CH3)2C(OCH3)2发生取代反应得到物质C和CH3OH,写出B的结构简式:____________________。
(5)判断同时满足下列条件的C的同分异构体的数目:_______。(不考虑立体异构)
①分子中含有![]() 结构且只有一个环状结构,与FeCl3发生显色反应;
结构且只有一个环状结构,与FeCl3发生显色反应;
②能与NaHCO3发生反应放出CO2。
③苯环上有且只有三个取代基
(6)请写出以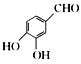 、(CH3)2C(OCH3)2、CH3NO2为原料制备
、(CH3)2C(OCH3)2、CH3NO2为原料制备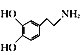 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。_____________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是( )
A.![]() 和
和![]() 不属于同分异构体
不属于同分异构体
B.质量相同的![]() 和
和![]() 完全燃烧时消耗氧气的质量较少的是
完全燃烧时消耗氧气的质量较少的是![]()
C.连接四个不同基团的碳原子为“手性碳原子”,![]() 含有两个手性碳原子
含有两个手性碳原子
D.标准状况下![]() L溴乙烷所含化学键总数为
L溴乙烷所含化学键总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种将燃料电池与电解池组合制备KMnO4的装置如图所示(电极甲、乙、丙、丁均为惰性电极)。该装置工作时,下列说法不正确的是

A. 甲为正极,丙为阴极
B. 丁极的电极反应式为MnO42――e-===MnO4-
C. KOH溶液的质量分数:c%>a%>b%
D. 标准状况下,甲电极上每消耗22.4L气体时,理论上有4molK+移入阴极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com