
【题目】A、B、C、D、E、F为原子序数依次增大的前36号元素,其中只有两种金属元素。A与C同主族,B与E同主族;B与C能形成两种常见化合物;C与F最外层只有1个电子,且内层均已排满;基态D原子成对电子数是未成对电子数的4倍。
请问答下列问題:
(1)基态B原子的轨道表达式为______,其最高能级的电子云有_____个不同的伸展方向。
(2)B、C、E原子半径由大到小的顺序为_________(用元素符号表示)。
(3)D和E中第一电离能较大的是_______(填元素符号),原因为___________。
(4)A与B形成的最简单化合物比A与E形成的最简单化合物的熔点______(填“高“或“低”),原因为___________。
(5)D的最高价氧化物对应的水化物中,D原子的杂化轨道类型为______,已知该分子中除氢外其他原子均满足最外层8电子稳定结构,则其结构式为________。
(6)单质F及其同族元素P、Q的堆积模型均为面心立方最密堆积,三种原子的半径分别为128pm、144pm、144pm,其中P和Q的相对原子质量分别为Mτ(P)、Mτ(Q)。
①单质F中的配位数为______;密度为_____g/cm3(用NA表示阿伏加德罗常数的值,列式即可)。
②单质P和Q的密度之比为________[用含Mτ(P)、Mτ(Q)的代数式表示]。
【答案】 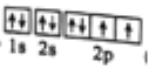 3 Na>S>O P P的3p轨道处于半充满状态,较难失去1各电子 高 水分子间较易形成氢键 sp3
3 Na>S>O P P的3p轨道处于半充满状态,较难失去1各电子 高 水分子间较易形成氢键 sp3 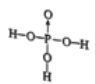 12
12 ![]()
![]()
【解析】根据题意可推断A、B、C、D、E、F分别为H、O、Na、P、S、Cu。
(1)基态B原子的轨道表达式为![]() 其最高能级的电子云有3个不同的伸展方向。
其最高能级的电子云有3个不同的伸展方向。
(2)根据电子层数和核内质子数的关系可得原子半径:r(Na)>r(S)>r(O)。
(3)P的3p轨道处于半充满状态,较难失去一个电子,所以第一电离能较大。
(4)水分子间较易形成氢键,所以熔点较高。
(5)D的最高价氧化物对应的水化物为H3PO4,分子的中心P原子为sp3杂化,除氢外其他原子均满足最外层8电子稳定结构,可知P与O之间形成了一个配位键,结构式为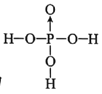 。
。
(6)①面心立方最密堆积的配位数为12;其密度为![]() 。
。
②P与Q的堆积方式相同,原子半径相同,所以密度之比即为摩尔质量之比,即相对原子质量之比。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.下面列出了几组物质,请将物质的合适序号填写在空格上。
①金刚石和石墨 ②D和T ③12C和13C ④O2和O3
⑤CH4和CH3CH2CH3 ⑥CH2=CHCH3和CH2=CH2
⑦CH3CH(CH3)CH2CH3和CH3(CH2)3CH3 ⑧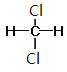 和
和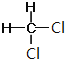
同系物____________;同分异构体____________。
Ⅱ.篮烷分子的键线式如图所示,试回答:
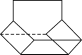
篮烷的一氯代物的种数为________种(不考虑立体异构)。
Ⅲ.在一定温度下,体积为2 L的恒容密闭容器中,NO2和N2O4之间发生反应2NO2(g) ![]() N2O4(g),如图所示。
N2O4(g),如图所示。
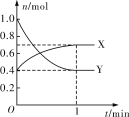
(1)曲线____________ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)该反应达到限度时,Y的转化率是__________,反应开始时与反应达到平衡状态时的压强之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CO2转化为甲醇的原理为 CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H<0.500℃时,在体积为1L 的固定容积的密闭容器中充入1mol CO2、3mol H2 , 测得CO2浓度与CH3OH 浓度随时间的变化如图所示,从中得出的结论错误的是( ) 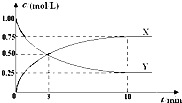
A.曲线X可以表示CH3OH(g) 或H2O(g) 的浓度变化
B.从反应开始到10min时,H2的反应速率v(H2)=0.225mol/(L﹒min)
C.平衡时H2 的转化率为75%
D.500℃时该反应的平衡常数K=3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的短周期元素,对应单质为a、b、c、d、e。B、C、D的最外层电子数之和为10,对应的最高价氧化物的水化物分别为m、n、p;q为B和E形成的二元化合物。上述物质发生的转化关系如图所示(部分产物已略去)。下列说法不正确的是
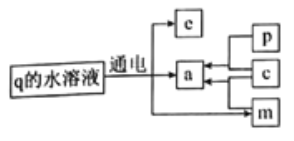
A. 可通过电解熔融状态的q制备b和e
B. 原子半径:B>C>D>E>A
C. n既能溶解在m的水溶液中,又能溶解在p的水溶液中
D. d可以保存在CS2中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)2SO2(g)+O2(g)2SO3(g)反应过程的能虽变化如图所示.己知1mol SO2(g)氧化为1mol SO3(g)的△H=﹣99kJ/mol. 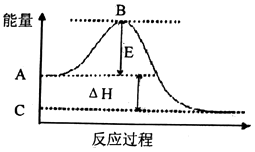
请回答下列问题:
①E的大小对该反应的反应热(填“有”或“无”)影构.
②图中△H=kJ/mol.
(2)由氢气和氧气反应生成1mol水蒸气,放出241.8kJ热量(25℃、101kPa下测得) ①写出该反应的热化学方程式: .
②若lmol水蒸气转化为液态水放热45kJ,则反应H2(g)+ ![]() O2(g)=H2O(l)的△H=kJ/mol.
O2(g)=H2O(l)的△H=kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图. 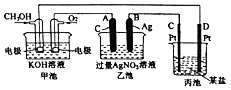
(1)通入O2的电极名称、C(Pt)电极的名称是 .
(2)写出通入O2的电极上的电极反应式是 .
(3)写出通入CH3OH的电极上的电极反应式是 .
(4)若丙池是电解饱和食盐水溶液,则阳极的电极反应为 , 阴极的电极反应为 . 在(阳极或阴极)附近滴入酚酞溶液变红.
(5)乙池中反应的化学方程式为 .
(6)当乙池中B(Ag)极的质里增加5.40g时,甲池中理论上消耗O2mL(标准状况下);若丙池中饱和食盐水溶液的体枳为500mL,电解后,溶液的pH= . (25℃,假设电解前后溶液的体积无变化).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2=2AB的能量变化如图所示,则下列说法正确的是( ) 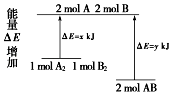
A.该反应的反应热△H=x﹣y kJ/mol
B.断裂1 mol A﹣A键和1 mol B﹣B键放出x kJ能量
C.2 mol AB的总能量高于1 mol A2和1 mol B2总能量
D.该反应是吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com