
【题目】BaCl2·xH2O中结晶水数目可通过重量法来确定:
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g。
回答下列问题:
(1)在操作②中,需要先后用稀硫酸和___________洗涤沉淀;检验沉淀中氯离子是否洗净的方法是___________。
(2)计算BaCl2·xH2O中的x=_________(要求写出计算过程)。
(3)操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果_________(填“偏低”、“偏高”或“不变”)。
【答案】蒸馏水 取水洗液于试管中,加入稀硝酸酸化,滴加AgNO3溶液,若无白色浑浊出现,则表明Cl-已经冼净 沉淀1.165g为硫酸钡质量,其物质的量=![]() =5.000×10-3mol,故氯化钡晶体中氯化钡的质量=0.005mol×208g/mol=1.04g,含有结晶水的质量=1.222g-1.04g=0.182g,则208:18x=1.04g:0.182g,解得x≈2 偏高
=5.000×10-3mol,故氯化钡晶体中氯化钡的质量=0.005mol×208g/mol=1.04g,含有结晶水的质量=1.222g-1.04g=0.182g,则208:18x=1.04g:0.182g,解得x≈2 偏高
【解析】
(1)应用硫酸与蒸馏水进行沉淀洗涤;具体方法是取水洗液于试管中,加入稀硝酸酸化,滴加AgNO3溶液,若无白色浑浊出现,则表明Cl-已经冼净;
(2)根据硫酸钡质量计算氯化钡质量,进而计算水的质量,根据二者质量之比确定x的值;
(3)部分沉淀被滤纸中的碳还原为BaS,单质固体硫酸钡的质量偏小,测定氯化钡的质量偏小,水的质量偏大。
(1)应用硫酸与蒸馏水进行进行沉淀洗涤,具体方法是取水洗液于试管中,加入稀硝酸酸化,滴加AgNO3溶液,若无白色浑浊出现,则表明Cl-已经冼净;
故答案为:蒸馏水;取水洗液于试管中,加入稀硝酸酸化,滴加AgNO3溶液,若无白色浑浊出现,则表明Cl-已经冼净;
(2)沉淀1.165g为硫酸钡质量,其物质的量=![]() =5.000×10-3mol,故氯化钡晶体中氯化钡的质量=0.005mol×208g/mol=1.04g,含有结晶水的质量=1.222g-1.04g=0.182g,则208:18x=1.04g:0.182g,解得x≈2;
=5.000×10-3mol,故氯化钡晶体中氯化钡的质量=0.005mol×208g/mol=1.04g,含有结晶水的质量=1.222g-1.04g=0.182g,则208:18x=1.04g:0.182g,解得x≈2;
故答案为:2;
(3)部分沉淀被滤纸中的碳还原为BaS,单质固体硫酸钡的质量偏小,测定氯化钡的质量偏小,水的质量偏大,故x的值偏高;
故答案为:偏高。


科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L。体积分别为![]() 和
和![]() 的HA溶液与BOH溶液按不同体积比混合,保持
的HA溶液与BOH溶液按不同体积比混合,保持![]() +
+![]() =100mL,
=100mL,![]() 、
、![]() 与混合溶液的pH的关系如图所示。下列说法正确的是( )
与混合溶液的pH的关系如图所示。下列说法正确的是( )
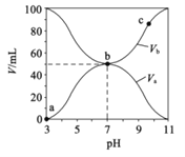
A.a→b过程中水的电离程度始终增大
B.![]() mol/L1
mol/L1
C.b点时,c(B-)=c(A-)=c(OH-)=c(H+)
D.由图可知BOH一定是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”![]() 以下有关主族元素原子的“未成对电子”的说法,错误的是
以下有关主族元素原子的“未成对电子”的说法,错误的是![]()
A.核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子”
B.核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子”
C.原子轨道中含有“未成对电子”的基态原子,其核外电子数可能为偶数
D.原子轨道中不含“未成对电子”的基态原子,其核外电子数一定为偶数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蚊虫、蚂蚁等叮咬人时,常向人体血液注入一种含有蚁酸(甲酸,HCOOH)的液体。
(1)写出甲酸在溶液中的电离方程式: ___________。
(2)当人受到蚂蚁叮咬时,皮肤上会起小疱,即使不治疗,过一段时间小疱也能自行痊愈,其原因为 ________。有同学认为,受到蚂蚁叮咬时及时涂抹稀氨水或肥皂水能起到治疗作用,这一观点________(填“正确”或“不正确”)。
(3)已知:25 ℃时,HCOOH的电离平衡常数K=1.8×10-4,H2CO3的电离平衡常数Ka1=4.3×10-7,Ka2=5.6×10-11。下列说法正确的是(______)
A.向碳酸钠溶液中加入甲酸溶液看不到明显现象
B.25 ℃时,向甲酸溶液中加入NaOH溶液,甲酸的电离程度和K值均增大
C.向0.1 mol·L-1甲酸溶液中加入蒸馏水,c(H+)增大
D.向碳酸中加入NaHCO3固体,溶液中c(H+)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量的判断和表示方法正确的是( )
A.由C(s,石墨)=C(s,金刚石) ΔH=+1.9 kJ·mol-1,可知:金刚石比石墨更稳定
B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
C.由H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,可知:含1 mol/L CH3COOH的溶液与含1mol/L NaOH的溶液混合,放出热量等于57.3 kJ
D.2gH2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为H2(g)+![]() O2(g) =H2O(l) ΔH=-285.8 kJ/mol
O2(g) =H2O(l) ΔH=-285.8 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. 混合气的平均分子量不再改变
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。已知:CO(g)+H2O(g)H2(g)+CO2(g)平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
试回答下列问题:
(1)上述正向反应是________反应 (填“放热”或“吸热”);
(2)下列条件的改变能加快其反应速率的是_______(选填序号);
①升高温度;②保持体积不变,只增加CO的质量;③保持体积不变,充入Ne使体系压强增大;④保持压强不变,充入Ne使容器的体积增大
(3)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2,发生反应CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如下图所示:
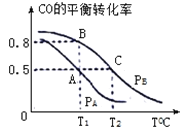
①A、B两点对应的压强大小关系是PA________PB;(填“>”,“<”,“=”)
②A、B、C三点的平衡常数KA、KB、KC的大小关系是 ____________;
③在P1压强、T1℃时,该反应的平衡常数K=___________;
(4)T1℃、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol H2:0.2mol CH3OH:0.2mol。此时v正 ____ v逆(填 >、< 或 =)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
I.[查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.[制备产品]
实验装置如图所示(省略夹持装置)
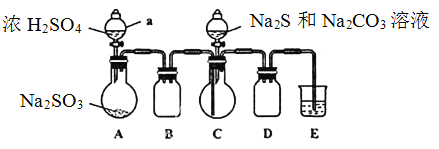
实验步骤:
(1)检查装置气密性,按图示加入试剂。仪器a的名称是____;E中的试剂是___(选填下列字母编号)。
A.稀H2SO4B.NaOH溶液 C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加浓H2SO4。
(3)待Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合液,滤液经____(填写操作名称)、结晶、过滤、洗涤、干燥、得到产品。
Ⅲ.[探究与反思]
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,_____,若沉淀未完全溶解,并有刺激性气味的气体产生,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成的Na2SO4的量,在不改变原有装置的基础上对原有实验步骤(2)进行了改进,改进后的操作是_______。
(3)Na2S2O3·5H2O的溶解度随温度升高显著增大,所得产品通过_____方法提纯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应“P4(s)+3NaOH(aq)+3H2O(l)=3NaH2PO2(aq)+PH3(g) ΔH>0”制得的NaH2PO2可用于化学镀镍。下列说法正确的是

A. P4分子中P原子均满足8电子稳定结构
B. 反应中NaOH作还原剂
C. 该反应能自发进行,则ΔS<0
D. 反应中生成1 mol NaH2PO2,转移电子数目为3×6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com