
【题目】 X、Y、Z、W、R是短周期中的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | 原子核内无中子 |
Y | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
Z | 地壳中含量最高的元素 |
W | 原子质量数为23,中子数为12 |
R | 其离子是第三周期金属元素的离子中半径最小的 |
(1)Y、Z、W、R四种元素的原子半径从大到小的顺序是_____________(用元素符号表示)。
(2)Y2电子式为 ;X、Y、Z形成的化合物可用作化肥,该物质所含化学键的类型是 (填共价或离子);X与Z形成的18e-微粒的结构式为 。
(3)砷(As)是人体必需的微量元素,与Y同一主族,As原子比Y原子多两个电子层,则砷的原子序数为________,其最高价氧化物的化学式为____________。该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是__________________(用化学式表示)。
(4)W在元素周期表中的位置为_______;能够说明W和R金属性强弱的依据有 。
a.W单质的熔点比R单质的熔点低
b.W的化合价比R的低
c.常温下W单质与水的反应很剧烈,而R单质在加热条件下与水反应现象不明显
d.W最高价氧化物的水化物的碱性比R强
(5)写出工业上冶炼R的化学反应方程式 。
【答案】(1) Na>Al>N>O(1分) (2) ![]() (1分) 离子键 共价键(2分)
(1分) 离子键 共价键(2分)
H—O—O—H(1分) (3) 33 As2O5 NH3>PH3>AsH3(各1分)
(4) 第三周期第ⅠA族 cd(各1分) (5)2Al2O3![]() 4Al+3O2↑(2分)
4Al+3O2↑(2分)
【解析】
试题分析:X 原子核内无中子,则X是H;Y是组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2,则Y是N;Z是地壳中含量最高的元素,因此Z是O;W是原子质量数为23,中子数为12,因此W的质子数=23-12=11,所以W是Na;R离子是第三周期金属元素的离子中半径最小的,所以R是Al。
(1)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则Y、Z、W、R四种元素的原子半径从大到小的顺序是Na>Al>N>O。
(2)N2电子式为![]() ;X、Y、Z形成的化合物硝酸铵可用作化肥,该物质所含化学键的类型是离子键和共价键;X与Z形成的18e-微粒为双氧水,其结构式为H—O—O—H。
;X、Y、Z形成的化合物硝酸铵可用作化肥,该物质所含化学键的类型是离子键和共价键;X与Z形成的18e-微粒为双氧水,其结构式为H—O—O—H。
(3)砷(As)是人体必需的微量元素,与Y同一主族,As原子比Y原子多两个电子层,则砷的原子序数=2+8+18+5=33,其最高价是+5价,则其氧化物的化学式为As2O5。同主族自上而下非金属性逐渐减弱,氢化物稳定性逐渐减弱,则该族第二到四周期元素的气态氢化物的稳定性从大到小的顺序是NH3>PH3>AsH3。
(4)Na的质子数是11,在元素周期表中的位置为第三周期第ⅠA族;A、金属性强弱与单质的熔沸点没有关系,a错误;b、金属性强弱与化合价没有关系,b错误;c、常温下W单质与水的反应很剧烈,而R单质在加热条件下与水反应现象不明显,这说明金属性是Na强于Al,c正确;d、金属性越强,最高价氧化物水化物的碱性越强在,则W最高价氧化物的水化物的碱性比R强说明钠的金属性强于铝,d正确,答案选cd。
(5)铝是活泼的金属,工业上冶炼R的化学反应方程式为2Al2O3![]() 4Al+3O2↑。
4Al+3O2↑。


科目:高中化学 来源: 题型:
【题目】用98%的浓H2SO4(密度为1.84g/cm3)配制1 mol/L的稀H2SO4 90 mL,配制过程中需用仪器的先后顺序是( )
①20 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒
A.①③⑤⑥⑦ B.②③⑦⑤⑥
C.②⑤⑦⑥① D.④③⑦⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化学反应过程中能量变化的曲线图。下列有关叙述正确的是( )
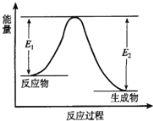
A.该反应为吸热反应
B.该图可以表示Ba(OH)2.8H2O与NH4Cl的反应
C.化学反应中的能量变化只表现为热量的变化
D.化学反应中有旧键断裂就一定有新键形成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量的水中,有1.16g白色沉淀析出,向所得的浊液里,逐渐加入0.5mol/L的盐酸,加入盐酸的体积和生成沉淀的质量如图所示:
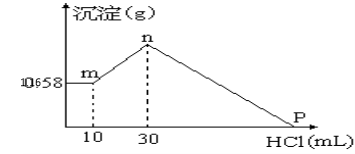
(1) 写出m-n段反应的离子方程式 。
(2) 混合物中NaOH的物质的量是____________,AlCl3的物质的量是 ,MgCl2的物质的量是___________。
(3) P点所表示的加入盐酸的体积是_________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.大量燃烧化石燃料是造成雾霾的一种重要因素
B.食品中的抗氧化剂本身是难于氧化的物质
C.含SO42﹣的澄清溶液中不会含Ba2+
D.凡溶于水能电离出H+离子的化合物均属于酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A.乙烯使溴的四氯化碳溶液褪色
B.乙烯使酸性KMnO4溶液褪色
C.将苯滴入溴水中,振荡后水层接近无色
D.甲烷与氯气混合,光照后黄绿色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
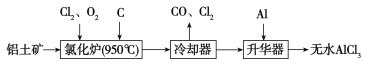
(1)为促进反应的进行,实际生产中需加入焦炭,其原因是
______________________________________________。
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式为
_______________________________________________。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件。该小组同学为探究中毒原因进行了如下实验。
(1)小组同学依据漂白液具有漂白消毒的性质推测,漂白液中ClO-具有氧化性。实验如下:
Ⅰ. 用pH试纸检验,漂白液pH>7,饱和![]() 溶液pH<7。
溶液pH<7。
Ⅱ. 取10 mL漂白液,依次加入Na2SO3溶液和BaCl2溶液,有白色沉淀生成,经检验白色沉淀不溶于盐酸。
Ⅲ. 另取10 mL,漂白液,加入品红溶液,溶液红色逐渐变浅,一段时间后褪为无色。
Ⅳ. 再取10 mL漂白液,加入品红溶液,加入少量稀硫酸酸化后,溶液红色立即变为无色。
①漂白液pH大于7的原因是(用离子方程式表示)__________。
②由实验Ⅱ得出ClO-具有氧化性,写出相应的离子方程式__________。
③对比实验Ⅲ和Ⅳ说明ClO-氧化性与溶液酸碱性的关系是__________。
(2)小组同学依据(1)中的实验,提出:漂白液在酸性溶液中有Cl2生成。用图所示的装置继续实验,探究漂白液在酸性溶液中是否能反应生成Cl2。
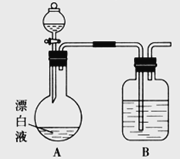
①装置B的作用是__________;盛放的药品是__________。
②若打开分液漏斗活塞向烧瓶中加入硫酸,不久烧瓶中有黄绿色气体产生。A中反应的离子方程式________。
③若打开分液漏斗活塞向烧瓶中加入饱和![]() 溶液,观察到产生大量的白色胶状沉淀,同时有黄绿色气体产生。A中加
溶液,观察到产生大量的白色胶状沉淀,同时有黄绿色气体产生。A中加![]() 溶液反应的离子方程式是__________。
溶液反应的离子方程式是__________。
(3)上述实验说明漂白液与酸性溶液混合会产生Cl2。若取10 mL漂白液与足量BaCl2溶液混合后,不断通入SO2至过量,在实验过程中可能的实验现象是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com