
����Ŀ��ij�о���ѧϰС�����ⶨ������(25 ����101 kPa)������Ħ���������ش��������⡣��С����Ƶļ���ʵ��װ������ͼ��ʾ��

��ʵ�����Ҫ�����������£�
����һ:
��1��������100 mL 1.0 mol��L��1������,��Ҫ20%,�ܶ�Ϊ1.1g��cm-3����������Ϊ______��
�����ƹ���������Ҫ�IJ���������__________________________________________��
�����в����ᵼ�����ʵ���Ũ��ƫ�����_________________
A��ת����Һ��δϴ���ձ��Ͳ�������ֱ�Ӷ���
B��������ƿ�н��ж���ʱ���ӿ̶���
C��������ƿ�н��ж���ʱ���ӿ̶���
D�����ݺ������ƿ����ҡ�ȣ�����Һ����ڿ̶��ߣ��ֲ�������ȱ��ˮ
�����: ����Ͳ��ȡ��10.0 mL 1.0 mol��L��1�����������ƿ�У�
������: ��2����ȡa g�ѳ�ȥ��������Ĥ��þ������ϵ��ͭ˿ĩ�ˣ�ΪʹHClȫ���μӷ�Ӧ��a����ֵ����Ϊ________��
������: �����ƿ��װ������ˮ������ͼ���Ӻ�װ�ã����װ�õ������ԣ�
������: ��3����Ӧ���������ϵ�¶Ȼָ������£���ȡ��Ͳ��ˮ�����ΪV mL��
��ʵ�鲽������Ӧѡ��________(�����)����Ͳ��
A��100 mL������B��200 mL������C��500 mL
�ڶ���ʱ���ָ�������,������Һ�尼Һ�����ʹ���ƽ�⣬��Ҫע��_____________________��
��������ˮ������Ӱ�죬��ʵ�������²������Ħ������ļ��㹫ʽΪVm��________����δ��ȥþ�����������Ĥ����������________(����ƫ������ƫС��������Ӱ����)��
���𰸡� 16.6mL ��Ͳ���ձ���100 mL����ƿ����ͷ�ιܣ������� C 0.12 B ��Ͳ�ڵ�Һ������ƿ��Һ����ƽ 0.2V L��mol��1 ƫС
��������������֪����ʵ��ԭ������һ����������������þ��Ӧ������������ˮ������ˮ����������������������������������ʵ���ȷ�����������ʵ��������һ�������µ�����Ħ�������
����һ:
��1����20%,�ܶ�Ϊ1.1g��cm-3����������ʵ���Ũ��Ϊ![]() mol/L������ϡ�Ͷ���c1V1=c2V2�����������100 mL 1.0 mol��L��1������,��Ҫ20%,�ܶ�Ϊ1.1g��cm-3����������Ϊ
mol/L������ϡ�Ͷ���c1V1=c2V2�����������100 mL 1.0 mol��L��1������,��Ҫ20%,�ܶ�Ϊ1.1g��cm-3����������Ϊ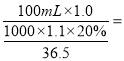 16.6mL��
16.6mL��
�����ƹ���������Ҫ�IJ�����������Ͳ���ձ���100 mL����ƿ����ͷ�ιܣ���������
��A��ת����Һ��δϴ���ձ��Ͳ�������ֱ�Ӷ��ݣ����ʼ��٣�Ũ��ƫС��B��������ƿ�н��ж���ʱ���ӿ̶��ߣ�Һ����ڿ̶��ߣ���Һ���ƫ��Ũ��ƫС��C��������ƿ�н��ж���ʱ���ӿ̶�����Һ����ڿ̶��ߣ�Ũ��ƫ��D�����ݺ������ƿ����ҡ�ȣ�����Һ����ڿ̶��ߣ��ֲ�������ȱ��ˮ����Һ�����ƫ���ˣ�Ũ��ƫС�����Ե������ʵ���Ũ��ƫ�����C��
�����: ����Ͳ��ȡ��10.0 mL 1.0 mol��L��1�����������ƿ�������Լ����n(H+)=0.01mol�������ܽ�þ�����ʵ���n(Mg)=1/2 n(H+)=0.005mol�������Ͽ����������������ʵ���Ϊ0.005mol����Щ�����ڱ�״�������Ϊ112mL��
������: ��2����ȡa g�ѳ�ȥ��������Ĥ��þ������ϵ��ͭ˿ĩ�ˣ�ΪʹHClȫ���μӷ�Ӧ��n(Mg)����Ϊ0.005mol��þ��Ħ������Ϊ24g/mol������a����ֵ����Ϊ0.12��
������: �����ƿ��װ������ˮ������ͼ���Ӻ�װ�ã����װ�õ������ԣ�
������: ��3����Ӧ���������ϵ�¶Ȼָ������£���ȡ��Ͳ��ˮ�����ΪV mL��
����Ͳ�е�ˮ�������ų��ģ�����ˮ�����������������������������ڱ�״�������Ϊ112mL����25 �桢101 kPa�¹��Ʋ��ᳬ��200mL��һ��ѹǿ�£��������������ѧ�¶ȳ����ȣ������ʵ�鲽������Ӧѡ��B��200 mL������Ͳ��
�ڶ���ʱ���ָ�������,������Һ�尼Һ�����ʹ���ƽ�⣬Ϊ��֤��Ӧװ��ϵͳ�����ѹǿ��ȣ���Ҫע����Ͳ�ڵ�Һ������ƿ��Һ����ƽ��������õ�����Ž�ȷ��
��������ˮ������Ӱ�죬��ʵ�������²������Ħ������ļ��㹫ʽΪVm��![]() =0.2V L��mol��1����δ��ȥþ�����������Ĥ�������ɵ�����������٣�ʹ�������ƫС��
=0.2V L��mol��1����δ��ȥþ�����������Ĥ�������ɵ�����������٣�ʹ�������ƫС��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����װ����ͼ��ʾ��������װ��KI��������Һ���м��������ӽ���Ĥ��������һ���ĵ�ѹ��ͨ�磬���������Һ����ɫ��һ��ʱ�����ɫ��dz����֪��3I2+6OH-=IO3-+5I-+3H2O������˵������ȷ���ǣ� ��

A. �Ҳ���ĵ缫����ʽ��2H++2e-=H2��
B. ������ʱ���Ҳ���Һ�к���IO3-
C. �����ڷ�����Ӧ���ܻ�ѧ����ʽKI+3H2O=KIO3+3H2��
D. ����������ӽ���Ĥ���������ӽ���Ĥ�������ڷ������ܻ�ѧ����ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ɫ��Һ��SO2���ã�������ɫ����ʵ����ͬ����(����)
��Ʒ����Һ�� ��KMnO4������Һ�� ����ˮ�� �ܵ��з�̪��NaOH��Һ
A. �ڢ� B. �٢� C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йػ�ѧ��Ӧ��˵������ȷ����
A. �Է���Ӧ���Ƿ��ȷ�ӦB. �Է���Ӧ����������ķ�Ӧ
C. �Է���Ӧһ����ʵ��D. ���Է���Ӧ��һ����������ʵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й������Ӽ����˵������ȷ������������
A. ��ij��Һ�м���AgNO3��Һ�����ɰ�ɫ����������Һ��һ������Cl��
B. ��ij��Һ�м���ϡ���ᣬ������ɫ���壬�����Һ��һ������CO![]()
C. ��ij��Һ�м���NaOH��Һ������ɫʯ����ֽ�����ݳ������壬��ֽ��죬�����Һ��һ������NH4+
D. ��ij��Һ�м���2��KSCN��Һ����Һ���Ժ�ɫ��������Һ�мӼ������Ƶ���ˮ����Һ��Ϊ��ɫ�������Һ��һ������Fe2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ƿ�з���ͭƬ��ϡ���ᣬ����ȡ�ϴ�����һ����������Ӧ��ʼ������ƿ�г�������ɫ���壬��ʱ�IJ���Ӧ�� (����)��
A. ���������ռ��������������ſ������ռ�
B. ����ƿ�к���ɫ������ʧ���������ſ������ռ�
C. ����ƿ�к���ɫ������ʧ������ˮ���ռ�
D. ��������ˮ���ռ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���2L�����ܱ������г���1mol PCl5 �� ������Ӧ��PCl5��g��PCl3��g��+Cl2��g�� ��Ӧ�����вⶨ�IJ������ݼ�������Ӧ�������������䣩��
t/s | 0 | 30 | 150 | 250 | 350 | 450 |
n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 | x |
��ش��������⣺
��1��x ��ֵ����
��2��0��50s �ڣ���PCl3��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ��������
��3��250s �Ժ�Cl2�����ʵ������ٸı��ԭ������
��4��250s ʱ��������Cl2�����ʵ����� �� PCl5�����ʵ����� �� PCl5��ת������ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ڿ�������Դ���ǣ� ��
����Ȼ�� ���������� �۵����� ��ʯ�� ��̫���� ��ϫ�� �߷��� ������
A.�٢ڢۢ�B.�ڢۢݢޢߢ�C.�ܢݢޢߢ�D.�٢ڢۢݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʣ�����ˮ���������( )
A. KCl��NaCl B. CuSO4��Na2SO4 C. CaCO3��Na2CO3 D. NH4NO3��NaNO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com