
【题目】下列反应的离子方程式书写正确的是
A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-
B.向FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+
C.向澄清石灰水中通入CO2:2OH-+CO2=CO32-+H2O
D.向稀HNO3溶液中加入少量铜粉:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
科目:高中化学 来源: 题型:
【题目】利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是( )
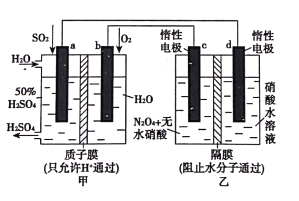
A.b电极反应式是O2+4e-+2H2O=4OH-
B.甲中每消耗l mol SO2,a电极附近溶液H+增加2mol
C.c电极反应式是N2O4-2e-+H2O=N2O5+2H+
D.甲、乙装置中分别生成的硫酸和N2O5的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种重要的有机化工原料,为探究草酸的制取和草酸的性质,进行如下实验:
实验Ⅰ:实验室用硝酸氧化淀粉水解液法制备草酸,装置如图所示:
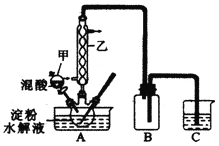
①一定量的淀粉水解液加入三劲烧瓶中
②控制反应温度55~60℃,边搅拌边缓慢滴加一定量的混合酸(65%的H2SO4与98%的H2SO4的质量比为2:1.25)
③反应3小时,冷却,有随后再重结晶得到草酸晶体硝酸氧化淀粉水解液的反应为:C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9H2O
(1)装置B的作用是 ______
(2)如何检验该装置的气密性: ______
(3)要控制反应温度55~60℃,应选择加热的方式是 ______,C装置中应加入 ______溶液。
实验Ⅱ:探究草酸与酸性高锰酸钾的反应
(4)向草酸溶液中逐滴加硫酸酸化的高锰酸钾溶液时,可观察到溶液由紫红色变为近乎无色,写出上述反应的离子方程式:______
(5)学习小组的同学发现,当向草酸溶液中逐滴加入硫酸酸化的高锰酸钾溶液时,溶液褪色总是先慢后快,为探究其原因,同学们做了如下对比实验:
实验序号 | H2C2O4(aq) | KMnO4(H+)(aq) | MnSO4(s) 质量(g) | 褪色时间(g) | ||
c(mol/L) | V(mL) | c(mol/L) | V(mL) | |||
实验1 | 0.1 | 2 | 0.01 | 4 | 0 | 30 |
实验2 | 0.1 | 2 | 0.01 | 4 | 5 | 4 |
由此你认为溶液褪色总是先慢后快的原因是 ______
(6)为测定上述实验中得到草酸的纯度,取5.0 g该草酸样品,配制成250 mL溶液,然后取25.00 mL此溶液溶于锥形瓶中,将0.10 mol/L酸性KMnO4溶液装在 ______(填仪器名称)中进行滴定,达到滴定终点时的现象是 ______,若消耗酸性KMnO4溶液体积为20.00 mL,则该草酸样品的纯度为 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量,某兴趣小组进行下面实验探究,查阅资料知道:
①2NO + Na2O2=2NaNO2
②2NO2+ Na2O2=2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-还原成Mn2+。
Ⅰ.产品制备与检验:用如下装置制备NaNO2:

(1)写出装置A烧瓶中发生反应的化学方程式并标出电子转移的方向和数目________。
(2)B装置的作用是______________________________。
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净NaNO2应在B、C装置间增加一个装置,请在框内画出增加的装置图,并标明盛放的试剂________。

(4)试设计实验检验装置C中NaNO2的存在(写出操作、现象和结论)________。
Ⅱ.含量的测定
称取装置C中反应后的固体4.000g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
滴定次数 | 1 | 2 | 3 | 4 |
KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
(5)第一组实验数据出现异常,造成这种异常的原因可能是________(双项选择)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
D.滴定终了俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数____________________。
(结果保留4位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。
(1)乙同学认为甲同学的结论是错误的,他的理由是__________________________(用化学方程式表示),所以他认为应该检验__________(填化学式)的产生来证明碳与浓硝酸反应。为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。

(2)为了减少干扰,对于A装置有下面4种操作方案,其中最合理的是(填写数字序号)_______。
①将炭与浓硝酸一同放在装置中加热;②先加热浓硝酸,然后将炭投入其中;
③先加热炭,再加入冷浓硝酸; ④先加热炭,再将炭投入冷浓硝酸。
(3)请用平衡移动原理解释B装置的作用____________________________________。
(4)C装置中出现的现象是_______________________________________________,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的化学方程式___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸(a-羟基丁二酸)是一种健康食品饮料,结构为: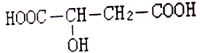 ,下列关于苹果酸的说法不正确的是
,下列关于苹果酸的说法不正确的是
A. 在铜或银作催化剂条件下加热,能与氧气反应
B. 在一定条件下能形成环状有机化合物
C. 在氢氧化钠的乙醇溶液中加热,能发生消去反应
D. 能发生缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(G2762011)规定葡萄酒中c最大使用量为0.25g/L.某兴趣小组用图装置(夹持装置略)收集某葡萄酒中SO2,并对含量进行测定。
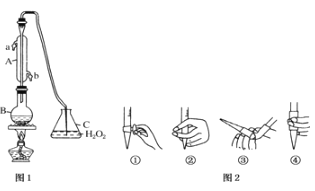
(1)仪器A的名称是________,水通入A的进口为_______________
(2)B中加入300.0ml葡萄酒和适量盐酸,加热使SO2全部逸出与C中H2O2完全反应其化学方程式为_________________________________
(3)除去C中过量的H2O2,然后用0.0900mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;若用50mL滴定管进行实验,当滴定管中的液面在刻度“20”处,则管内液体的体积______(填序号)
(①=20mL,②=30mL,③<20mL,④>30mL).
(4)滴定至终点时,消耗NaOH溶液12.50mL,该葡萄酒中SO2含量为:___g/L
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素,已知:
①A原子的最外层电子数是次外层电子数的两倍,B的阴离子与C的阳离子跟氖原子的电子层结构相同,E原子的最外层上的电子数比最内层多5。
②常温下B2是气体,它的相对分子质量是氢气的16倍。
③C的单质在B2中燃烧,生成淡黄色固体F,F与AB2反应可生成B2。
④D的单质在B2中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体DB2,D在DB2中的含量为50%。根据以上情况回答:
(1)E位于第___周期___族;
(2)C的离子结构示意图是_____,F中的化学键为______;
(3)AB2的电子式为___; F和AB2反应的化学方程式为_______;
(4)C、D、E三种元素的原子半径从小到大的顺序为___; (用元素符号回答)
(5)常温下,E的单质与C的最高价氧化物对应水化物的水溶液反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①Al2O3 ![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3
Al(OH)3
②Cu2(OH)2CO3![]() CuCl2
CuCl2![]() Cu
Cu
③饱和NaCl(aq)![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④Fe2O3![]() FeCl3(aq)
FeCl3(aq) ![]() 无水FeCl3
无水FeCl3
⑤MgCl2(aq)![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO
A.①②③④B.①②③⑤C.②④⑤D.①④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com