
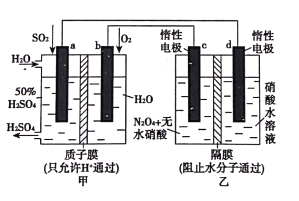
【题目】利用膜技术原理和电化学原理制备少量硫酸和绿色硝化剂N2O5,装置如图所示,下列说法正确的是( )
A.b电极反应式是O2+4e-+2H2O=4OH-
B.甲中每消耗l mol SO2,a电极附近溶液H+增加2mol
C.c电极反应式是N2O4-2e-+H2O=N2O5+2H+
D.甲、乙装置中分别生成的硫酸和N2O5的物质的量相等
【答案】B
【解析】
甲装置能自发的进行氧化还原反应且没有外接电源,所以是原电池,a极上二氧化硫失电子为负极,b上氧气得电子为正极,乙属于电解池,与电源的正极b相连的电极c为阳极,N2O4在阳极失电子生成N2O5,d为阴极,阴极上氢离子得电子生成氢气,据此分析。
A. 电极a为负极,电极b为正极,正极发生还原反应,O2+4e-+4H+=2H2O,电解液是硫酸,不能出现氢氧根离子,故A错误;
B.依据电子转移数相同可知,甲装置的a电极的电极反应式: SO2-2e+2H2O=4H++SO42-, b电极的电极反应为O2+4e-+4H+=2H2O,总反应为2SO2 + O2 +2H2O=2H2SO4,可知消耗1mol二氧化硫时,甲中每消耗l mol SO2,a电极附近溶液H+增加2 mol,故B正确;
C.c是阳极,d是阴极,阳极上N2O4放电生成N2O5,电极反应为![]() ,故C错误;
,故C错误;
D. 依据电子转移数相同可知,甲装置的左侧的电极反应式: SO2-2e-+2H2O=4H++SO42-, 可知电子转移数为2mole~时,生成1mol硫酸,乙装置中阳极N2O4-2e-+2HNO3=2N2O5+2H+,转移电子的物质的量为2mole~时,生成2mol五氧化二氮,转移相同电子数时,生成硫酸和五氧化二氮的物质的量为1:2,故D错误;
答案选B。


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
【题目】如下图所示,利用海水可提取很多重要的化工原料。
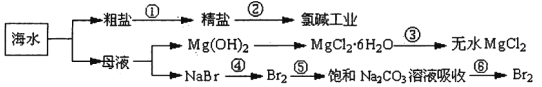
下列有关说法正确的是.( )。
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.第②步中工业上可采用石墨为阴极,铁为阳极,采用阳离子交换膜的电解装置
C.第③步中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2
D.在第④步中溴元素被氧化,第⑤、⑥步中既有溴元素被氧化也有溴元素被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是

A.反应的化学方程式:CO+2H2CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,(CO)=0.075mol/(L·min1)
D.反应至3分钟,用甲醇来表示反应的平均速率为![]() mol/(L·min1)
mol/(L·min1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物中间体Q、医用材料PVA的合成路线如图。
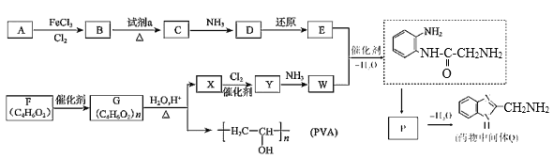
已知:①R-Cl+2NH3→R-NH2+NH4Cl
②R-NO2![]() R-NH2
R-NH2
③-NH2+![]()
(1)A的分子式是________。
(2)B→C是硝化反应,试剂a是________(填名称)。
(3)C→D转化的化学方程式是________。
(4)E的结构简式是________。
(5)F含有的官能团是________(填名称),与其含有相同官能团的同分异构体还有________种。
(6)G→X的化学方程式是________。
(7)W能发生缩聚反应,形成的高分子结构简式是________。
(8)P的结构简式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质X的结构简式如图所示,它常用于制香料或作为饮料酸化剂,在医学上也有广泛用途。下列关于物质X的说法正确的是( )
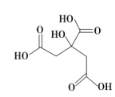
A.X的分子式为C6H7O7
B.X分子内所有原子均在同一平面内
C.1mol物质X最多可以和3mol氢气发生加成反应
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关甲、乙、丙、丁四个图示的叙述正确的是( )

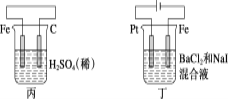
A.甲中负极反应式为2H++2e-=H2↑
B.乙中阳极反应式为Ag++e-=Ag
C.丙中H+向碳棒方向移动
D.丁中电解开始时阳极产生黄绿色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】泡沫灭火器在灭火时能喷射出大量二氧化碳及泡沫,它们能粘附在可燃物上,使可燃物与空气隔绝,达到灭火的目的。泡沫灭火器内有两个容器,分别盛放两种液体,它们是硫酸铝和碳酸氢钠溶液,两种溶液互不接触,不发生任何化学反应。(平时千万不能碰倒泡沫灭火器)当需要灭火时,把灭火球倒立,两种溶液混合在一起,就会产生大量的二氧化碳气体。
完成下列填空:
①泡沫灭火器的反应_____________________。
②钠和铝的金属性较强的是_______________。
③二氧化碳是_____________化合物。(选填“离子”或“共价”)
④苏打水中含有碳酸氢钠,碳酸氢钠是__________________电解质。(选填“强”或“弱”) 。
⑤硫酸铝溶液呈_____________性(选填“酸”、“碱”或“中”),氢氧化铝受热分解,生成___________和水。
⑥含氢氧化铝的药物可用于治疗胃酸过多,解释其原因_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 将过量的氨水加入到CuSO4溶液中,最终得到蓝色沉淀
B. 由于氢键的作用,H2O的稳定性强于H2S
C. 在核电荷数为26的元素原子核外价电子排布图为![]()
D. 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.Cl2通入水中:Cl2+H2O=2H++Cl-+ClO-
B.向FeCl3溶液中加入铁粉:Fe3++Fe=2Fe2+
C.向澄清石灰水中通入CO2:2OH-+CO2=CO32-+H2O
D.向稀HNO3溶液中加入少量铜粉:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com