
【题目】如图所示,在一个密闭的玻璃管两端各放一团棉花,再用注射器同时在两端注入适量的浓氨水和浓盐酸,下列说法不正确的是( )
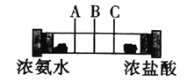
A.玻璃管中发生的反应可表示为:NH3+HCl=NH4Cl
B.用手触摸玻璃管外壁,会感觉到有热量放出
C.实验时会在玻璃管的B处附近看到白雾
D.将浓盐酸换成浓硝酸也会有相似现象
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】以玉米(主要成分是淀粉)为原料制备乙醇的流程如下:

下列说法中不正确的是
A. C12H22O11属于二糖
B. 1mol葡萄糖分解成3mol乙醇
C. 可用碘水检验淀粉是否完全水解
D. 可采取蒸馏的方法初步分离乙醇和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式的为( )
A.向FeI2溶液中通入少量的氯气:Cl2+2Fe2+=2Fe3++2Cl-
B.光导纤维遇碱性土壤“短路”:SiO2+2OH-=SiO32-+H2O
C.电解MgCl2溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.向明矾溶液中加入Ba(OH)2使Al3+刚好沉淀完全:Al3++3OH-=Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、_________________、_______
(2)实验时大烧杯上若不加盖板,求得中和热![]() 的数值__________
的数值__________![]() 填“偏大”“偏小”或“无影响”
填“偏大”“偏小”或“无影响”![]() 。
。
(3)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如右表所示。
![]() 设充分反应后溶液的比热容
设充分反应后溶液的比热容![]() ,忽略实验仪器的比热容及溶液体积的变化,则
,忽略实验仪器的比热容及溶液体积的变化,则![]() ____________________;
____________________;![]() ____________________。
____________________。![]() 已知溶液密度均为
已知溶液密度均为![]()
![]() 原因是_____________________________________________________________。
原因是_____________________________________________________________。
反应物 | 起始温度 | 终了温度 | 中和热 |
A. |
|
|
|
B. |
|
|
|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某香料F的合成路径如图所示![]() 部分产物略去
部分产物略去![]() 。
。

已知:①同一个碳原子上连接有两个羟基时不稳定,会自动脱水
②![]()
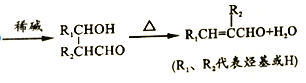
请回答下列问题:
![]()
![]() 的系统命名为______;A的结构简式为___________。
的系统命名为______;A的结构简式为___________。
![]() 含有的官能团名称是 ______________。
含有的官能团名称是 ______________。
![]() 写出步骤III第①步反应的化学方程式_____________;反应Ⅱ的反应类型为_____。
写出步骤III第①步反应的化学方程式_____________;反应Ⅱ的反应类型为_____。
![]() 在引发剂作用下,D可以缩聚合成高聚物,其化学方程式____________________。
在引发剂作用下,D可以缩聚合成高聚物,其化学方程式____________________。
![]() 物质G的化学式为
物质G的化学式为![]() ,同时满足下列条件的G的同分异构体有_____
,同时满足下列条件的G的同分异构体有_____![]() 写结构简式
写结构简式![]() 。
。
①核磁共振氢谱显示苯环上有四种不同的氢
②常温下,能与![]() 溶液反应产生气体
溶液反应产生气体
③遇氯化铁溶液会显色
![]() 结合上述合成方法,以乙醇为原料,无机试剂任选,设计合成聚
结合上述合成方法,以乙醇为原料,无机试剂任选,设计合成聚![]() 丁烯醛
丁烯醛![]() 的线路图:__________________________________________________。合成路线示例如下:CH2=CH2
的线路图:__________________________________________________。合成路线示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
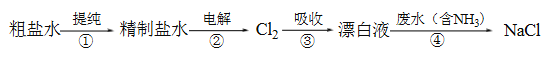
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下发生反应:4NO2(g)+O2(g)![]() 2N2O5(g) ΔH<0,T1时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如表所示。
2N2O5(g) ΔH<0,T1时,向体积为2L的恒容密闭容器中通入NO2和O2,部分实验数据如表所示。
时间/s | 0 | 5 | 10 | 15 |
c(NO2)/(mol·L-1) | 4.00 | 2.52 | 2.00 | c3 |
c(O2)/(mol·L-1) | 1.00 | c1 | c2 | 0.50 |
(1)0~10s内N2O5的平均反应速率为__ ,此温度下的平衡常数为___。
(2)其他条件不变,将容器体积压缩一半,则重新达到平衡时c(N2O5)___2.00mol·L-1(填“>、<或=”,下同)
(3)假设温度T1时平衡常数为K1,温度T2时平衡常数为K2,若K1<K2,则T1____T2。
(4)下列可以作为平衡的依据的是___
A.容器内混合气体的颜色不再改变
B.生成1molO2的同时消耗2molN2O5
C.混合气体的平均摩尔质量不再变化
D.混合气体的密度不再变化
(5)改变哪些措施可以增加NO2的平衡转化率___(答出任意两条及以上)
(6)已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ·mol1
2C(s)+O2(g)=2CO(g) ΔH=﹣221.0 kJ·mol1
C(s)+O2(g)=CO2(g) ΔH=﹣393.5 kJ·mol1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=___ kJ·mol1,利于该反应自发进行的条件是___(选填“高温”或“低温”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g) △H=-a kJ·mol-1已知:下列说法正确的是( )
2HI(g) △H=-a kJ·mol-1已知:下列说法正确的是( )

A.H2、I2和HI分子中的化学键都是非极性共价键
B.相同条件下,1 mol H2(g)和1 mol I2(g)的总能量小于2 mol HI(g)的总能量
C.断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ
D.向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g)![]() 4C(g)+2D(g),在不同条件下反应,其平均反应速率v(X)如下,其中反应速率最快的是 ( )
4C(g)+2D(g),在不同条件下反应,其平均反应速率v(X)如下,其中反应速率最快的是 ( )
A.v(A)=0.4mol/(L·s)B.v(B)=0.8mol/(L·s)C.v(C)=1.2mol/(L·s)D.v(D)=0.7mol/(L·s)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com