
����Ŀ����.��ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+���ӹ�ҵ��ˮ�л������������ͽ���ͭ�Ĺ���������ͼ��ʾ��
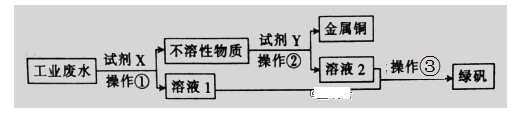
��1�������۵�����Ϊ__________ ��
��2���Լ�XΪ__________���ѧʽ�����������漰�����ӷ�Ӧ����ʽΪ__________ ��
��3���о����������ֺ���Ʒ��Ϻ��з��ĵ�õȣ����ں���+5 ���飨As��Ԫ�أ����������������ģ���˪�ijɷ��� As2O3�����綾���ʣ�ר���Ҹ棺�Է�ʱ��Ҫͬʱ����ʳ�ú��ʺ���ˣ����������ж�����������һ����ʽ����������+����ά���� C=��˪����ʹ���ж�������ά���� C ��________��������������������ԭ����
��4����֪ij��Ӧ�з�Ӧ����������У�KMnO4��H2SO4��MnSO4��H2C2O4��K2SO4��H2O��һ��δ֪��X��
����0.5 molH2C2O4�ڷ�Ӧ��ʧȥ1 mol��������X����X�Ļ�ѧʽΪ__________ ��
�ڽ��������ͻ�ԭ������ƽ��ϵ���������з����У����õ����ű������ת�Ƶķ���� ��Ŀ��__________
![]()
������֪H2C2O4Ϊ���ᣬ��д���÷�Ӧ�����ӷ���ʽ��__________
���𰸡���ȴ�ᾧ Fe Fe + 2H+ = Fe2+ + H2�� ��ԭ�� CO2 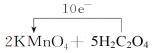 2 MnO4- +5 H2C2O4+6H+ = 2Mn2+ +10 CO2��+8H2O
2 MnO4- +5 H2C2O4+6H+ = 2Mn2+ +10 CO2��+8H2O
��������
��.��ҵ��ˮ�м�����������ۣ�����Cu2+��Ӧ���û���Cu��ʣ����ҺΪ����������Һ���ᾧ��ɵ��̷���
��3������Ʒ���ں���+5 ���飬�븻��ά���� C��ʳ��ͬʳ���ɷ���������ԭ��Ӧ��ά����C�ɽ�+5�۵��黹ԭΪ+3�ۣ�
��4����Ӧ��H2C2O4ʧȥ���ӣ�����CԪ�ػ��ϼ۴�+3�����ߵ�+4�ۣ�����Ӧ���֪X�к���CԪ�أ��һ��ϼ�Ϊ+4�ۣ�������ԭ��Ӧ��MnԪ�ػ��ϼ۽��ͣ���˸�������ԭ��Ӧ�ķ�Ӧ��ΪKMnO4��H2SO4��H2C2O4��������ΪMnSO4��K2SO4��H2O��һ��δ֪��X�����ݻ��ϼ������غ㡢ԭ���غ��д����Ӧ����ʽΪ��2KMnO4 +5 H2C2O4+3H2SO4 = 2MnSO4 +10 CO2��+8H2O���ݴ˷�������
��.��1���ɷ�����֪������Ϊ��ȴ�ᾧ��
��2���Լ�XΪ���ۣ������ķ�ӦΪFe+Cu2+=Cu+Fe2+����������������ϡ���ᷴӦ���ɵõ�����������Һ����˲����ڵķ�ӦΪFe + 2H+ = Fe2+ + H2����
��3��ά����C�ɽ�+5�۵��黹ԭΪ+3�ۣ��ڷ�Ӧ������ԭ����
��4���ٸ��ݷ�����֪X�Ļ�ѧʽΪCO2��
�ڸ÷�Ӧ����������KMnO4����ԭ����H2C2O4�������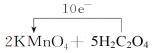 ��
��
�۷�Ӧ����ʽΪ��2KMnO4 +5 H2C2O4+3H2SO4 = 2MnSO4 +10 CO2��+8H2O�������ӷ���ʽΪ��2MnO4- +5H2C2O4+6H+ = 2Mn2+ +10 CO2��+8H2O��


 �߽�������ϵ�д�
�߽�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ⶨij����ϡ����Ʒ�з�Ԫ�ص�����������������ʵ�顣���ø����ᣨ�߷е��ᣩ����Ʒ�еķ�Ԫ��ת��Ϊ�����⣨�ͷе��ᣩ��������ͨ���ζ�������ʵ��װ����ͼ��ʾ��

��1��c��������________________
��2�����װ�������ԣ���b��f�м�ˮ��ˮ��û����a��eĩ�ˣ�______________����������裩����c������ƿf������ð��������a���γ�һ��ˮ����ֹͣ���ȣ�_________________________��˵��װ�����������á�
��3��c�м���һ������������m g����ϡ����Ʒ��f��ʢ�еμӷ�̪��NaOH��Һ������b��c��ʹˮ��������c��
����c��ͨˮ������Ŀ����________________________________��
��c�г���HF�����⣬���ܻ�������SiF4(��ˮ��)�������ɣ�����SiF4���ɣ�ʵ������__________(����ƫ������ƫ������������Ӱ����)��
�����۲쵽f����Һ��ɫ��ȥ����Ҫ��f�м�ʱ����NaOH��Һ�������ʹʵ����ƫ�ͣ�ԭ��_______________________________��
��4�������Һ�м���V1ml c1 mol��L-1La(NO3)3��Һ���õ�LaF3����������c2 mol��L-1 EDTA����Һ�ζ�ʣ���La3+��La3+��EDTA��1:1��ϣ�������EDTA����ҺV2 mL�������ϡ����Ʒ�з�����������Ϊ____________(д������ʽ���ɣ����軯��
��5������Ʒ����ʵ��ǰ����Ҫ��0.084g�����ƴ�����Ʒ����ʵ�飬�ı���������������������Ӧ�¶ȡ�����ʵ�飩���������������Ԫ���������ظ���Ρ��ò�����Ŀ����_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʵ���ǻ�ѧѧϰ����Ҫ���ݡ����������յ�֪ʶ������������ݡ�
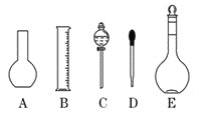
(1)ʵ������Ҫ0.1 mol/L NaOH��Һ480 mL�� ������Һ����������ش��������⣺
����ͼ��ʾ��������������Һ�϶�����Ҫ����________(�����)��
���ɼ����֪��Ӧѡ��________mL������ƿ����������ƽ��ȡ________g NaOH��
��������NaOH��Һʵ���У�������������ȷ��������ʱ���ӿ̶��ߣ� ����������ҺŨ��________0.1 mol/L (����������������������С��������ͬ)���ܽ�NaOH�����Һ����ȴ�����º���ת��������ƿ�С�������ת�ƻ�ʹ��������ҺŨ��________0.1 mol/L��
(2)ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϡ�
A.��ȡ��Һ B.���� C.�����ᾧ D.���� E.���� F.��Һ
�ٳ�ȥϴ��ˮ��IJ�Ҷ�Ӻ�����________��
�ڴ�ʳ��ˮ����ʳ�ι���________��
�۴ӵ��ɳ�ӻ�����л�õ�________��
�ܴ���ˮ�л����________��
�ݷ���CCl4 �е�Ϊ76.75��ͼױ��е�Ϊ110.6��Ļ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ɫ��������A������KCl��CaCO3��Na2CO3��Na2SiO3��CuSO4�еļ��֣����³�ѹ�½�������ʵ�顣

�����ƶ�����ȷ����
A. ��ɫ��ҺB��pH��7
B. ��ɫ����F����Ҫ�ɷ���H2SiO3
C. �����A����Na2SiO3��CuSO4��CaCO3
D. ����ɫ��ҺB�м�HNO3�ữ���������ٵμ�AgNO3�����а�ɫ�������ɣ�˵�������A����KCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(22Ti)��������������ܱ���Ϊ��δ�����͵Ľ���������������Ҫ�ɷ�ΪFeTiO3����������MgO��SiO2�����ʣ���Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ����������������Ʊ��������������£�
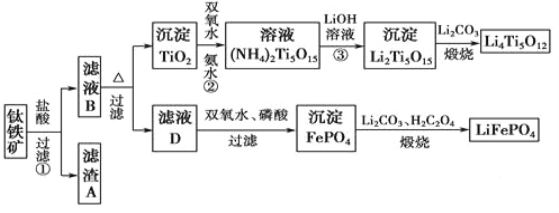
(1)Tiλ��Ԫ�����ڱ��е�λ��Ϊ________����������Ԥ����ʱ��Ҫ���з��飬��ԭ����_______��
(2)���̢��У����Ľ����ʽ����ͼ��ʾ����ͼ��֪�������Ľ�����Ϊ80%ʱ�������õ�ʵ��������_________��
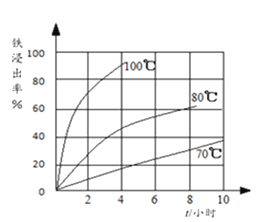
(3)���̢��й���TiO2��˫��ˮ����ˮ��Ӧת����(NH4)2Ti5O15��Һʱ��TiԪ�صĽ������뷴Ӧ�¶ȵĹ�ϵ��ͼ��ʾ����Ӧ�¶ȹ���ʱ��TiԪ�ؽ������½���ԭ����___________��

(4)д������ҺD����FePO4�����ӷ���ʽ____________________________________��
(5)������ͼ��֪FePO4�Ʊ�LiFePO4�Ļ�ѧ����ʽ��_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǹ�ˮ����[Cr(CH3COO)2]2��2H2O(Ħ������376g/mol)��һ���������ռ�������ɫ���壬�ױ����������������ᣬ�����Ҵ���������ˮ�����ѡ����Ʊ�װ��(��ʡ�Լ��ȼ�֧��װ��)�Ͳ�������:
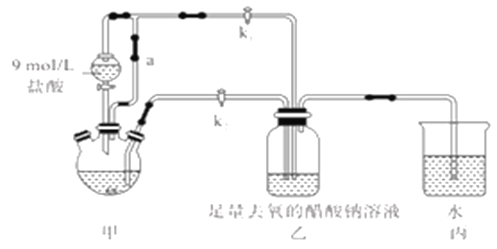
�ټ��װ��������,��������ƿ�����μ������п�ۣ�200mL0.200mol/LCrC13��Һ��
�ڹر�k2��k1,������Һ©�������������ƺõ��١�
�۴�������ƿ�ȵ���Һ������ɫ(Cr3+)��Ϊ����ɫ(Cr2+)ʱ������Һת�Ƶ�װ�����С������ִ�������ɫ����ʱ���رշ�Һ©����������
�ܽ�װ�����л������ٹ��ˡ�ϴ�Ӻ�������õ�11.28g[Cr(CH3COO)2]2��2H2O
��1��װ�ü�����ͨ��a��������________����μ����װ�õ��������Ƿ�����?__________��
��2�����ɺ���ɫ��������ӷ�Ӧ����ʽ____________________________��
��3�����������Һ�Զ�ת����װ�����е�ʵ�����Ϊ________________��
��4��װ�ñ���������________________��
��5��Ϊ�õ���������IJ�Ʒ��ϴ��ʱ��ʹ�õ��Ⱥ�˳��ѡ������ϴ�Ӽ�__________(�����)��
������ ������ˮ(�����ȴ) ����ˮ�Ҵ� ������
��6����ʵ����[Cr(CH3COO)2]2��2H2O�IJ�����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��A��ͨ���������ر�Bʱ��C�к�ɫ������ɫ�ޱ仯������Bʱ��C����ɫ������ɫ��ȥ��������ж���ȷ����
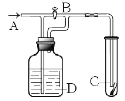
A.ͨ���Cl2����ˮ����B.D�в�������ŨH2SO4
C.D�п�����ˮD.D�п����DZ���ʳ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019����Ԫ�����ڱ�����150���ꡣ��֪X��Y��Z��W��M��Ϊ������Ԫ�ء�25��ʱ��������������Ӧ��ˮ����(Ũ�Ⱦ�Ϊ0.01mol��L-1)��Һ��pH��ԭ�Ӱ뾶�Ĺ�ϵ��ͼ��ʾ������˵������ȷ���ǣ� ��
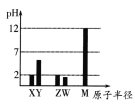
A.Y�����������Ļ�ѧʽ����ΪYO2
B.����Ԫ����ֻ��һ���ǽ���Ԫ��
C.W��M�����Ӱ뾶��С˳��W<M
D.X�������̬�⻯���Z����̬�⻯�ﷴӦ�����к������Ӽ����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̵�������Ҫ�ɷ�Ϊ�۳���������H2O��NOx������NOx����Ҫ�Ĵ�����Ⱦ��֮һ��Ϊ�˼��ij�����̵�����NOx�������ɼ���״����50.00 L�̵��������������������ͨ�������ữ��H2O2��Һ�У�ʹNOx��ȫ������ΪNO3����ȥ�����H2O2����ˮϡ����100.00 mL����ȡ20.00 mL����Һ������30.00 mL 0.01000 mol��L1FeSO4����Һ������������ַ�Ӧ����0.001000 mol��L1 K2Cr2O7����Һ�ζ����յ㣬����K2Cr2O7��Һ10.00 mL���ζ������з������·�Ӧ��
Fe2+ + NO3 + H+ �� NO�� + Fe3+ + H2O ��δ��ƽ��
![]() + Fe2+ + H+ �� Cr3+ + Fe3++ H2O ��δ��ƽ��
+ Fe2+ + H+ �� Cr3+ + Fe3++ H2O ��δ��ƽ��
��1��NO��H2O2����ΪNO3�����ӷ���ʽ��_________��
��2������100mL 0.001000 mol��L1 K2Cr2O7����Һʱ�������õ��ձ�����Ͳ���������⣬�����õ��IJ���������_________��_________��
��3����FeSO4����Һ���ֱ��ʣ���ʹNOx�����ⶨ���_________������ƫ���� ����ƫ����������Ӱ�� ������
��4����״���¸ù����̵�����NOx���ۺϳ�NO2���ĺ���Ϊ_________mg��m3��д��������̣���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com