
����Ŀ�������Ǹ�ˮ����[Cr(CH3COO)2]2��2H2O(Ħ������376g/mol)��һ���������ռ�������ɫ���壬�ױ����������������ᣬ�����Ҵ���������ˮ�����ѡ����Ʊ�װ��(��ʡ�Լ��ȼ�֧��װ��)�Ͳ�������:
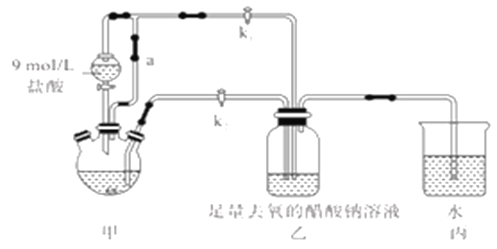
�ټ��װ��������,��������ƿ�����μ������п�ۣ�200mL0.200mol/LCrC13��Һ��
�ڹر�k2��k1,������Һ©�������������ƺõ��١�
�۴�������ƿ�ȵ���Һ������ɫ(Cr3+)��Ϊ����ɫ(Cr2+)ʱ������Һת�Ƶ�װ�����С������ִ�������ɫ����ʱ���رշ�Һ©����������
�ܽ�װ�����л������ٹ��ˡ�ϴ�Ӻ�������õ�11.28g[Cr(CH3COO)2]2��2H2O
��1��װ�ü�����ͨ��a��������________����μ����װ�õ��������Ƿ�����?__________��
��2�����ɺ���ɫ��������ӷ�Ӧ����ʽ____________________________��
��3�����������Һ�Զ�ת����װ�����е�ʵ�����Ϊ________________��
��4��װ�ñ���������________________��
��5��Ϊ�õ���������IJ�Ʒ��ϴ��ʱ��ʹ�õ��Ⱥ�˳��ѡ������ϴ�Ӽ�__________(�����)��
������ ������ˮ(�����ȴ) ����ˮ�Ҵ� ������
��6����ʵ����[Cr(CH3COO)2]2��2H2O�IJ�����______________��
���𰸡�ƽ��ѹǿ��֤��Һ©���е�Һ��˳������ �ر�k1��k2����ֹˮ�м�ס��ͨ��a����Է�Һ©����������һ��ʱ��֮��Һ©����ˮ����˳�����£������������� 2Cr2++4CH3COO��+2H2O�T[Cr(CH3COO)2]22H2O�� �ر�k1����k2 ��ֹ��������װ�����������۸� �ڢ� 75.0%
��������
����ʵ��Ŀ�ļ�ʵ����̣����ʵ��װ��ͼ�ɵã����з�����Ӧ��2CrCl3+Zn=2CrCl2+ZnCl2��Zn+2HCl=ZnCl2+H2�����������������������ѹǿ��ʹ���з�Ӧ�����Һ�������У�������Ӧ��2CrCl2+4CH3COONa+2H2O�T[Cr(CH3COO)2]22H2O��+4NaCl��Ȼ����ˡ�ϴ��������õ�[Cr(CH3COO)2]22H2O���塣
��1��������ƿ���Һ©��֮������ͨ��a���ӣ����������������ƿʱ��ʼ�ձ���������ƿ���Һ©����ѹǿ��ȣ���ƽ��ѹǿ�����ã��Ա�֤��Һ©���е�Һ��˳�����¡����װ�������Ե�ԭ��ͨ�������װ�ò�ͬ��λ�������ѹǿ������������������Լ����װ�õ������Եķ�������Ϊ���ر�k1��k2����ֹˮ�м�ס��ͨ��a����Է�Һ©����������һ��ʱ��֮��Һ©����ˮ����˳�����£���������������
��2������ɫ������CrCl2��CH3COONa��Һ��Ӧ���ɵ�[Cr(CH3COO)2]2��2H2O�����ӷ���ʽΪ��2Cr2++4CH3COO-+2H2O=[Cr(CH3COO)2]22H2O����
��3����ʵ���������������������ѹǿ��ʹ���з�Ӧ�����Һ�������У�������Ӧ���ɴ����Ǹ�ˮ����[Cr(CH3COO)2]2��2H2O�����Բ��������Һ�Զ�ת����װ�����е�ʵ�����Ϊ���ر�k1����k2��
��4�������Ǹ�ˮ����[Cr(CH3COO)2]2��2H2O�ױ�����������ֱ�ӺͿ����Ӵ�������װ�ñ�������������ֹ��������װ�����������۸���
��5����Ϊ�����Ǹ�ˮ�������������ᣬ�����Ҵ���������ˮ�����ѣ�����ϴ�Ӳ�Ʒ������������Ҵ�������ˮϴȥ��������ӣ���������ϴȥ�����ˮ������ϴ��ʱ��ʹ�õ��Ⱥ�˳��Ϊ���ڢ���
��6��CrC13�����ʵ���Ϊ��0.2L��0.200mol/L=0.04mol������Crԭ���غ㣬[Cr(CH3COO)2]2��2H2O�����۲���Ϊ��376g/mol��0.04mol=15.04g������Ϊʵ�ʲ���Ϊ11.28g�����Ա�ʵ����[Cr(CH3COO)2]2��2H2O�IJ�������11.28g��15.04g��100%=75.0%��


 ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڡ�ͬλ�ء�����ͬ�������塱����ͬϵ�����ͬ���칹�塱��˵���������� ��������
A. ͬλ����ָ��������ͬ����������ͬ��ͬ��Ԫ�صIJ�ͬԭ��
B. ͬ����������ָ��ͬ��Ԫ���γɵIJ�ͬ����
C. ��Ϊͬ���칹����������ʷ���ʽ��ͬ����ѧ����һ������
D. ������ͬ��ͨʽ�������������ɸ���![]() ��ԭ���ŵ��л���һ����Ϊͬϵ��
��ԭ���ŵ��л���һ����Ϊͬϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ2A(g)![]() 2Y(g) + E(g)��H>0�ﵽƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ�ǣ� ��
2Y(g) + E(g)��H>0�ﵽƽ��ʱ��Ҫʹ����Ӧ���ʽ��ͣ�A��Ũ������Ӧ��ȡ�Ĵ�ʩ�ǣ� ��
A.��ѹB.��ѹC.��СE��Ũ��D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������

��1����ˮ�������ɺ�ˮ��õ�ˮ�ij��÷���֮һ����ʵ���������һ������װ�ÿ϶� ��Ҫ���������е�һ���֣�����ʵ���������µ��ϡ������ҵ�˳��������__________ ������ţ���������������ˮӦ��________������a������b�����ڽ��롣
��2���������������ʾ����������Եõ���ˮ�����ӵ�ˮ����ȡ�⣬��Ҫ�������� �е�______������ţ�������������Ϊ__________����õ�ˮ�м������Ȼ�̼����ȡ�� ���ʵ�ʵ���������_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.��ҵ��ˮ�к��д�����FeSO4���϶��Cu2+��������Na+���ӹ�ҵ��ˮ�л������������ͽ���ͭ�Ĺ���������ͼ��ʾ��
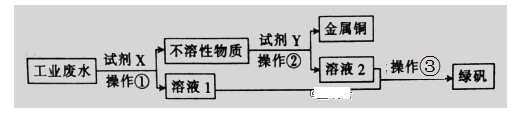
��1�������۵�����Ϊ__________ ��
��2���Լ�XΪ__________���ѧʽ�����������漰�����ӷ�Ӧ����ʽΪ__________ ��
��3���о����������ֺ���Ʒ��Ϻ��з��ĵ�õȣ����ں���+5 ���飨As��Ԫ�أ����������������ģ���˪�ijɷ��� As2O3�����綾���ʣ�ר���Ҹ棺�Է�ʱ��Ҫͬʱ����ʳ�ú��ʺ���ˣ����������ж�����������һ����ʽ����������+����ά���� C=��˪����ʹ���ж�������ά���� C ��________��������������������ԭ����
��4����֪ij��Ӧ�з�Ӧ����������У�KMnO4��H2SO4��MnSO4��H2C2O4��K2SO4��H2O��һ��δ֪��X��
����0.5 molH2C2O4�ڷ�Ӧ��ʧȥ1 mol��������X����X�Ļ�ѧʽΪ__________ ��
�ڽ��������ͻ�ԭ������ƽ��ϵ���������з����У����õ����ű������ת�Ƶķ���� ��Ŀ��__________
![]()
������֪H2C2O4Ϊ���ᣬ��д���÷�Ӧ�����ӷ���ʽ��__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ��ж����ڵ�һ���֡���֪AԪ��ԭ�ӵ�����������������Ӳ�����3�����ࡣ���й��ڱ�������Ԫ�ص�˵����ȷ���� (����)
A. X�ĵ����ڿ����п���ȼ��
B. X��Y��Z����Ԫ����YԪ���γɵĵ��������Ӱ뾶���
C. ����������Ӧ��ˮ����������ǿ����AԪ��
D. A����ͨ��NaZ��Һ�У����ݷ�Ӧ�����֤��A��Z�ǽ����Ե����ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к��нϴ�����Cl����![]() ��OH����3�������ӣ����ֻȡһ�θ���Һ���ܹ��ֱ�3�����������μ������������ʵ�����˳����ȷ���ǣ�������
��OH����3�������ӣ����ֻȡһ�θ���Һ���ܹ��ֱ�3�����������μ������������ʵ�����˳����ȷ���ǣ�������
�ٵμ�Mg��NO3��2��Һ���ڹ��ˣ��۵μ�AgNO3��Һ���ܵμ�Ba(NO3)2��Һ
A.�٢ڢܢڢ�B.�ܢڢ٢ڢ�C.�٢ڢۢڢ�D.�ܢڢۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к��нϴ�����Cl����![]() ��OH����3�������ӣ����ֻȡһ�θ���Һ���ܹ��ֱ�3�����������μ������������ʵ�����˳����ȷ���ǣ�������
��OH����3�������ӣ����ֻȡһ�θ���Һ���ܹ��ֱ�3�����������μ������������ʵ�����˳����ȷ���ǣ�������
�ٵμ�Mg��NO3��2��Һ���ڹ��ˣ��۵μ�AgNO3��Һ���ܵμ�Ba(NO3)2��Һ
A.�٢ڢܢڢ�B.�ܢڢ٢ڢ�C.�٢ڢۢڢ�D.�ܢڢۢڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̽���������������ԣ������˵��Լ��ǣ�������
A.AlCl3����ˮ��ϡ����B.![]() ����ˮ��ϡ����
����ˮ��ϡ����
C.Al��NaOH��Һ��ϡ����D.![]() ��Һ��NaOH��Һ��ϡ����
��Һ��NaOH��Һ��ϡ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com