
| A、实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B、用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 |
| C、氯离子存在时铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中 |
| D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液都出现沉淀,表明二者均可使蛋白质变性 |
| ||
| 170℃ |


科目:高中化学 来源: 题型:
| A、实验室将Na2SO3溶液直接加热蒸发结晶可得到Na2SO3晶体 |
| B、用湿润的pH试纸来检验溶液的pH值 |
| C、用KSCN溶液检验硫酸亚铁溶液是否氧化变质 |
| D、用四氯化碳萃取溴的苯溶液中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甘油 | B、吗啡 | C、冰毒 | D、海洛因 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳的燃烧热大于110.5 kJ/mol |
| B、①的反应热为221 kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物不是强碱 |
| D、XW2分子中各原子最外层电子均达到电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发掉0.5L水 |
| B、标况下通入44.8L HCl气体 |
| C、将溶液加热蒸发浓缩至0.5L |
| D、加入10mol/L盐酸0.6L,再将溶液稀释至2L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 180℃ |
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CO2的电子式 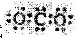 | ||
B、Cl-的结构示意图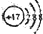 | ||
| C、H216O、D216O、H218O、D216O互为同素异形体 | ||
D、质量数为37的氯原子
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com