
【题目】研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义。
(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
①CO(g)+NO2(g)=NO(g)+CO2(g) △H=-a KJ·mol-1 (a>0)
②2CO(g)+2NO(g)=N2(g)+2CO2(g) △H=-b KJ·mol-1 (b>0)
若用标准状况下3.36LNO2氧化CO至CO2(NO2完全反应)的整个过程中转移电子的物质的量为_____mol,放出的热量为_________ kJ(用含有a和b的代数式表示)。
(2)己知下列反应的反应热:
①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) △H=-870.3kJ/mo1
②C(s)+O2(g) =CO2(g) ΔH=-393.5kJ/mo1
③2C(s)+2H2(g)+O2(g) =CH3COOH(1) ΔH=-488.3kJ/mo1
请写出H2燃烧热的热化学方程式______________________________________。
(3)在101kPa下,CH4(g)、H2(g)、C(s) 的燃烧热分别为890.3kJ/mol、285.8kJ/mol 和393.5kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式_______________________________。
【答案】 0.6 -3/40(2a+b) H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJmol-1 CH4(g)=C(s)+2H2(g) △H=+74.8kJmol-1
【解析】(1) NO2氧化CO至CO2,氮元素化合价由+4价变为0价,n(e-)=![]() ×4=0.6 mol;已知:①CO(g)+NO2(g)=NO(g)+CO2(g)△H1=-a KJ·mol-1(a>0),②2CO(g)+2NO(g)=N2(g)+2CO2(g)△H2=-b KJ·mol-1(b>0),根据盖斯定律,由①×2+②得反应4CO(g)+2 NO2(g)= N2(g)+4 CO2(g) ΔH=-2a-b kJ·mol-1;
×4=0.6 mol;已知:①CO(g)+NO2(g)=NO(g)+CO2(g)△H1=-a KJ·mol-1(a>0),②2CO(g)+2NO(g)=N2(g)+2CO2(g)△H2=-b KJ·mol-1(b>0),根据盖斯定律,由①×2+②得反应4CO(g)+2 NO2(g)= N2(g)+4 CO2(g) ΔH=-2a-b kJ·mol-1;
4CO(g)+2NO2(g)= N2(g)+4CO2(g) ΔH=-2a-b kJ·mol-1;
2 mol -2a-b
0.15 mol x
x=![]() kJ·mol-1=-
kJ·mol-1=-![]() kJ·mol-1,故放热
kJ·mol-1,故放热![]() kJ;
kJ;
(2) 己知:①CH3COOH(1)+2O2(g)=2CO2(g)+2H2O(1) △H1=-870.3kJ/mo1;②C(s)+O2(g) =CO2(g) ΔH2=-393.5kJ/mo1;③2C(s)+2H2(g)+O2(g) =CH3COOH(1) ΔH3=-488.3kJ/mo1;根据盖斯定律,由![]() ×③-②+①得反应H2(g)+
×③-②+①得反应H2(g)+![]() O2(g)=H2O(l) △H=
O2(g)=H2O(l) △H=![]() ×ΔH3-ΔH2+ΔH1=
×ΔH3-ΔH2+ΔH1=![]() ×(-488.3kJ/mo1)-(-393.5kJ/mo1)+(-870.3kJ/mo1)=-285.8kJmol-1,故H2燃烧热的热化学方程式为H2(g)+
×(-488.3kJ/mo1)-(-393.5kJ/mo1)+(-870.3kJ/mo1)=-285.8kJmol-1,故H2燃烧热的热化学方程式为H2(g)+![]() O2(g)=H2O(l) △H=-285.8kJmol-1;(3)实验测得碳单质、氢气、甲烷的燃烧热(△H)分别为-393.5kJ/mol、-285.8kJ/mol、-890.3kJ/mol,则它们的热化学反应方程式分别为:①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol;②H2(g)+
O2(g)=H2O(l) △H=-285.8kJmol-1;(3)实验测得碳单质、氢气、甲烷的燃烧热(△H)分别为-393.5kJ/mol、-285.8kJ/mol、-890.3kJ/mol,则它们的热化学反应方程式分别为:①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol;②H2(g)+![]() O2(g)═H2O(l)△H=-285.8kJ/mol;③CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ/mol;根据盖斯定律,由①+②×2-③得,C(s)+2H2(g)=CH4(g),△H=[(-393.5kJ/mol)+(-285.8kJ/mol)×2]-(-890.3kJ/mol)=-74.8kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式为:CH4(g)=C(s)+2H2(g) △H=+74.8kJmol-1。
O2(g)═H2O(l)△H=-285.8kJ/mol;③CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ/mol;根据盖斯定律,由①+②×2-③得,C(s)+2H2(g)=CH4(g),△H=[(-393.5kJ/mol)+(-285.8kJ/mol)×2]-(-890.3kJ/mol)=-74.8kJ/mol,则CH4(g)分解为H2(g)、C(s)的热化学方程式为:CH4(g)=C(s)+2H2(g) △H=+74.8kJmol-1。


科目:高中化学 来源: 题型:
【题目】下列保存试剂的方法中,错误的是( )
A.漂粉精保存在烧杯中B.新制的氯水保存在棕色瓶中,避光
C.氢氧化钠溶液保存在带木塞的试剂瓶D.碘单质保存在棕色瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
①3He和4He是同位素 ②金属性:K>Ca>Mg>Be
③四氯化碳的电子式:![]() ④离子键就是阴、阳离子的静电引力
④离子键就是阴、阳离子的静电引力
⑤通常活泼金属与活泼非金属元素形成离子化合物
⑥NaHSO4在熔融状态下电离,破坏了离子键和共价键
⑦用电子式表示溴化氢的形成过程为:![]()
A. ①④⑥ B. ④⑤⑥ C. ③④⑥⑦ D. 全部都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
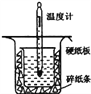
(1)从如图实验装置看,其中尚缺少的一种玻璃用品是___________________。
(2)若改用60mL 0.25 molL-1H2SO4和50mL 0.55molL-1NaOH溶液进行反应与上述实验相比,所放出的热量_____________(填“相等”“不相等”),若实验操作均正确,则所求中和热______(填“相等”“不相等”)
(3) 写出稀盐酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol):_____________________________________。
(4)某学生实验记录数据如下:
实验 | 起始温度t1/℃ | 终止温度t2/℃ | |
序号 | 硫酸 | 氢氧化钠溶液 | 混合溶液 |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热△H=__________(结果保留一位小数)。
(5)上述实验数值结果与57.3kJ/mol 有偏差,产生偏差的原因可能是________________________。
a.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
b.量取盐酸的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.实验装置保温、隔热效果差
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.物质在溶解时,若达到饱和状态,则该物质不再溶解
B.晶体失去结晶水,一定是风化的结果
C.从饱和溶液中结晶析出的晶体都含有结晶水
D.某饱和溶液冷却而析出晶体后,该溶液仍为饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列四组实验,不能得到相应实验结论的是
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓硫酸 | Na2SO3 | 酸性KMnO4溶液变浅 | SO2有还原性 | |
B | 浓盐酸 | KMnO4 | FeBr2溶液变为黄色 | 氧化性:Cl2 >Br2 | |
C | 稀硫酸 | 碳酸钠 | CaCl2溶液无明显变化 | CO2不与CaCl2反应 | |
D | 浓硫酸 | 蔗糖 | 溴水褪色 | 浓硫酸具有脱水性、强氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为 ![]() Fe2O3(s)+CO(g)=
Fe2O3(s)+CO(g)= ![]() Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
Fe(s)+CO2(g)已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式K= , △H0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)=、CO的平衡转化率=:
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 .
A.减少Fe的量
B.增加Fe203的量
C.移出部分CO2
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com