
【题目】Ⅰ.氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。
(1)该反应中氧化剂是____________ ,氧化产物是____________。用单线桥表示反应的电子转移__________________。
(2)从反应可以看出氧化性:Cl2___________N2(填“>” “<”“=” )。若71g氯气参与反应,理论上生成N2的体积(标准状况)为_________________L(保留小数点后一位)。工作人员通过能否看到白烟判断管道是否漏气,请结合上述反应,写出生成的白烟的化学式______________。
Ⅱ.实验室现需配制100 mL 0.1mol/L的氢氧化钠溶液,请将步骤补充完整
计算可得需要氢氧化钠的质量为_____________ g。
将称量好的固体放入小烧杯中,加适量蒸馏水溶解;
将所得溶液冷却至室温后,沿玻璃棒小心转入100 mL_________(填仪器名称)
用少量蒸馏水烧杯2~3次,每次洗涤液都转入容量瓶中;
继续加蒸馏水至液面距刻度线1~2cm处,改用____________小心滴加蒸馏水至刻度线处;摇匀;装瓶,贴标签。
【答案】Cl2 N2 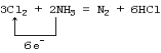 > 7.5 NH3+HCl=NH4Cl 0.4g 容量瓶 胶头滴管
> 7.5 NH3+HCl=NH4Cl 0.4g 容量瓶 胶头滴管
【解析】
Ⅰ. 由方程式可知,反应中Cl元素化合价降低被还原,Cl2为氧化剂,N元素化合价升高被氧化,NH3为还原剂,过量NH3可与HCl反应生成氯化铵,有白烟生成;
Ⅱ.配制100 mL 0.1mol/L的氢氧化钠溶液的步骤为:计算→称量→溶解、冷却→移液→定容→摇匀→装瓶→贴签,一般用天平称量(用到药匙)称量,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,转移完毕,用少量蒸馏水洗涤烧杯及玻璃棒2~3次并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,塞好瓶塞,反复上下颠倒摇匀。
Ⅰ.(1)由方程式可知,反应中Cl元素化合价降低被还原,Cl2为氧化剂,N元素化合价升高被氧化,N2是氧化产物,生成1molN2时有6mol电子转移,用单线桥表示反应的电子转移如下: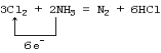 ,故答案为:Cl2;N2;
,故答案为:Cl2;N2;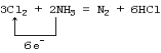 ;
;
(2)由氧化剂的氧化性强于氧化产物可知,氯气的氧化性强于氮气;由方程式可得如下关系:3Cl2—N2,则71g氯气参与反应生成标准状况下N2的体积为![]() ×
×![]() ×22.4L/mol≈7.5L;当NH3过量时,过量NH3可与HCl反应生成氯化铵,有白烟生成,反应的化学方程式为NH3+HCl=NH4Cl,故答案为:>;7.5;NH3+HCl=NH4Cl;
×22.4L/mol≈7.5L;当NH3过量时,过量NH3可与HCl反应生成氯化铵,有白烟生成,反应的化学方程式为NH3+HCl=NH4Cl,故答案为:>;7.5;NH3+HCl=NH4Cl;
Ⅱ. 100 mL 0.1mol/L氢氧化钠溶液中含有的氢氧化钠的物质的量为1mol/L×0.1L=0.1mol,则氢氧化钠的质量为40g/mol×0.1mol=4.0g;将所得溶液冷却至室温后,沿玻璃棒小心转入100 mL容量瓶中,并用玻璃棒引流;加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,故答案为:4.0;容量瓶;胶头滴管。


科目:高中化学 来源: 题型:
【题目】用含砷氧化铜矿[含CuO、Cu2(OH)2CO3、As2O3及重金属盐等]制取Cu2(OH)2SO4的工艺流程如下:
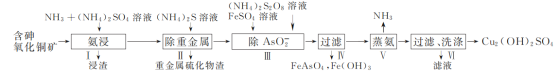
(1) 步骤Ⅰ“氨浸”时,控制温度为50~55 ℃,pH约为9.5,含铜化合物转化为[Cu(NH3)4]SO4溶液。
① CuO被浸取的离子方程式为________。
②浸取温度不宜超过55 ℃,其原因是________。
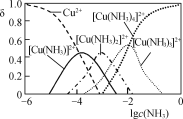
③ Cu2+与NH3结合时,溶液中含铜微粒的物质的量分布分数(δ)与溶液中游离的c(NH3)的对数值的关系如图所示。若用1 L浸取液(由等物质的量NH3和NH4+组成)将amolCu2(OH)2CO3全部浸出为[Cu(NH3)4]2+(CO32-转变为HCO3-,不考虑其他反应,溶液体积变化忽略不计),原浸取液中起始时c(NH3)应满足的条件是________。
(2) “除AsO2-”时,FeSO4需过量,一方面使AsO2-沉淀完全,另一目的是________。
(3) “蒸氨”时发生反应的化学方程式为________。
(4) 为了实现生产过程中物质循环利用,可采取的措施为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物燃料电池进行废水处理,实现碳氮联合转化。其工作原理如下图所示,其中M、N为厌氧微生物电极。
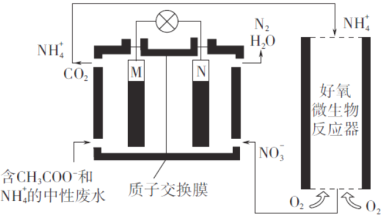
下列有关叙述错误的是
A. 负极的电极反应为CH3COO-—8e-+2H2O==2CO2↑+7H+
B. 电池工作时,H+由M极移向N极
C. 相同条件下,M、N两极生成的CO2和N2的体积之比为3:2
D. 好氧微生物反应器中发生的反应为NH3+2O2==NO3-+2H++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图所示装置,探究氯碱工业原理,下列说法正确的是

A. 石墨电极与直流电源负极相连
B. 铜电极的反应式为:2H2O+2e-![]() 2OH-+H2↑
2OH-+H2↑
C. 氢氧化钠在石墨电极附近产生, Na+ 向石墨电极迁移
D. 用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计二氧化碳熔盐捕获及电化学转化装置,其示意图如下:
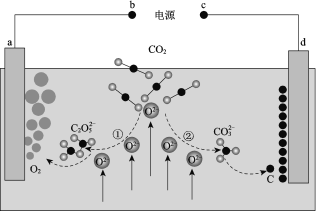
下列说法不正确的是
A. b为电源的正极
B. ①②中,捕获CO2时碳元素的化合价发生了变化
C. a极的电极反应式为2C2O52 4e == 4CO2 + O2
D. 上述装置存在反应:CO2 ===== C + O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释相关的离子方程式错误的是
A. H2S溶于水:H2S+H2O![]() HS-+H3O+
HS-+H3O+
B. 向Na2S2O3溶液中加入稀硫酸:S2O3-+2H+=S↓+SO2↑+H2O
C. NH4Cl溶液呈酸性:NH4++H2O=NH3·H2O+H+
D. K2Cr2O7溶于水:Cr2O7-+H2O![]() 2CrO42-+2H+
2CrO42-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于取代反应的是
A.CH2=CHCH3+Cl2![]() CH2=CHCH2Cl+HCl
CH2=CHCH2Cl+HCl
B. +Br2→
+Br2→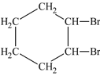
C.![]() +H2
+H2![]()
![]()
D.2CH2=CH2+O2![]() 2CH3CHO
2CH3CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S在金属离子的鉴定分析、煤化工等领域都有重要应用。请回答:
Ⅰ.工业上一种制备H2S的方法是在催化剂、高温条件下,用天然气与SO2反应,同时生成两种能参与大气循环的氧化物。
(1)该反应的化学方程式为_____________。
Ⅱ.H2S可用于检测和沉淀金属阳离子。
(2)H2S的第一步电离方程式为________。
(3)已知:25 ℃时,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27。该温度下,向浓度均为0.1 mol·L-1的CdCl2和SnCl2的混合溶液中通入H2S,当Sn2+开始沉淀时,溶液中c(Cd2+)=________(溶液体积变化忽略不计)。
Ⅲ.H2S是煤化工原料气脱硫过程的重要中间体。反应原理为
ⅰ.COS(g)+H2(g) ![]() H2S(g)+CO(g) ΔH=+7 kJ·mol-1;
H2S(g)+CO(g) ΔH=+7 kJ·mol-1;
ⅱ.CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH=-42 kJ·mol-1。
CO2(g)+H2(g) ΔH=-42 kJ·mol-1。
(4)已知:断裂1 mol分子中的化学键所需吸收的能量如表所示。
分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
能量/(kJ·mol-1) | 1 319 | 442 | x | 678 | 930 | 1 606 |
表中x=________。
(5)向10 L容积不变的密闭容器中充入1 mol COS(g)、1 mol H2(g)和1 mol H2O(g),进行上述两个反应。其他条件不变时,体系内CO的平衡体积分数与温度(T)的关系如图所示。
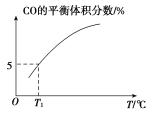
①随着温度升高,CO的平衡体积分数_____(填“增大”或“减小”)。原因为_______
②T1℃时,测得平衡时体系中COS的物质的量为0.80 mol。则该温度下,COS的平衡转化率为_____;反应ⅰ的平衡常数为_____(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分元素在周期表中的分布如图所示(虚线为金属元素与非金属元素的分界线),下列说法不正确的是

A. B只能得电子,不能失电子
B. 原子半径Ge>Si
C. As可作半导体材料
D. Po处于第六周期第VIA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com