
【题目】以NA表示阿伏加德罗常数,下列说法中正确的是( )
A. 53g碳酸钠中含NA个CO32—B. 0.1molOH—含NA电子
C. 1.8g重水(D2O)中含NA个中子D. 标准状况下11.2L臭氧(O3)中含NA个氧原子
科目:高中化学 来源: 题型:
【题目】把图2的碎纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平)。下列对该反应的说法不正确的是( )
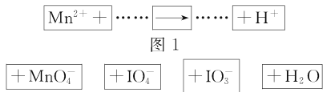
A.![]() 作氧化剂B.若有
作氧化剂B.若有![]() 参加反应转移
参加反应转移![]() 电子
电子
C.氧化剂与还原剂的物质的量之比为5∶2D.配平后![]() 、
、![]() 的化学计量数分别为2、3
的化学计量数分别为2、3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是以有机物A合成聚酯类高分子化合物F的路线:
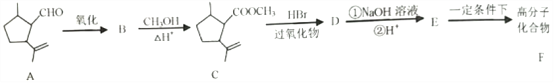
已知: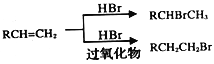
回答下列问题:
(1)C→D的反应类型为__________,C中的官能团名称为__________。
(2)D与NaOH水溶液反应的化学方程式为__________。
(3)①E生成F的化学方程式为__________。
②若F的平均相对分子质量为20000,则其平均聚合度为__________。(填字母)
A.54 B.108 C.119 D.133
(4)E在一定条件下还可以合成含有六元环状结构的G。G的结构简式为__________;满足下列条件的G的同分异构体有__________种。(不考虑立体异构)
①含有1个六元碳环且环上相邻4个碳原子上各连有一个取代基
②1mol该物质与足量新制Cu(OH)2反应产生 2mol砖红色沉淀
(5)参照上述合成路线,写出用![]() 为原料制备化合物
为原料制备化合物![]() 的合成路线___________。(其他试剂任选)
的合成路线___________。(其他试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是中学化学常见的三种物质,它们之间的相互转化关系如下![]() 、Y、Z、E、F为英文字母,部分反应条件及产物略去
、Y、Z、E、F为英文字母,部分反应条件及产物略去![]()

I.若Y是一种易溶于水,且能使品红溶液褪色的无色刺激性气味的气体。
(1)则Y和新制氯水主要成分反应生成两种强酸的化学方程式______________。
(2) Y气体的大量排放会形成酸雨,在工业上可以用足量氨水吸收,化学方程式为________________。
(3)Z的水溶液可以制得某种强酸E。实验室用![]() 的浓
的浓![]() 溶液配制
溶液配制![]() 稀E溶液
稀E溶液![]() 。
。
①制该稀E溶液需要使用的玻璃仪器有胶头滴管、量筒、烧杯、____和_____;
②算所需E浓溶液的体积为___mL(保留1位小数)。
II.若Z是淡黄色固体粉末。在呼吸面具或潜水艇中由Z和CO2制备氧气的化学反应方程式为____。
III.若Z是红棕色气体。
(1)试写出Z与水反应制备另一种强酸F的化学方程式_______。
(2)2.0g铜镁合金完全溶解于![]() 密度为
密度为![]() 质量分数为
质量分数为![]() 的浓F溶液中,得到Z和
的浓F溶液中,得到Z和![]() 和
和![]() 均为浓F溶液的还原产物
均为浓F溶液的还原产物![]() 的混合气体
的混合气体![]() 标准状况
标准状况![]() ,向反应后的溶液中加入
,向反应后的溶液中加入![]() 溶液,当金属离子全部沉淀,得到
溶液,当金属离子全部沉淀,得到![]() 沉淀。则合金中铜与镁的物质的量之比为_____,加入NaOH溶液的体积为_____mL。
沉淀。则合金中铜与镁的物质的量之比为_____,加入NaOH溶液的体积为_____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一含Ni的单核六配位配合物,其阳离子空间结构为八面体。1mol该配合物的稀水溶液与足量![]() 混合生成
混合生成![]() 沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为
沉淀233g;将溶液过滤,滤液与硝酸银溶液混合不生成沉淀。元素分析表明该配合物所含部分原子个数比为![]() 。
。
(1)请画出Ni的价电子排布图:______________________,H、N、O的电负性由大到小的顺序为______________________。
(2)滤液与硝酸银溶液混合不生成沉淀的原因是___________________________________。
(3)该配合物阴离子的中心原子杂化方式为____________,请写出该配合物的化学式:________________。
(4)多原子分子中各原子若在同一平面,且有相互平行的p轨道,则p电子可以在多个原子间运动,形成“离域![]() 键”。下列微粒中存在“离域
键”。下列微粒中存在“离域![]() 键”的是_________
键”的是_________![]() 填序号
填序号![]() 。
。
A.![]()
![]()
![]()
![]() 苯
苯
(5)如图是六方NiAs晶胞的晶胞图及坐标参数,其中![]() ,
,![]() ,
,![]() 。晶胞顶点、棱上小球为Ni,As在体内。
。晶胞顶点、棱上小球为Ni,As在体内。

①写出As的配位数为_________,Ni的配位数为_________。
②已知晶胞参数为![]() ,
,![]() ,则晶胞的密度为____________
,则晶胞的密度为____________![]() 写表达式
写表达式![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】G是药物合成中的一种重要中间体,下面是G的一种合成路线:
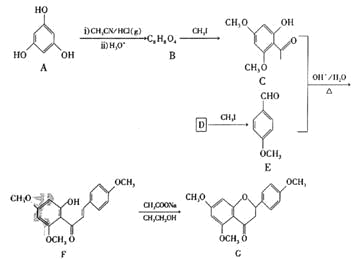
已知:![]()
![]()
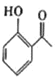 或
或![]()
回答下列问题:
![]() 的结构简式为________,其中所含官能团的名称为_______;B生成C的反应类型为_______。
的结构简式为________,其中所含官能团的名称为_______;B生成C的反应类型为_______。
![]() 的名称是________。
的名称是________。
![]() 由C和E合成F的化学方程式为________。
由C和E合成F的化学方程式为________。
![]() 的同分异构体中,能发生银镜反应且分子结构中含苯环的还有________种,其中核磁共振氢谱上有6组峰,峰面积之比为
的同分异构体中,能发生银镜反应且分子结构中含苯环的还有________种,其中核磁共振氢谱上有6组峰,峰面积之比为![]() 的同分异构体的结构简式为________
的同分异构体的结构简式为________![]() 写出一种即可
写出一种即可![]() 。
。
![]() 参照上述合成路线,以
参照上述合成路线,以![]() 为原料
为原料![]() 其他试剂任选
其他试剂任选![]() ,设计制备巴豆醛
,设计制备巴豆醛![]() 的合成路线________。
的合成路线________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)![]() 可用作食盐的抗结剂,高温下
可用作食盐的抗结剂,高温下![]() 会分解生成
会分解生成![]() 、KCN、
、KCN、![]() 、
、![]() C、C等物质,上述物质中涉及的几种元素的第一电离能由大到小的顺序为______;
C、C等物质,上述物质中涉及的几种元素的第一电离能由大到小的顺序为______;![]() 中,铁原子不是采用
中,铁原子不是采用![]() 杂化的理由是______。
杂化的理由是______。
(2)![]() 气态为单分子时,分子中S原子的杂化轨道类型为______,分子的立体构型为______;
气态为单分子时,分子中S原子的杂化轨道类型为______,分子的立体构型为______;![]() 的三聚体环状结构如图1所示,该结构中
的三聚体环状结构如图1所示,该结构中![]() 键长有a、b两类,b的键长大于a的键长的可能原因为______。
键长有a、b两类,b的键长大于a的键长的可能原因为______。
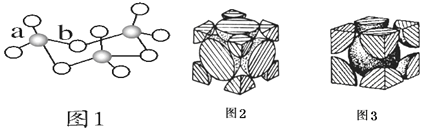
(3)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域![]() 键”
键”![]() 或大
或大![]() 键
键![]() 。大
。大![]() 键可用
键可用![]() 表示,其中m、n分别代表参与形成大
表示,其中m、n分别代表参与形成大![]() 键的电子数和原子个数,如苯分子中大
键的电子数和原子个数,如苯分子中大![]() 键表示为
键表示为![]() 。
。
①下列微粒中存在“离域![]() 键”的是______;
键”的是______;
A.![]()
![]()
![]()
![]()
②![]() 分子中大
分子中大![]() 键可以表示为______;
键可以表示为______;
(4)铁、钾两种单质的堆积方式剖面图分别如图2、图3所示。铁晶体中原子的空间利用率为______![]() 用含
用含![]() 的式子表示
的式子表示![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用如图实验装置制备Cu(NH3)xSO4·H2O。并测量x值。
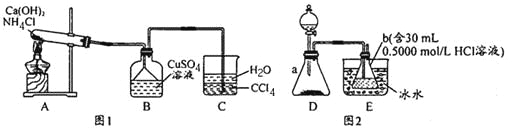
(Cu(NH3)xSO4·H2O制备)见图1
(1)A中发生的化学反应方程式为________________________________。
(2)C中CCl4的作用是______________。
(3)B中先产生蓝色沉淀,随后沉淀溶解变成深蓝色溶液,此溶液中含有Cu(NH3)xSO4,若要从溶液中析出Cu(NH3)xSO4·H2O晶体,可加入试剂___________________________。
(x值的测量)见图2
步骤一:检查装置气密性,称取0.4690g晶体[M=(178+17x)g/mol]于锥形瓶a中
步骤二:通过分液漏斗向锥形瓶a中滴加l0%NaOH溶液至无气体产生为止
步骤三:用0.5000mol/L的NaOH标准溶液液滴定b中剩余HCI,消耗标准溶液液16.00mL
(4)步骤二的反应可理解为Cu(NH3)xSO4与NaOH在溶液中反应,其离子方程式为_________________。
(x值的计算与论证)
(5)计算:x=__________。
该学习小组针对上述实验步骤,提出测量值(x)比理论值偏小的原因如下:
假设1:步骤一中用于称量的天平砝码腐蚀缺损;
假设2:步骤二中_____________________________________________________(任写两点);
假设3 :步骤三中测定结束读数时,体积读数偏小。该假设_______(填“成立”或“不成立”)。
(6)针对假设l,你对实验的处理意见是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:①乙醇蒸气通过红色粉末(CrO3),红色粉末变成绿色粉末(Cr2O3),生成乙醛。②乙醛能还原酸性高锰酸钾溶液。某小组设计如下装置制备少量乙醛。下列说法错误的是( )
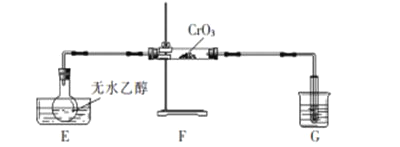
A.水槽E中装热水,烧杯G中装冷水
B.检验乙醛的方法是向反应后的溶液中滴加酸性高锰酸钾溶液
C.E中增加一支温度计,有利于提高乙醇的利用率
D.常采用蒸馏操作分离、纯化粗产品中的乙醛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com