
【题目】C和H2在生产、生活、科技中是非常重要,已知:①2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
②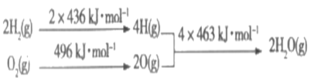
下列推断正确的是
A.C(s)的燃烧热为110.5kJ·mol-1
B.2H2(g)+O2(g)=2H2O(g) △H=+484kJ·mol-1
C.C(s)+H2O(g)=CO(g)+H2(g) △H=+131.5kJ·mol-1
D.将2mol H2O(l)分解成H2(g)和O2(g),至少需要提供4×463kJ的热量
【答案】C
【解析】
A. 1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量为燃烧热;
B. 2molH2断开化学键需要吸收的热量为2mol×436 kJ·mol-1,1mol O2断开化学键需要吸收的热量为1mol×496 kJ·mol-1,4molH原子和2molO原子形成2molH2O(g)时放出的热量为4mol×463 kJ·mol-1,根据△H=反应物的总键能-生成物的总键能进行计算,并书写热化学方程式;
C. 由反应①2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1和反应②2H2(g)+O2(g)=2H2O(g) △H=-484kJ·mol-1,可知反应①-②得C(s)+H2O(g)=CO(g)+H2(g);
D. 根据已知条件②可知2mol H2O(g)分解成H2(g)和O2(g),提供的热量为4×463kJ。
A.1mol C(s)完全燃烧生成稳定的氧化物即CO2时所放出的热量为燃烧热,A项错误;
B.2molH2断开化学键需要吸收的热量为2mol×436 kJ·mol-1,1mol O2断开化学键需要吸收的热量为1mol×496 kJ·mol-1,4molH原子和2molO原子形成2molH2O(g)是时放出的热量为4mol×463 kJ·mol-1,根据△H=反应物的总键能-生成物的总键能,可得△H=2mol×436 kJ·mol-1+1mol×496 kJ·mol-1-4mol×463 kJ·mol-1=-484 kJ·mol-1,因此热化学方程式为:2H2(g)+O2(g)=2H2O(g) △H=-484kJ·mol-1,B项错误;
C.由反应①2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1和反应②2H2(g)+O2(g)=2H2O(g) △H=-484kJ·mol-1,可知反应①-②得C(s)+H2O(g)=CO(g)+H2(g),△H=+131.5 kJ·mol-1,即热化学方程式为:C(s)+H2O(g)=CO(g)+H2(g) △H=+131.5kJ·mol-1,C项正确;
D.根据已知条件②可知2mol H2O(g)分解成H2(g)和O2(g),提供的热量为4×463kJ,D项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】电化学降解法可用于治理水中硝酸盐的污染,其原理如图。下列说法不正确的是( )

A.A为电源正极
B.在Pt电极上发生氧化反应
C.阴极的电极反应式为:2NO3- + 6H2O + 10e- = N2 + 12OH-
D.若电路转移10mol e-,质子交换膜右侧溶液质量减少18g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲要检验不同条件下制得的乙烯,四个实验小组均用图所示装置对所制得的进行除杂、检验,所用试剂X、Y分别见下表所示.你认为设计中不需要除杂的小组是( )
小组 | 乙烯的制备 | 试剂X | 试剂Y |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
C | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | Br2的CCl4 |
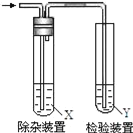
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型药物克利贝特可由物质X在一定条件下制得,下列有关叙述正确的是
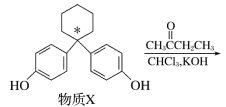
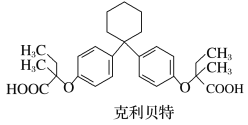
(注:化学上将连接四个不同基团的碳原子称为手性碳原子,可用*标记)
A.苯酚和物质X互为同系物
B.物质X中用*标记的碳原子为手性碳原子
C.1 mol 物质X最多可与8 mol H2发生加成反应
D.用饱和NaHCO3溶液可以鉴别物质X和克利贝特
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类生活、社会可持续发展密切相关,下列说法中不正确的是
A.2020年北京冬奥会速滑服主要材料是聚氨酯,属于有机高分子化合物
B.用CO2生产可降解塑料![]() ,原子利用率100%,符合绿色化学原则
,原子利用率100%,符合绿色化学原则
C.生活中菜叶、鱼骨等垃圾可以作为沼气原料,沼气属于不可再生能源
D.我国成功研制世界最大口径单体碳化硅反射镜,碳化硅属于无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或试剂的选择都合理的是
A.减压过滤时,常用倾析法先转移上部清液,溶液量不超过漏斗容量的2/3,慢慢开大水龙头,待溶液快流尽时再转移下部沉淀
B.用酸性高锰酸钾溶液检验FeCl2和FeCl3混合液中的Fe2+
C.用NaOH溶液除去溶在乙酸乙酯中的乙酸
D.向CoCl2溶液中逐滴加入浓盐酸并振荡,溶液的颜色会从蓝色逐渐变成粉红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源。制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题。
(1)已知; ![]() (g)+H2(g)→
(g)+H2(g)→![]() (g) H=-119.6kJ/mol
(g) H=-119.6kJ/mol
![]() (g)+2H2(g)→
(g)+2H2(g)→![]() (g) H=-237.1kJ/mol
(g) H=-237.1kJ/mol
![]() (g)+3H2(g)→
(g)+3H2(g)→![]() (g) H=-208.4kJ/mol
(g) H=-208.4kJ/mol
请求出![]() (g)+H2(g)→
(g)+H2(g)→![]() (g) H=________kJ/mol
(g) H=________kJ/mol
(2)储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢。
![]() (g)
(g)![]()
![]() (g)+3H2(g)
(g)+3H2(g)
在某温度下,向恒容容器中加入环已烷,其起始浓度为a mol·L-1,平衡时苯的浓度为b mol·L-1,该反应的平衡常数K=_______(用含a、b的关系式表达)。
(3)一定条件下,如下图所示装置可实现有机物的电化学储氢(除目标产物外,近似认为无其它有机物生成)。
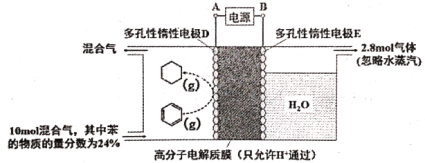
①实现有机物储氢的电极是__________;A 正极 B 负极 C 阴极 D 阳极
其电极反应方程为:___________。
②实验研究表明,当外加电压超过一定值以后,发现电极D产物中苯(g)的体积分数随着电压的增大而减小,其主要原因是相关电极除目标产物外,还有一种单质气体生成,这种气体是__________。已知单质气体为2 mol,求此装置的电流效率η=__________。[η=(生成目标产物消耗的电子数/转移的电子总数)×100%,计算结果保留小数点后1位]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2000年诺贝尔化学奖授予两位美国化学家和一位日本化学家,以表彰他们在导电塑料领域的贡献,他们首先把聚乙炔树脂制成导电塑料。下列关于聚乙炔的叙述错误的是( )
A.聚乙炔是以乙炔为单体发生加聚反应形成的高聚物
B.聚乙炔的化学式为![]() 分子中所有碳原子不可能在同一直线上
分子中所有碳原子不可能在同一直线上
C.聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质
D.聚乙炔树脂不加任何填充物即可成为电的良导体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,对于0.10molL﹣1的氨水,下列判断正确的是
A.与AlCl3溶液反应发生的离子方程式为 Al3++3OH﹣═Al(OH)3↓
B.用HNO3溶液完全中和后,溶液不显中性
C.加水稀释后,溶液中c(NH4+)c(OH﹣)变大
D.1L0.1molL﹣1的氨水中有6.02×1022个NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com