
(19分)根据侯德榜提出的工艺,制碱厂设计生产流程如下:

(1)该流程中可循环利用的物质是 。向母液中通氨气,并加入细小食盐颗粒,冷却析出副产品,通氨气的作用有 。
A.增大NH4+的浓度,使NH4Cl更多地析出
B.使NaHCO3更多地析出
C.使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(2)检验产品纯碱中是否含有NaCl的试剂是 。
(3)某学习小组在实验室模拟制碱有关工艺。
①若利用氯化铵和熟石灰制取氨气,反应方程式是 ,制得的氨气可用下列盛有NaCl溶液的 装置吸收。

②已知用饱和NaNO2与NH4C1溶液加热可制取氮气。该小组模拟工业合成氨设计如下装置:
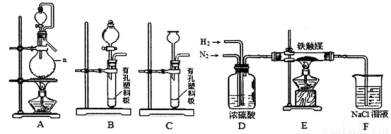
仪器a的名称是 ;氢气的发生装置应选用 ;A装置加热片刻后,即应移去酒精灯以防反应物冲出,其原因是 。装置D的作用是①除去N2、H2中的水;② ;③观察并调节气泡速率,控制N2、H2的比例。
有同学认为:从氨合成器(E装置)中出来的气体连续通入F装置的NaCl溶液中,可能会发生倒吸。你认为是否可能并说明理由 。
(19分)(1)CO2、NaCl(溶液)(2分) AC(2分)
(2)AgNO3溶液、HNO3溶液(2分)
(3)①2NH4Cl + Ca(OH)2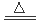 CaCl2 + 2NH3↑ + 2H2O (2分) b(2分)
CaCl2 + 2NH3↑ + 2H2O (2分) b(2分)
②蒸馏烧瓶(1分);B(1分);因本反应放热,不需持续加热(2分);使N2、H2混合均匀(2分)
否(1分),该反应生成的氨气中含有大量难溶于水的N2和H2,氨气溶于水气压降低不是很大(2分)
【解析】
试题分析:(1)合成氨厂产生的氨气及CO2、NaCl发生反应:NH3+ H2O+NaCl=NaHCO3↓+NH4Cl,把产生的NaHCO3过滤出来,灼烧,发生分解反应:2NaHCO3=Na2CO3+H2O+CO2↑;在母液中含有NH4Cl及未反应的NaCl,把NH4Cl分离出来可以做氮肥或金属的除锈试剂;CO2及NaCl可以用于重新反应产生NaHCO3的生产;该流程中可循环利用的物质是CO2、NaCl。NH4Cl是强酸弱碱盐,在溶液中存在水解平衡:NH4++H2O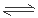 NH3H2O+H+;向母液中通氨气,使盐的水解平衡逆向移动,c(NH4+)增大。并加入细小食盐颗粒,就可以析出更多NH4Cl。溶液中c(Na+)增大,就可以产生更多的NaHCO3。(2)检验产品纯碱中是否含有NaCl的方法是加水溶解,然后加入硝酸酸化,使溶液中的CO32-反应产生CO2气体逸出,再向溶液中加入AgNO3溶液,若产生白色沉淀,就证明含有NaCl,没有白色沉淀,就证明不含有NaCl。所以向溶液中加入试剂是AgNO3溶液、HNO3溶液。(3)①若利用氯化铵和熟石灰制取氨气,反应方程式是2NH4Cl + Ca(OH)2
NH3H2O+H+;向母液中通氨气,使盐的水解平衡逆向移动,c(NH4+)增大。并加入细小食盐颗粒,就可以析出更多NH4Cl。溶液中c(Na+)增大,就可以产生更多的NaHCO3。(2)检验产品纯碱中是否含有NaCl的方法是加水溶解,然后加入硝酸酸化,使溶液中的CO32-反应产生CO2气体逸出,再向溶液中加入AgNO3溶液,若产生白色沉淀,就证明含有NaCl,没有白色沉淀,就证明不含有NaCl。所以向溶液中加入试剂是AgNO3溶液、HNO3溶液。(3)①若利用氯化铵和熟石灰制取氨气,反应方程式是2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑ + 2H2O;a安装一个多孔球泡,但是由于该装置完全浸没在水中,因此不能起到倒吸的作用,错误;b.氨气极容易溶于水,当在导管末端安装一个倒扣的漏斗时,由于漏斗的容积较大,可以吸收大量的氨气,使烧杯中的液面下降。漏斗中的水在重力作用下流到烧杯中,从而防止倒吸现象的发生;正确;c.倒扣的漏斗浸没在溶液中,作用与导管一样;错误;d.导管伸入到液面一下,会引起倒吸,倒吸到左边的空瓶中,但是由于空瓶的另一个导管紧靠瓶底,水溶液会沿导管流到反应装置中,从而引起倒吸现象,错误;因此制得的氨气可用下列盛有NaCl溶液的b装置吸收。②仪器a的名称是蒸馏烧瓶;氢气是用Zn粒与稀盐酸在常温下发生反应制取。Zn是块状固体,盐酸是液体,反应不需要加热,制取的氢气难溶于水,为了使反应随时发生,使反应随时停止,应该使用的发生装置是B;A装置加热片刻后,即应移去酒精灯以防反应物冲出,其原因是本反应放热,不需持续加热;装置D的作用是①除去N2、H2中的水;②使N2、H2混合均匀;③观察并调节气泡速率,控制N2、H2的比例。有同学认为:从氨合成器(E装置)中出来的气体连续通入F装置的NaCl溶液中,可能会发生倒吸。我觉的不可能产生倒吸现象;因为在产生的氨气中还含有大量的不能在NaCl溶液中溶解的N2和H2,所以氨气溶于水气压降低不是很大。
CaCl2 + 2NH3↑ + 2H2O;a安装一个多孔球泡,但是由于该装置完全浸没在水中,因此不能起到倒吸的作用,错误;b.氨气极容易溶于水,当在导管末端安装一个倒扣的漏斗时,由于漏斗的容积较大,可以吸收大量的氨气,使烧杯中的液面下降。漏斗中的水在重力作用下流到烧杯中,从而防止倒吸现象的发生;正确;c.倒扣的漏斗浸没在溶液中,作用与导管一样;错误;d.导管伸入到液面一下,会引起倒吸,倒吸到左边的空瓶中,但是由于空瓶的另一个导管紧靠瓶底,水溶液会沿导管流到反应装置中,从而引起倒吸现象,错误;因此制得的氨气可用下列盛有NaCl溶液的b装置吸收。②仪器a的名称是蒸馏烧瓶;氢气是用Zn粒与稀盐酸在常温下发生反应制取。Zn是块状固体,盐酸是液体,反应不需要加热,制取的氢气难溶于水,为了使反应随时发生,使反应随时停止,应该使用的发生装置是B;A装置加热片刻后,即应移去酒精灯以防反应物冲出,其原因是本反应放热,不需持续加热;装置D的作用是①除去N2、H2中的水;②使N2、H2混合均匀;③观察并调节气泡速率,控制N2、H2的比例。有同学认为:从氨合成器(E装置)中出来的气体连续通入F装置的NaCl溶液中,可能会发生倒吸。我觉的不可能产生倒吸现象;因为在产生的氨气中还含有大量的不能在NaCl溶液中溶解的N2和H2,所以氨气溶于水气压降低不是很大。
考点:考查侯氏制碱的反应原理、气体制取装置的选择、气体的制取、吸收、实验方案的设计与评价。
考点分析: 考点1:物质的制备 试题属性

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年福建省泉州市高三3月月考理综化学试卷(解析版) 题型:选择题
常温下,浓度均为1.0 mol·L-1的NH3·H2O和NH4Cl混合溶液10 mL,测得其pH为9.3。下列有关叙述正确的是
A.加入适量的NaCl,可使c(NH4+) = c(Cl-)
B.滴加几滴浓氨水,c(NH4+)减小
C.滴加几滴浓盐酸, 的值减小
的值减小
D.1.0 mol·L-1的NH4Cl溶液中c(NH4+)比该混合溶液大
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省商丘市高三第一次模拟考试化学试卷(解析版) 题型:推断题
(12分)已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1 :2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质问的转化关系如图所示(某些条件已略去)。请回答:

(1)甲和水反应生成戊和丙的化学方程式为_______________________。
(2)乙与强碱反应的离子方程式:________________________。
(3)丁中所包含的化学键类型有___________________(填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
丙分子溶于水所得溶液中含有的氢键有____________种。
(4)利用单质B与D为原料、含H+的固体物质作电解质,以金属铂为电极材料组成原电池制备丙,则生成产物丙的电极反应式为______________。
(5)反应②中,0.5molNaClO参加反应时,转移1mol电子,其化学方程式为:______________。
(6)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。已知该反应生成l mol乙时放出536kJ热量,其热化学方程式为:___________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三年级3月适应性训练理综化学试卷(解析版) 题型:实验题
(15分)某NiO的废料中有FeO、CuO、Al2O3、MgO、SiO2等杂质,用此废料提取NiSO4和Ni的流程如下:

已知:有关金属离子生成氢氧化物沉淀所需的pH如下图:

(1)滤渣1的主要成分为 。
(2)电解脱铜:金属铜在 极析出。
(3)①用离子方程式解释加入H2O2的作用 。
②加Na2CO3调节溶液的pH至5,则滤渣2的主要成分为 。
(4)从滤液2中获得NiSO4.6H2O的实验操作是 、过滤、洗涤、干燥。
(5)电解浓缩后的滤液2可获得金属镍,其基本反应原理示意图如下:

①A极的电极反应式为 和2H++2e-=H2↑。
②B极附近pH会 (填“增大”、“减小”或“不变”);用平衡移动原理解释B极附近pH变化的原因: 。
③若一段时间后,在A、B两极均收集到11.2L气体(标准状况下),理论上能得到Ni g。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市海淀区高三年级3月适应性训练理综化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.银氨溶液可以用于区分麦芽糖和蔗糖
B.乙醇、乙二醇、丙三醇的沸点依次升高
C.1mol乙酰水杨酸( )最多可以和2mol NaOH反应
)最多可以和2mol NaOH反应
D.可用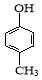 和HCHO 为原料合成
和HCHO 为原料合成
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省枣庄市高三下学期开学初检测试卷理综化学试卷(解析版) 题型:选择题
下述实验操作不能达到实验目的的是
编号 | 实验目的 | 实验操作 |
A | 验证SO2具有漂白性 | 将SO2通入品红溶液中,品红溶液褪色 |
B | 验证Fe2+的还原性 | FeCl2溶液中加入酸性KMnO4溶液,KMnO4溶液褪色 |
C | 检验尿液中是否含有葡萄糖 | 在尿液中加新制的Cu(OH)2悬浊液加热至沸腾 |
D | 验证Na2CO3溶液中存在水解平衡 | 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省文登市高三第二次统考理科综合化学试卷(解析版) 题型:填空题
(20分)近年来大气问题受到人们越来越多的关注。按要求回答下列问题:
Ⅰ.实现反应CH4(g)+CO2(g) 2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义。在2L密闭容器中,通入5mol CH4与5mol CO2的混合气体,一定条件下发生上述反应,测得CH4的平衡转化率与温度、压强的关系如图。
2CO(g)+2H2(g),△H0,对减少温室气体排放和减缓燃料危机具有重要意义。在2L密闭容器中,通入5mol CH4与5mol CO2的混合气体,一定条件下发生上述反应,测得CH4的平衡转化率与温度、压强的关系如图。

则p1、p2、p3、p4由大到小的顺序 ,该反应的正反应是______(填“吸热”或“放热”)反应,当1000℃甲烷的转化率为80%时,该反应的平衡常数K=________。
Ⅱ.PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) △H1=-574kJ·mol-1
CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H2=-1160kJ·mol-1
CH4(g) + 2NO2 (g) = N2(g) + CO2(g) + 2H2O(g) △H3
则△H3= ,如果三个反应的平衡常数依次为K1、K2、K3,则K3=__________(用K1、K2表示)
(2)实验室可用NaOH溶液吸收SO2,某小组同学在室温下,用pH传感器测定向20mL0.1mol·L-1NaOH溶液通入SO2过程中的pH变化曲线如图所示。
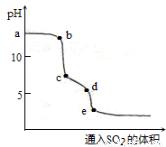
①ab段发生反应的离子方程式为________________。
②已知d点时溶液中溶质为NaHSO3,此时溶液中离子浓度由大到小的顺序为_______,如果NaHSO3的水解平衡常数Kh=1×10-12mol·L-1,则该温度下H2SO3的第一步电离平衡常数Ka=________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三第一次模拟考试理科综合化学试卷(解析版) 题型:选择题
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中只生成氧化物
C.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2的混合溶液在阴极上依次析出Cu、Fe、Al
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省泰安市高三下学期一模理科综合化学试卷(解析版) 题型:填空题
【化学—物质结构与性质】
碳是形成化合物种类最多的元素。
(1)C、N、O三种元素的第一电离能由大到小的顺序为______,碳的最简单气态氢化物中心原子的杂化类型为___________。
(2)类肉素[(SCN)2]的结构式为N C—S—S—C
C—S—S—C N。其分子中
N。其分子中 键和
键和 键的个数比为__________;该物质对应的酸有两种,理论上硫氰酸(H—S—C
键的个数比为__________;该物质对应的酸有两种,理论上硫氰酸(H—S—C N)的沸点低于异硫氰酸(H—N=C=S)的沸点,其原因是___________________。
N)的沸点低于异硫氰酸(H—N=C=S)的沸点,其原因是___________________。
(3)位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同的元素,其基态原子的价层电子排布式为 ____________。
(4)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能,其晶胞结构如图所示(其中·为碳原子,○为硅原子)。每个碳原子周围与其距离最近的硅原子有_____个;设晶胞边长为a cm,密度为b g·cm-3,则阿伏加德罗常数可表示为__________(用含a、b的式子表示).

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com