
【题目】实验室制备1,2-二溴乙烷的反应原理如下所示:
第一步:CH3CH2OH ![]() CH2=CH2+H2O;
CH2=CH2+H2O;
第二步:乙烯与溴水反应得到1,2-二溴乙烷。
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140 ℃下脱水生成乙醚(CH3CH2OCH2CH3)。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):
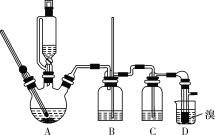
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g/cm3) | 0.79 | 2.2 | 0.71 |
沸点/(℃) | 78.5 | 132 | 34.6 |
熔点/(℃) | -130 | 9 | -116 |
请回答下列问题:
(1)写出乙烯与溴水反应的化学方程式:___________________________________。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是___________(填字母代号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是__________________。
(4)在装置C中应加入_________(填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
a.水 b.浓硫酸
c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__________(填“上”或“下”)层。
(6)若产物中有少量未反应的Br2,最好用________(填字母代号)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用__________的方法除去。
(8)判断该制备反应已经结束的最简单方法是___________________________。
【答案】 CH2=CH2+Br2―→CH2BrCH2Br d 安全瓶的作用 c 下 b 蒸馏 溴的颜色完全褪去
【解析】(1)根据乙烯的加成反应书写;
(2)根据乙醇在浓硫酸做催化剂、脱水剂条件下加热到140度发生副反应生成乙醚分析解答;
(3)从防止气体压强突然增大角度分析解答;
(4)根据二氧化硫、二氧化碳的性质分析解答;
(5)根据1,2-二溴乙烷密度大于水,不溶于水分析解答;
(6)根据溴的性质类似与氯气,分析解答;
(7)依据乙醚与1,2-二溴乙互溶,二者熔沸点不同选择分离方法;
(8)根据溴水为橙黄色,如果完全反应,则D溶液中不存在溴分析解答。
(1)乙烯与溴水发生加成反应,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(2)乙醇在浓硫酸做催化剂、脱水剂条件下加热到140度发生副反应生成乙醚,所以要制备乙烯应尽可能快地把反应温度提高到170℃,减少副产物乙醚的生成,故答案为:d;
(3)装置B的长玻璃管可以平衡装置中的压强,起安全瓶的作用,故答案为:安全瓶;
(4)浓硫酸具有脱水性,强氧化性,能够与乙醇脱水生成的碳发生氧化还原反应生成二氧化硫、二氧化碳气体,二者为酸性氧化物能够与碱液反应,为除去乙烯中的二氧化硫、二氧化碳气,应选择碱性溶液;a.二氧化碳水溶性较小,吸收不充分,故a不选;b.二氧化碳、二氧化硫与浓硫酸不反应,不能用浓硫酸吸收,故b不选;c.二氧化硫、二氧化碳气为酸性氧化物,能够与氢氧化钠溶液反应而被吸收,故c选;d.碳酸氢钠不能吸收二氧化碳,故d不选;故选:c;
(5)1,2-二溴乙烷密度大于水,不溶于水,所以:将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层;故答案为:下;
(6)a.溴更易溶于1,2-二溴乙烷,用水无法除去溴,故a不选;b.常温下Br2和氢氧化钠发生反应:2NaOH+Br2═NaBr+NaBrO+H2O,再分液除去,但1,2-二溴乙烷在氢氧化钠水溶液、加热条件下容易发生水解反应,低温下,可用氢氧化钠出去溴杂质,故b选;c.NaI与溴反应生成碘,碘与1,2-二溴乙烷互溶,不能分离,故c不选;d.酒精与1,2-二溴乙烷互溶,不能除去混有的溴,故d不选;故选b;
(7)乙醚与1,2-二溴乙互溶,二者熔沸点不同选择,应用蒸馏的方法分离二者;故答案为:蒸馏;
(8)溴水为橙黄色,如果完全反应生成的1,2-二溴乙烷无色,所以可以通过观察D中溴水是否完全褪色判断制备反应已经结束;故答案为:D中溴水完全褪色。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiCIO4。溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。

回答下列问题:
(1)外电路的电流方向是由____极流向____极。(填字母)
(2)电池正极反应式为__ __。
(3)是否可用水代替电池中的混合有机溶剂?____(填“是”或“否”),原因是_________ ___。
(4)MnO2可与KOH和KClO3,在高温下反应,生成K2MnO4,反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关描述中正确的是( )
A.牺牲阳极的阴极保护法是应用电解原理防止金属的腐蚀
B.AlCl3溶液和Al2(SO4)3溶液分别加热蒸发,所得固体的成分相同
C.室温时将Na2CO3溶液加水稀释后,再恢复至室温,pH和KW均减小
D.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化亚铜可用于彩色照相,是一种白色结晶状粉末,见光分解,在空气中会慢慢氧化成绿色,溶于氢溴酸、盐酸、硝酸和氨水,在热水中也会发生分解。实验室制备CuBr的装置示意图和步骤如下:
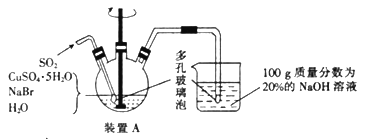
实验步骤:
①在装置A中加人50.0 g CuSO4o5H2O、30.9 g NaBr、150 mL蒸馏水,60℃时不断搅拌,以适当流速通入SO2;
②溶液冷却后倾去上层清液,在避光的条件下过滤;
③依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤;
④在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6 g。
回答下列问题:
(1)步骤②中过滤需要避光的原因是________________________________________________。
(2)步骤①中实验所用蒸馏水事先要进行的处理操作是_______________,控制反应在60℃条件下进行,实验中可采取的措施是________________________。
(3)步骤③中洗涤剂需“溶有SO2”的原因是__________________________________;最后洗涤剂改用乙醚的目的是_____________________________________。
(4)装置A中反应生成CuBr的离子方程式为__________________________;说明反应已完成的现象是_____________________________________________________。
(5)本实验产品的产率是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝阳极氧化处理后形成的氧化膜比铝的天然氧化膜耐磨性、耐腐蚀性及装饰性有明显的提高,工业中以铝为阳极,置于硫酸溶液中电解,装置如图,下列说法正确的是( ) 
A.阳极电极方程式为Al﹣3e+6OH﹣=Al2O3+3H2O
B.随着电解的进行,溶液的pH逐渐增大
C.当阴极生成气体3.36L(标况)时,阳极增重2.4g
D.电解过程中H+移向Al电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯氧布洛芬钙G是评价较好的解热、镇痛、消炎药,下面是它的一种合成路线(具体反应条件和部分试剂略)

已知①氯化亚砜(SOCl2)可与醇发生反应,醇的羟基被氯原子取代而生成氯代烃。
② (X表示卤素原子)
(X表示卤素原子)
③R-X+NaCN![]() RCN+NaX
RCN+NaX
回答下列问题:
(1)写出D的结构简式:_______________。
(2)B→C的反应类型是___________;F中所含的官能团名称是_________。
(3)写出F和C在浓硫酸条件下反应的化学方程式_______________。
(4)A的同分异构体中符合以下条件的有______种(不考虑立体异构)
①属于苯的二取代物;②与FeCl3溶液发生显色反应。
其中核磁共振氢谱图中共有4个吸收峰的分子的结构简式为____________。
(5)结合上述推断及所学知识,参照上述合成路线任选无机试剂设计合理的方案,以苯甲醇(![]() )为原料合成苯乙酸苯甲酯(
)为原料合成苯乙酸苯甲酯(![]() )写出合成路线__________,并注明反应条件。
)写出合成路线__________,并注明反应条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)具有较强的还原性,还能与中强酸反应,在精细化工领域应用广泛。将SO2通入按一定比例配制成的Na2S和Na2CO3的混合溶液中,可制得Na2S2O3·5H2O(大苏打)。
已知:Na2S、Na2CO3、Na2SO3、NaHCO3溶液呈碱性;NaHSO3溶液呈酸性。
(1)实验室用Na2SO3和硫酸制备SO2,可选用的气体发生装置是________(填字母代号)。
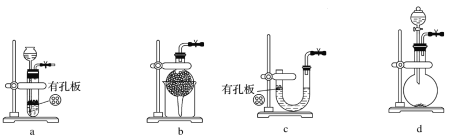
(2)向Na2S和Na2CO3的混合溶液中不断通入SO2气体的过程中,发现:
①浅黄色沉淀先逐渐增多,反应的化学方程式为_____________________________________;
②当浅黄色沉淀不再增多时,反应体系中有无色无味的气体产生,反应的化学方程式为________________________________;
③浅黄色沉淀逐渐减少(这时有Na2S2O3生成);
④继续通入过量的SO2,浅黄色沉淀又会逐渐增多,反应的化学方程式为________________________。
(3)制备Na2S2O3时,为了使反应物利用率最大化,Na2S和Na2CO3的物质的量之比应为____________;通过反应顺序,可比较出:温度相同时,同物质的量浓度的Na2S溶液和Na2CO3溶液pH更大的是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原子的电子排布式为1s22s22p63s23p63d54s2,下列说法中不正确的是( )
A. 该元素原子中共有25个电子
B. 该元素原子核外有4个能层
C. 该元素原子最外层共有2个电子
D. 该元素原子M电子层共有8个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年新学期初,市教育局在全市中小学开展了“节约用水用电,倡导绿色简约生活”的活动。下列做法不应该提倡的是
A.路远的同学可乘公交车上学B.作业不要使用修正带或涂改液
C.将化学实验室的废水直接排入水池D.养成随手关水关灯的习惯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com